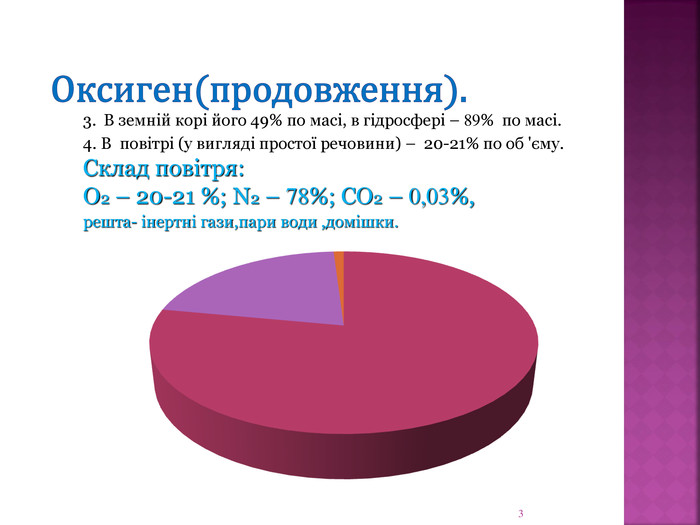
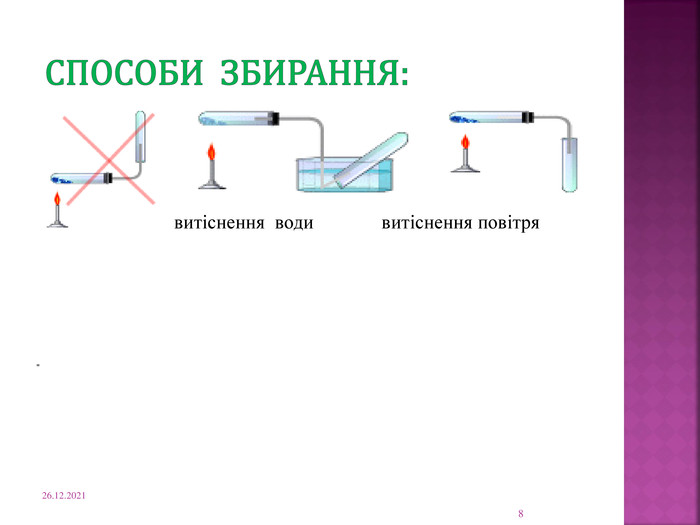
Презентація "Оксиген як хімічний елемент.Кисень як проста речовина."
Про матеріал
Матеріал до уроку при вивченні теми:"Кисень"
Презентація "Оксиген як хімічний елемент.Кисень як проста речовина." Перегляд файлу
Зміст слайдів


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку