Презентация "Первый закон термодинамики"
Про матеріал
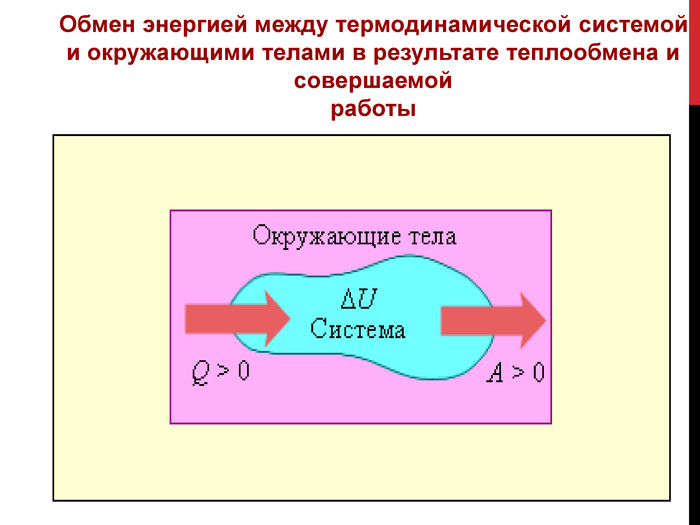
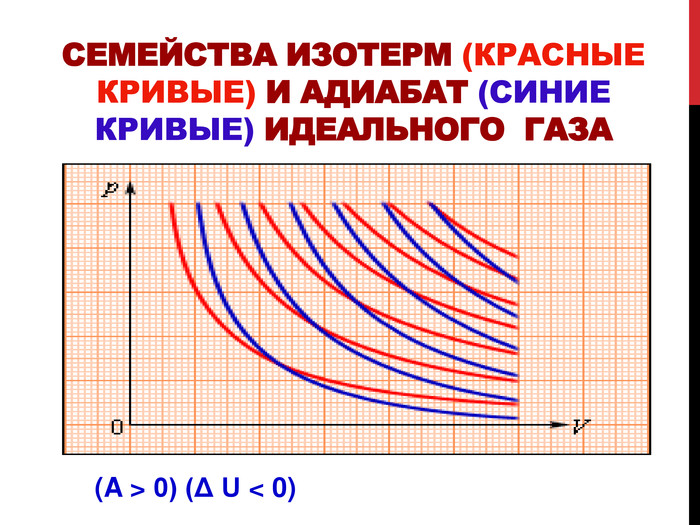
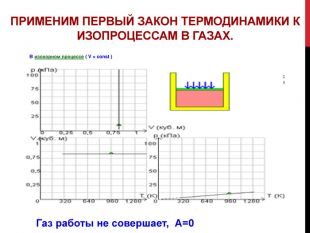
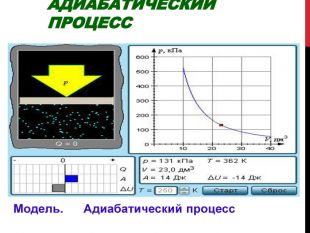
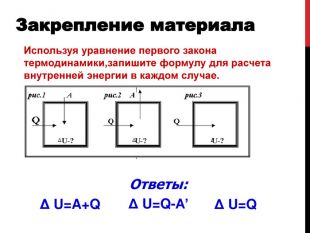
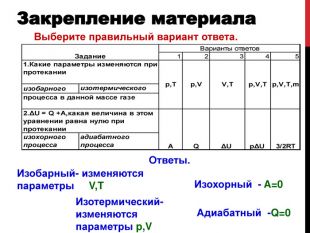
Представленная работа поможет ученикам старших классов изучить закон сохранения энергии, распространенный на тепловые явления — первый закон термодинамики, дает понятие адиабатического процесса. Изложение темы презентации в доступной форме. В завершение, автор предлагает ученикам ряд вопросов для закрепления материала. Перегляд файлу
Зміст слайдів
ppt
До підручника
Фізика (академічний рівень, профільний рівень) 11 клас (Бар’яхтар В.Г., Божинова Ф.Я., Кирюхіна О.О., Кірюхін М.М.)
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку