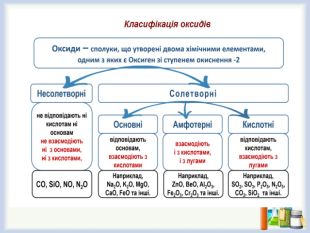
Презентація "Поняття про амфотерні оксиди і гідроксиди"
Про матеріал
Презентація з хімії для 8 класу "Поняття про амфотерні оксиди і гідроксиди" Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки
-
дякую.


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку


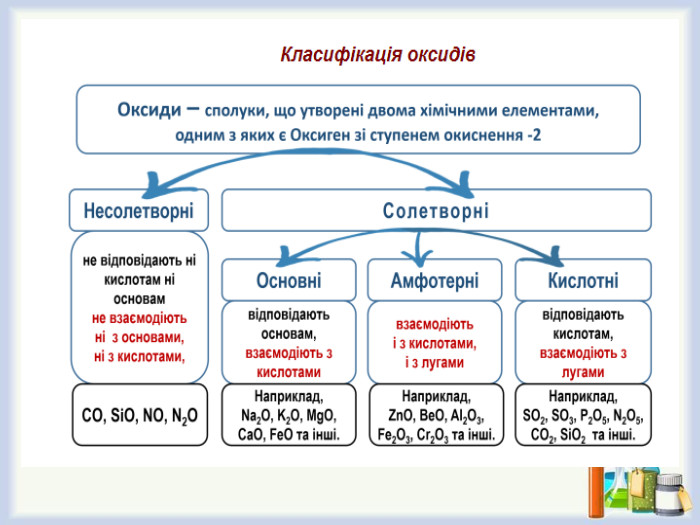






![Хімічні властивостіУ розчинах амфотерних гідроксидів індикатори не змінюють свого забарвлення. Взаємодія з кислотами. Zn(OH)2 + 2 HCl → Zn. Cl2 + 2 H2 O2. Взаємодія з лугамипри сплавлянні Zn(OH)2 + 2 Na. OH → Na2 Zn. O2 + 2 H2 O Натрій цинкатв розчині Zn(OH)2↓ + 2 Na. OH = Na2[Zn(OH)4] Натрій тетрагідроксоцинкат Хімічні властивостіУ розчинах амфотерних гідроксидів індикатори не змінюють свого забарвлення. Взаємодія з кислотами. Zn(OH)2 + 2 HCl → Zn. Cl2 + 2 H2 O2. Взаємодія з лугамипри сплавлянні Zn(OH)2 + 2 Na. OH → Na2 Zn. O2 + 2 H2 O Натрій цинкатв розчині Zn(OH)2↓ + 2 Na. OH = Na2[Zn(OH)4] Натрій тетрагідроксоцинкат](/uploads/files/4514985/459256/519669_images/9.jpg)


![Завдання 3. Здійсніть перетворення. Дайте назви сполукам. Зазначте типи хімічних реакцій. Al→Al2 O3→Al. Cl3→Al(OH)3→Na3[Al(OH)6] ↓ Na3 Al. O3 Завдання 3. Здійсніть перетворення. Дайте назви сполукам. Зазначте типи хімічних реакцій. Al→Al2 O3→Al. Cl3→Al(OH)3→Na3[Al(OH)6] ↓ Na3 Al. O3](/uploads/files/4514985/459256/519669_images/12.jpg)