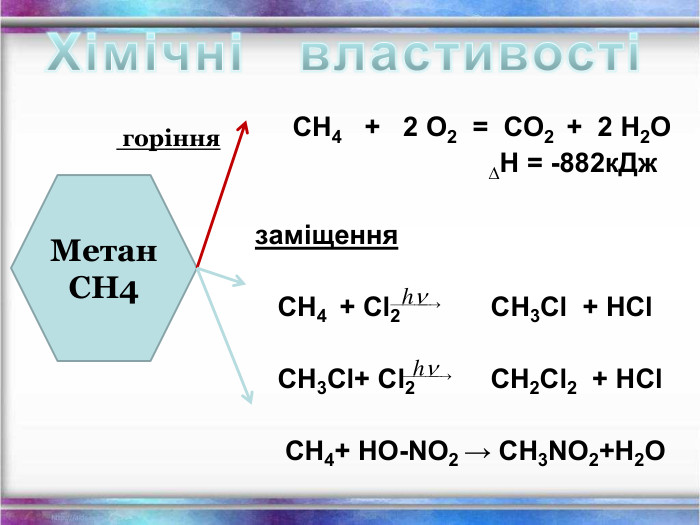
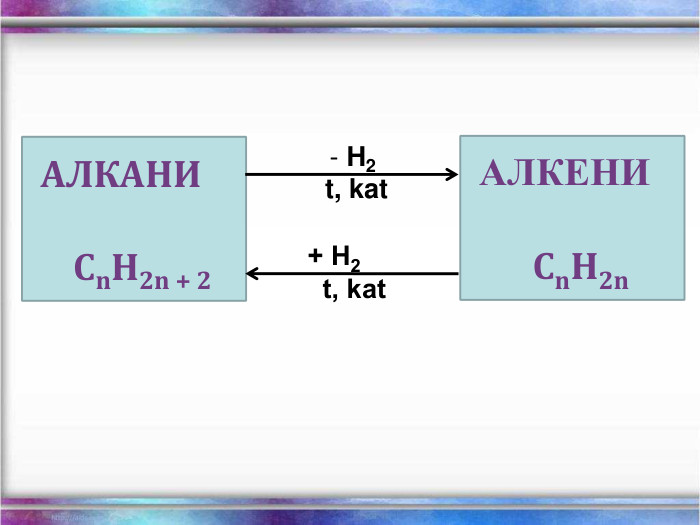
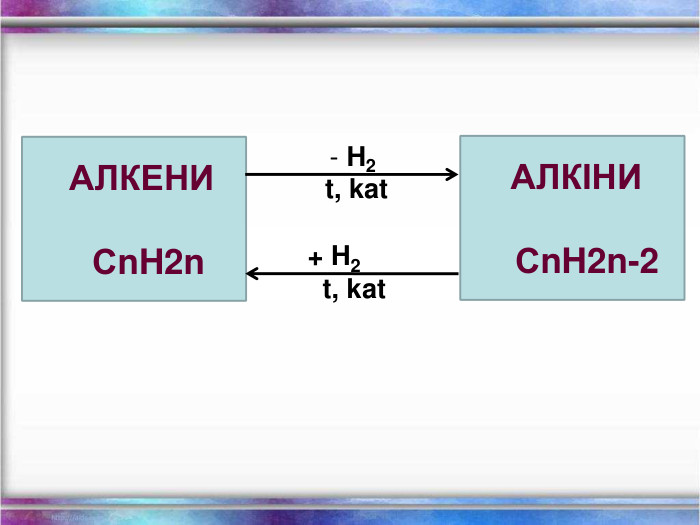
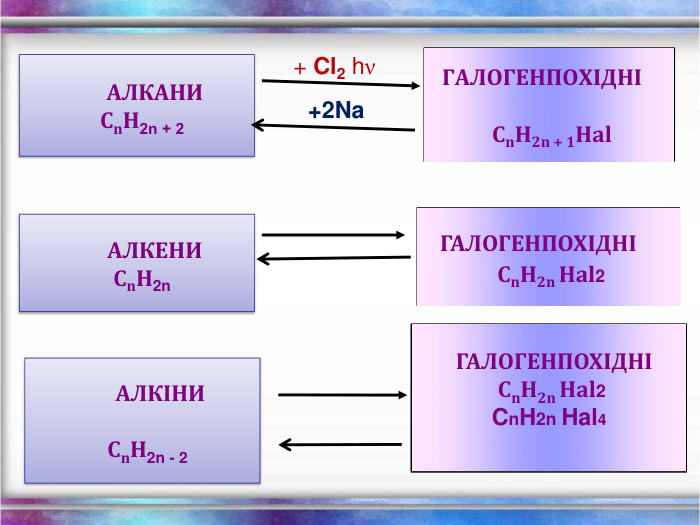
Презентація Повторення Склад, властивості, застосування окремих представників вуглеводнів (метан, етан, етен, етин)
Про матеріал
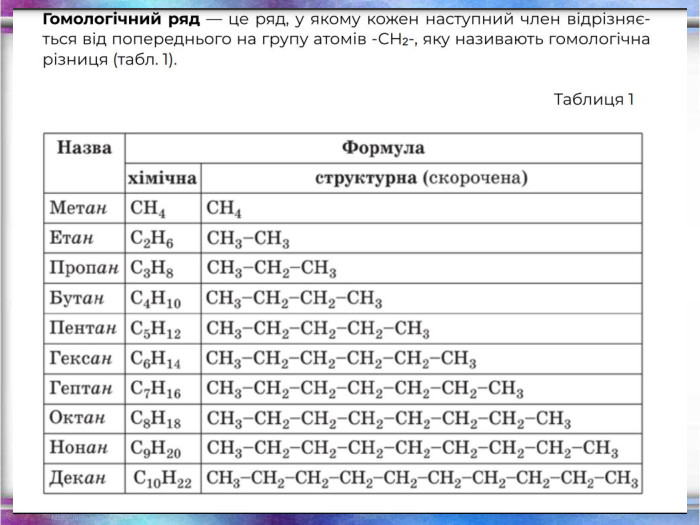
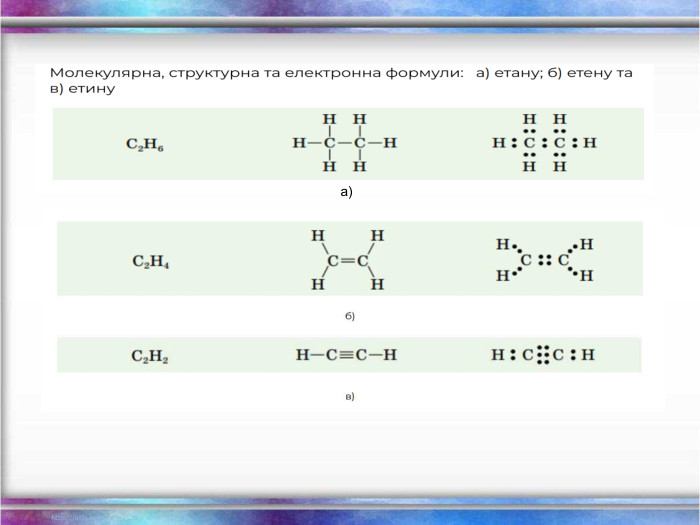
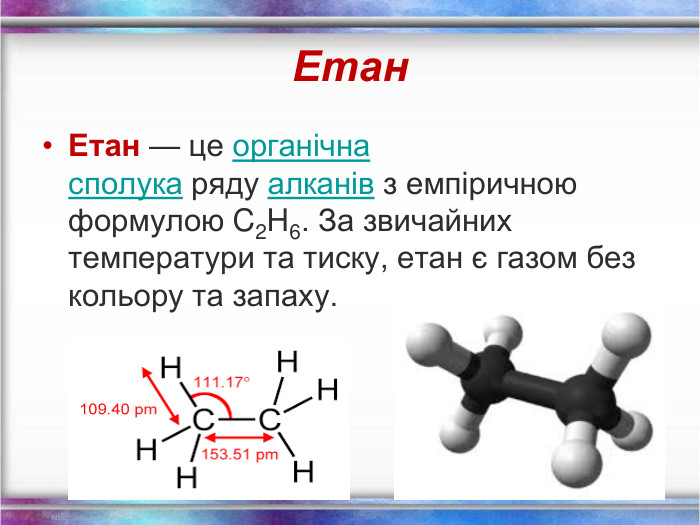
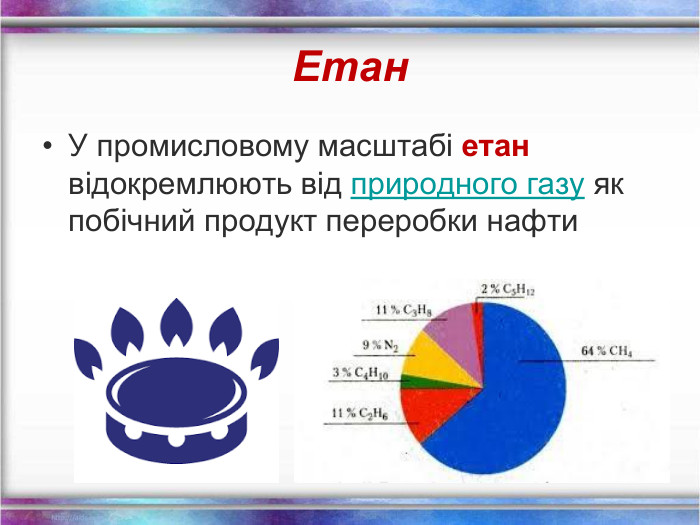
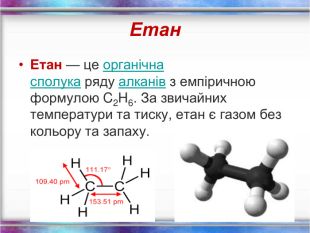
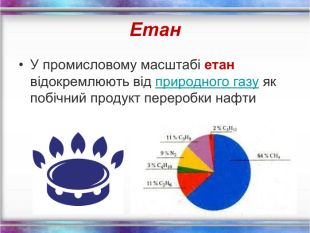
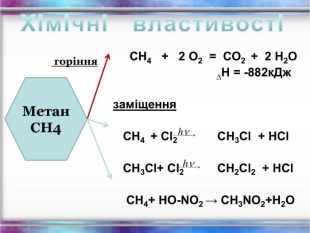
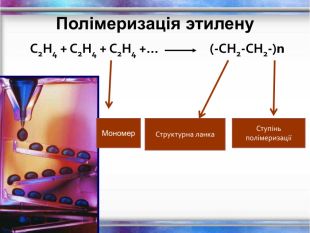
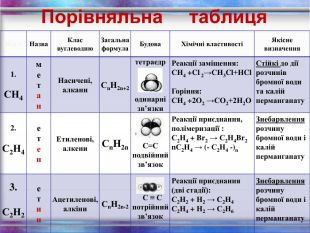
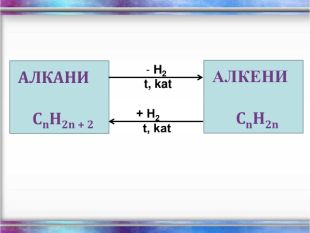
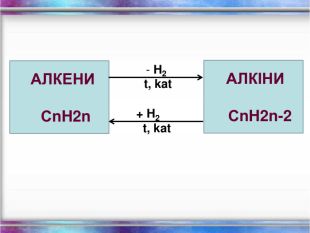
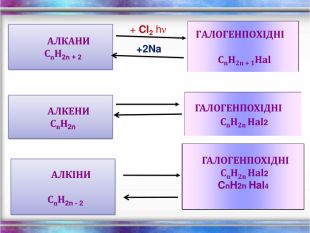
Повторення за курс 9 класу Склад, властивості, застосування окремих представників вуглеводнів (метан, етан, етен, етин) Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку