Презентація "Реакції обміну між розчинами електролітів, умови їх перебігу. Йонно-молекулярні рівняння хімічних реакцій. Завдання"
Про матеріал
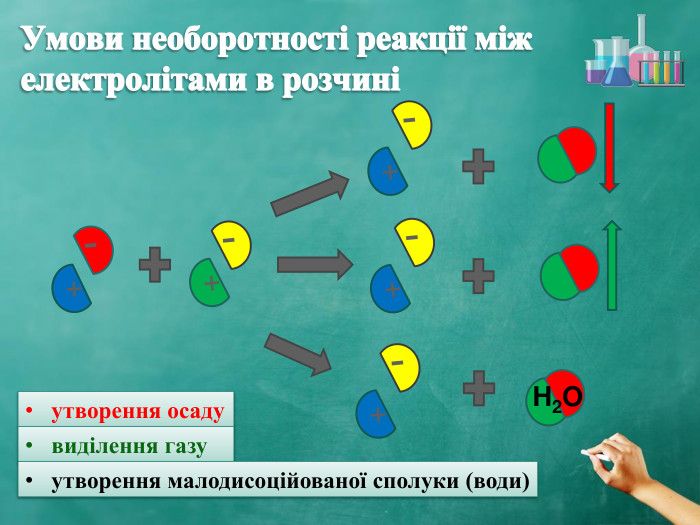
Мета: 1. З’ясувати умови протікання реакцій йонного обміну.
2. Навчитися писати йонні рівняння реакцій.
3. Узагальнити набуті знання.
Перегляд файлу
Зміст слайдів
pptx
До підручника
Хімія 9 клас (Григорович О.В.)
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку