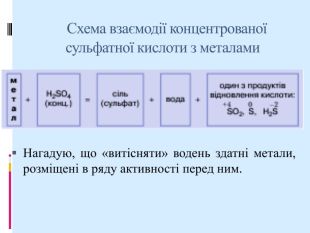
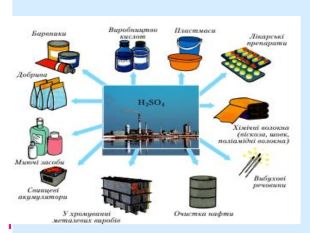
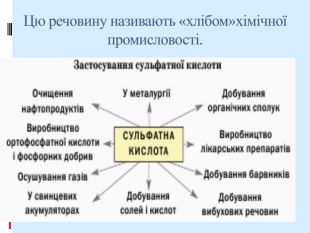
Презентація:"Сульфатна кислота. Фізичні і хімічні властивості. Сульфати. Якісна реакція на сульфат-іон. Значення сульфатної кислоти"

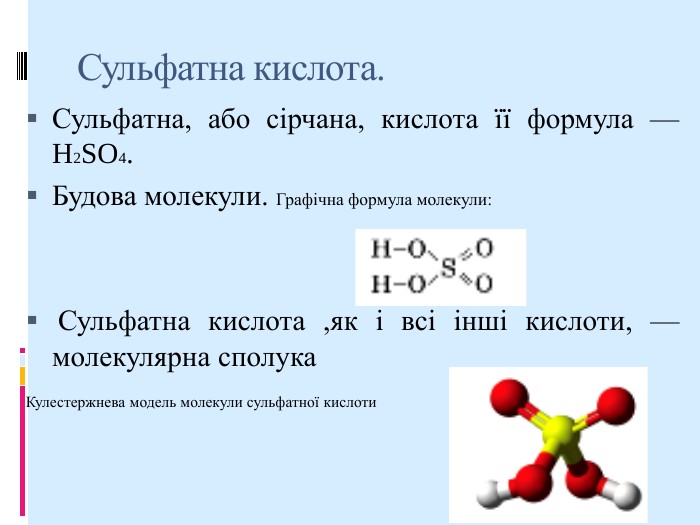
















Фізичні властивості. За звичайних умов чиста сульфатна кислота — безбарвна оліїста рідина без запаху, майже удвічі важча за воду (ρ = 1,83 г/см3). Температура плавлення сполуки становить +10,3 °С, а кипіння +280 °С. Під час кипіння кислота починає розкладатися на сульфур(VI) оксид і воду. Сульфатна кислота необмежено розчиняється у воді, тобто змішується з нею в будь яких співвідношеннях з утворенням розчину.
Потрібно знати Розчинення кислоти у воді супроводжується виділенням великої кількості теплоти. Для того щоб із концентрованої сульфатної кислоти виготовити її розбавлений розчин, кислоту доливають у воду, а не навпаки. Тоді температура рідини зростає повільніше, і вдається запобігти її закипанню й розбризкуванню.
Хімічні властивості. Сульфатна кислота завдяки наявності в молекулі двох ковалентт них полярних зв’язків О–Н є двохосновною. Її дисоціація за першою стадією в розбавленому розчині відбувається майже повністю (це сильна кислота), а за другою — частково: H2SO4→H + HSO4; HSO4→H + SO4Іˉ. Проте у йонноомолекулярних рівняннях сульфатну кислоту записують такою сукупністю йонів: 2H +SO4Іˉ.
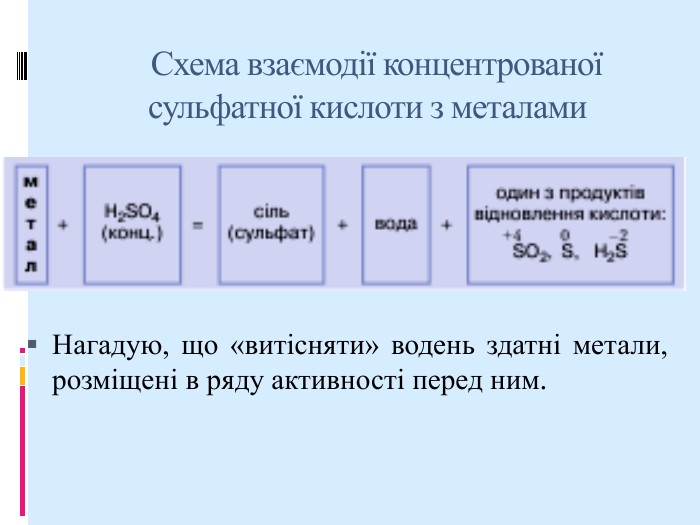
Реакції з металами. взаємодіє майже з усіма металами. Можливість цих реакцій, а також склад їх продуктів залежать від концентрації кислоти і хімічної активності металу. Метал завжди є відновником. Тому сульфатна кислота, реагуючи з ним, буде окисником і відновлюватиметься. +1 +6 –2 У молекулі H2SO4 можуть відновлюватися (зменшувати ступінь окиснення) два елементи — Гідроген і Сульфур. Якщо з металом взаємодіє розбавлена сульфатна кислота, то відновлюється Гідроген. Продукти реакції — сульфат металічного елемента і водень: 2Al + 3H2SO4 (розб.) = Al2(SO4)3+ 3H2↑.
Із розбавленою сульфатною кислотою не реагують мідь а), ртуть, золото, платина, інші хімічно пасивні метали. Якщо реагентом є концентрована сульфатна кислота, то відновлюється Сульфур. Із концентрованою кислотою реагують також метали, розміщені в ряду активності після водню (крім золота,платини).
Сульфати. Сульфатна кислота утворює солі, загальна назва яких — сульфати Більшість сульфатів розчиняється у воді. При випарюванні їх розчинів часто виділяються кристалогідрати, наприклад CuSO4•5H2O, FeSO4•7H2O, Al2(SO4)3•18H2O. Малорозчинними є солі CaSO4 і Ag2SO4, а практично нерозчинними — BaSO4 і PbSO4. Утворення осаду барій сульфату використовують як якісну реакцію на йони SO4Іˉ
Найважливіші природні сульфати гіпсСаSO4·2Н2О; глауберова сільNa2SO4·10H2О; гірка сільMgSO4·7H2О. Із наведених формул стає зрозуміло, що це кристалогідрати, тобто вони містять кристалізаційну воду, яка при нагріванні випаровується. На цій властивості кристалогідратів ґрунтується виробництво алебастру 2СаSO4·Н2О з природного гіпсу, який нагрівають до 120–190 °С, у наслідок чого він втрачає частину води. При змочуванні водою кімнатної температури алебастр легко приєднує воду й знову перетворюється на гіпс. Це відбувається щоразу при накладанні гіпсових пов’язок на травмовані частини тіла, під час виготовлення гіпсових виробів художнього та будівельного призначення.
Глауберову сіль Na2SO4·10H2О застосовують у виробництві скла, соди, фарб, у медицині. Гірку сіль MgSO4·7H2О використовують в обробці тканин, дубінні шкіри, виготовленні медичних препаратів. Купрум(ІІ) сульфат, пентагідрат, або мідний купорос CuSO4•5H2O,застосовують у сільському господарстві як засіб проти хвороб і шкідників рослин.
Охорона навколишнього середовища від забруднення викидами сульфуровмісних речовин. Серед сульфуровмісних забрудників навколишнього середовища найбільш шкідливими є сульфур(ІV) оксид і гідроген сульфід, або сірководень. Щодо гідроген сульфіду, то потрібно наголосити на високій токсичності цієї газуватої речовини з неприємним запахом тухлих яєць (утворюється при гнитті білка курячого яйця й спричинює його неприємний запах).
Поняття про кислотні дощі та причини їх виникнення. Чи доводилося вам спостерігати, як після довгоочікуваного літнього дощу рослини замість того, щоб рости й давати врожай, жовкнуть,в’януть і навіть гинуть (досить часто це трапляється з огірками)? З великою ймовірністю можна стверджувати, що дощ був не звичайний, а кислотний, і завдав шкоди рослинам. Кислотні дощі пошкоджують листки, руйнують їх захисні воскові покриви, через що ті стають легкопроникними для комах, шкідливих грибів і мікроорганізмів. Окрім рослин, кислотні дощі завдають шкоди тваринам,водоймам, ґрунтам. Хімічний аналіз кислотних дощів показує наявність у них сульфатної та нітратної кислот. Поява цих речовин — наслідок розглянутих хімічних перетворень оксидів Сульфуру і Нітрогену в атмосфері. Кислотний дощ— це дощ, що містить певну кількість кислот, утворених унаслідок взаємодії з водою наявних у повітрі таких забруднювачів, як оксиди Сульфуру і Нітрогену. Щороку внаслідок спалювання твердого палива, роботи двигунів внутрішнього згорання, промислових викидів заводів по виробництву сульфатної і нітратної кислот концентрація цих оксидів у повітрі збільшується. Тому кислотні дощі створюють реальну загрозу людині, рослинному й тваринному світу.
Фізіологічна дія гідроген сульфіду проявляється в тому, що він блокує дихальний центр. Смертельною дозою для людини є вдихання протягом 5–10 хв повітря з об’ємною часткою гідроген сульфіду 0,08%. Забруднюють повітря сульфуровмісними речовинами викиди нафтопереробних заводів, теплові електростанції.
Охорона навколишнього середовища полягає насамперед у зменшенні викидів, а отже, у модернізації виробництва, запровадженні технології замкненого циклу, коли гази, що є відходами названих виробництв, використовують як сировину для інших виробництв. Користь від цього подвійна — не забруднюється навколишнє середовище, а вироблена з гідроген сульфідних відходів нафтопереробної промисловості сульфатна кислота має найменшу вартість. Удосконаленням технології виробництва сульфатної кислоти. займався український хімік Іван Євграфович Ададуров (1879–1938).
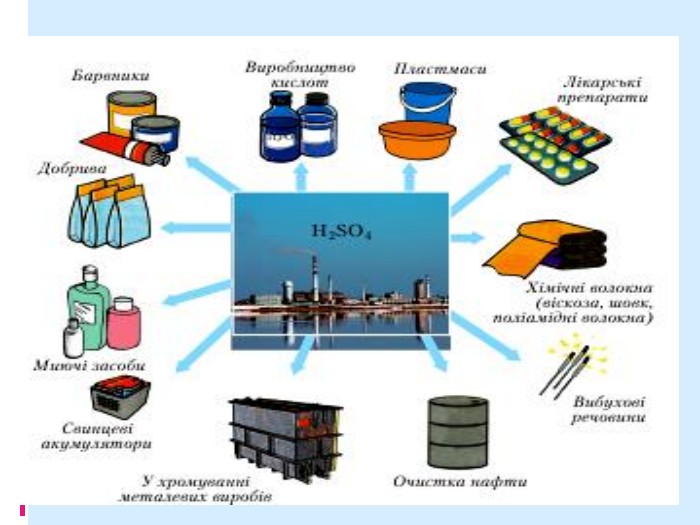
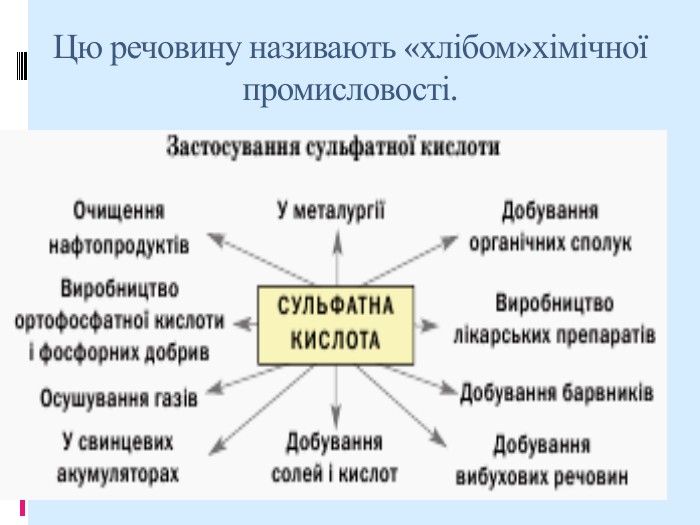
ВИСНОВКИ Сульфатна кислота H2SO4 — безбарвна оліїста рідина без запаху, яка необмежено розчиняється у воді. Це сильна й нелетка двохосновна кислота. Вона реагує з металами, основними й амфотерними оксидами, основами, амфотерними гідроксидами, а також солями з утворенням сульфатів. Сульфатну кислоту та її солі широко використовують у різних галузях.


про публікацію авторської розробки
Додати розробку