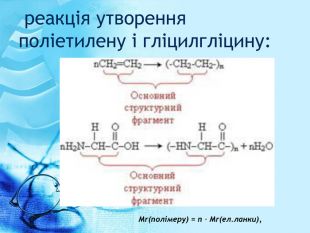
Презентація "Високомолекулярні сполуки"
Про матеріал
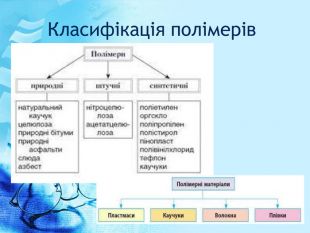
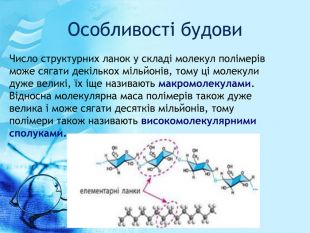
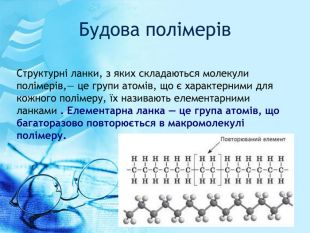
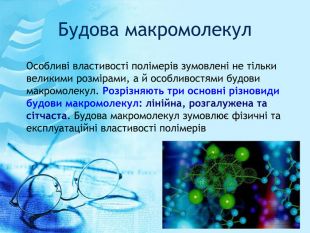
Презентація до уроку на тему: "Високомолекулярні сполуки". Презентація підготовлена за підручником О.В. Григорович "Хімія 10 клас" (рівень стандарту). - Харьків: Ранок, 2018. - С.192-199. У розробці даються поняття про високомолекулярні сполуки та молімери, висвітлені питання, що стосуються властивостей молімерів, будови макромолекул, реакції полімеризації та поліконденсації, наведено приклади розв'язування задач. Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку







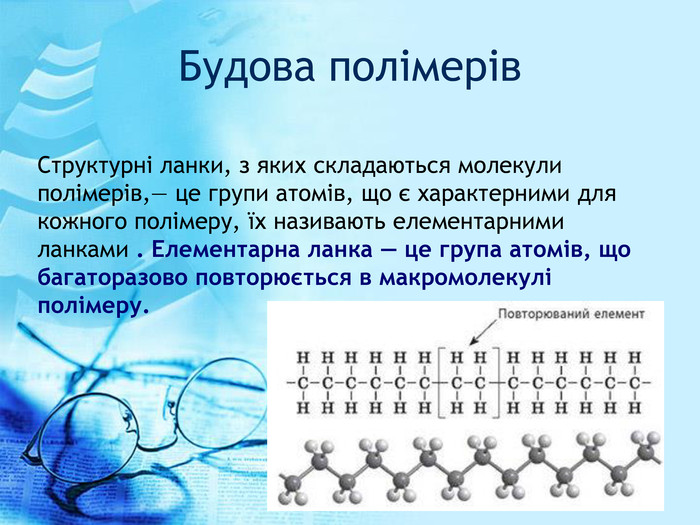










![Назву лінійного полімеру утворюють додаванням префікса «полі»: а) до назви складової повторюваної ланки, яку пишуть у дужках (систематичні назви); б) до назви мономера, з якого одержали полімер (напівсистематичні назви, які IUPAC рекомендує використовувати для найпоширеніших полімерів). Назву складової повторюваної ланки утворюють за правилами хімічної номенклатури. [–CH2–CH2–]n Полі (етилен), поліетилен Назви полімерів Назву лінійного полімеру утворюють додаванням префікса «полі»: а) до назви складової повторюваної ланки, яку пишуть у дужках (систематичні назви); б) до назви мономера, з якого одержали полімер (напівсистематичні назви, які IUPAC рекомендує використовувати для найпоширеніших полімерів). Назву складової повторюваної ланки утворюють за правилами хімічної номенклатури. [–CH2–CH2–]n Полі (етилен), поліетилен Назви полімерів](/uploads/files/197377/238059/257509_images/23.jpg)
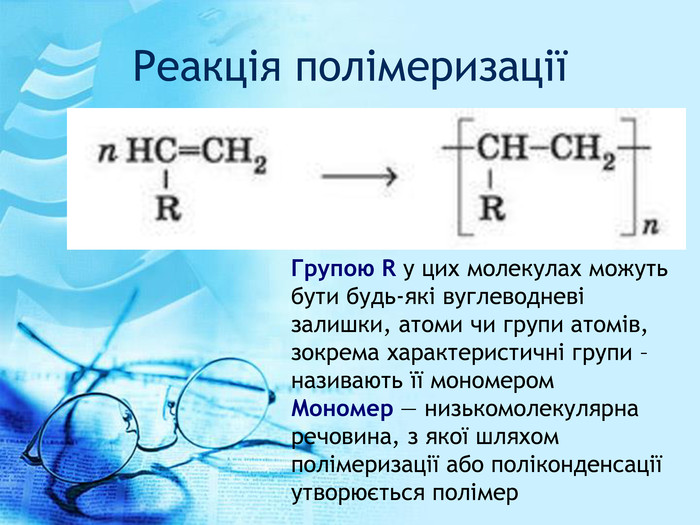


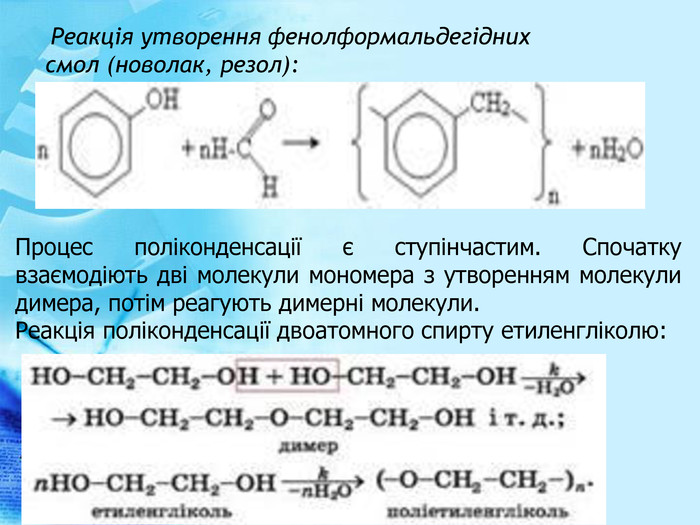

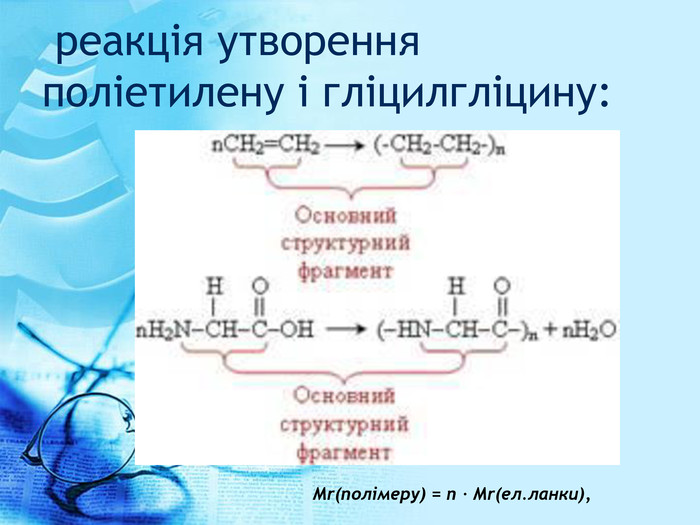



![Завдання1. Формулу поліпропілену можна записати так: H-[CH2-CH(CH3)]n-H. Визначте молярну масу поліпропілену, якщо кожна молекула містить по 150 структурних ланок.2. Формулу полістиролу можна записати так: H-[CH2-CH(C6 H5)]n-H. Визначте число структурних ланок у його молекулах п, якщо його молярна маса дорівнює 12 482 г/моль. Завдання1. Формулу поліпропілену можна записати так: H-[CH2-CH(CH3)]n-H. Визначте молярну масу поліпропілену, якщо кожна молекула містить по 150 структурних ланок.2. Формулу полістиролу можна записати так: H-[CH2-CH(C6 H5)]n-H. Визначте число структурних ланок у його молекулах п, якщо його молярна маса дорівнює 12 482 г/моль.](/uploads/files/197377/238059/257509_images/33.jpg)
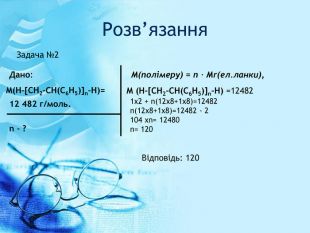
![Розв’язання. Дано: H-[CH2-CH(CH3)]n-Hn=150 M(H-[CH2-CH(CH3)]n-H) - ?M(полімеру) = n ∙ Mr(ел.ланки),М(H-[CH2-CH(CH3)]n-H) = 150х (12х3 + 1х6) + 1х2= 6302 г/моль. Відповідь: 6302 г/моль. Задача №1 Розв’язання. Дано: H-[CH2-CH(CH3)]n-Hn=150 M(H-[CH2-CH(CH3)]n-H) - ?M(полімеру) = n ∙ Mr(ел.ланки),М(H-[CH2-CH(CH3)]n-H) = 150х (12х3 + 1х6) + 1х2= 6302 г/моль. Відповідь: 6302 г/моль. Задача №1](/uploads/files/197377/238059/257509_images/34.jpg)
![Розв’язання. Дано: M(H-[CH2-CH(C6 H5)]n-H)=12 482 г/моль.n - ?M(полімеру) = n ∙ Mr(ел.ланки),Відповідь: 120 М (H-[CH2-CH(C6 H5)]n-H) =124821х2 + n(12х8+1х8)=12482n(12х8+1х8)=12482 - 2104 хn= 12480n= 120 Задача №2 Розв’язання. Дано: M(H-[CH2-CH(C6 H5)]n-H)=12 482 г/моль.n - ?M(полімеру) = n ∙ Mr(ел.ланки),Відповідь: 120 М (H-[CH2-CH(C6 H5)]n-H) =124821х2 + n(12х8+1х8)=12482n(12х8+1х8)=12482 - 2104 хn= 12480n= 120 Задача №2](/uploads/files/197377/238059/257509_images/35.jpg)
![ДОМАШНЄ ЗАВДАННЯ: Опрацювати параграф 32 Виконати впр.510 ст. 199 Формулу капрону, що є продуктом поліконденсації певної амінокислоти, можна записати так: H-[NH-(CH2)x-CO]n-OH. Визначте число атомів Карбону в одній молекулі цієї амінокислоти, якщо молярна маса капрону дорівнює 6368 г/моль, а кожна його молекула містить по 50 структурних ланок. ДОМАШНЄ ЗАВДАННЯ: Опрацювати параграф 32 Виконати впр.510 ст. 199 Формулу капрону, що є продуктом поліконденсації певної амінокислоти, можна записати так: H-[NH-(CH2)x-CO]n-OH. Визначте число атомів Карбону в одній молекулі цієї амінокислоти, якщо молярна маса капрону дорівнює 6368 г/моль, а кожна його молекула містить по 50 структурних ланок.](/uploads/files/197377/238059/257509_images/36.jpg)