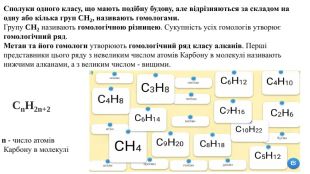
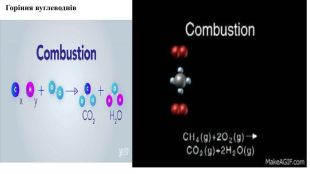
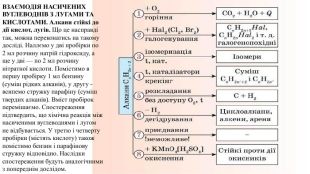
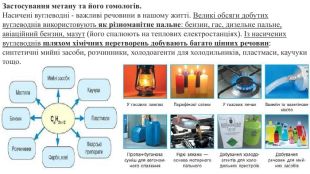
Презентація. Властивості метану та його гомологів.
Про матеріал
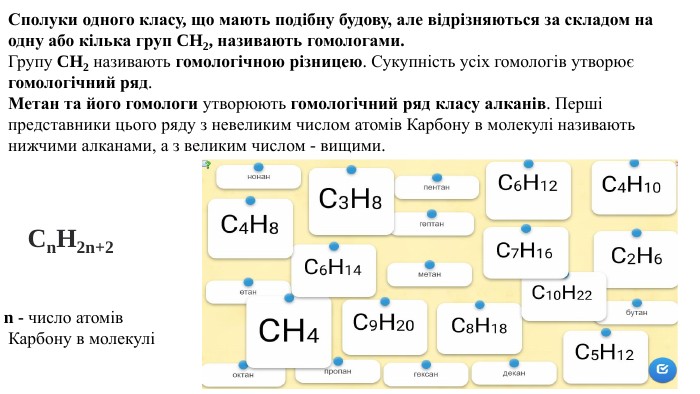
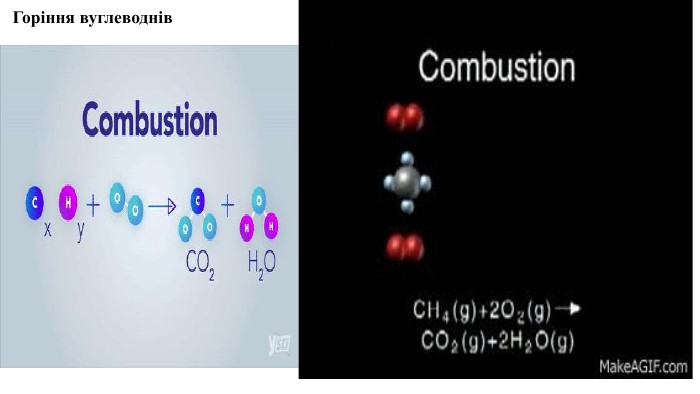
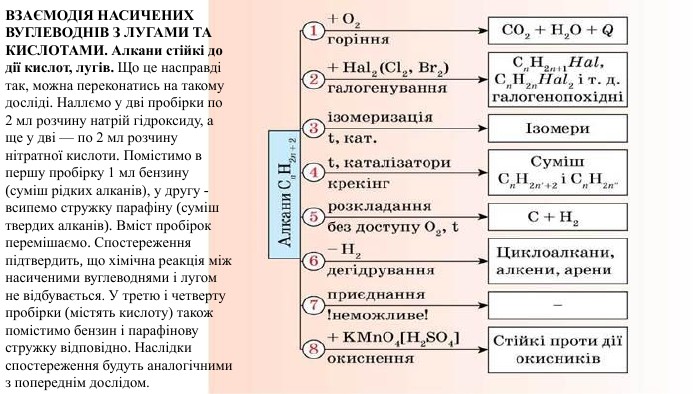
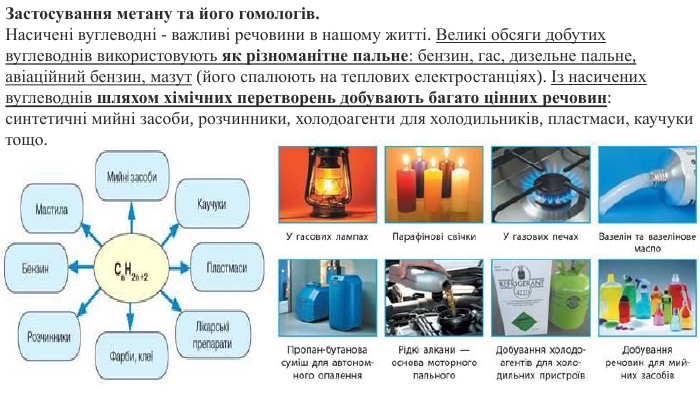
Пропоную до уваги добірку навчального матеріала у вигляді презентації. Презентація за темою "Властивості метану та його гомологів" може бути корисною та використана під час підготовки до уроку або під час уроку онлайн або офлайн заняття.
Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку