Презентація " Властивості середніх солей"
Про матеріал
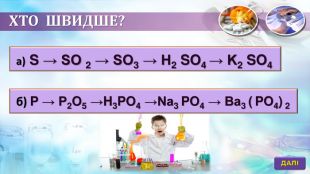
Презентація" Властивості середніх солей"'.
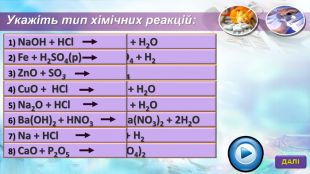
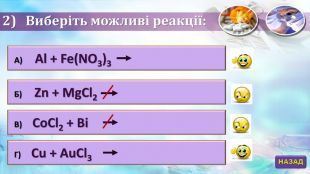
Дана розробка дасть можливість практично знайомити учнів з основними представниками неорганічних сполук-солями; провести реакції нейтралізації, заміщення,розкладу. Перегляд файлу
Зміст слайдів
pptx
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку