Презентація «Вступ до органічної хімії 9 клас
| Презентація допоможе провести урок на тему «Особливості органічних сполук (порівняно з неорганічними).Елементи-органогени». |



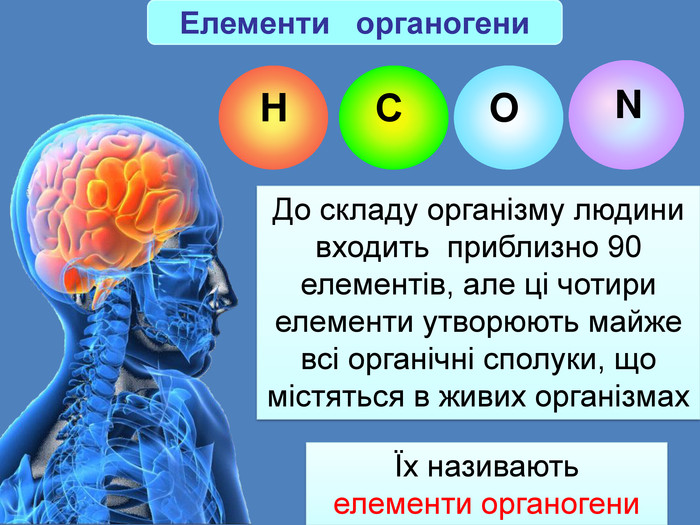









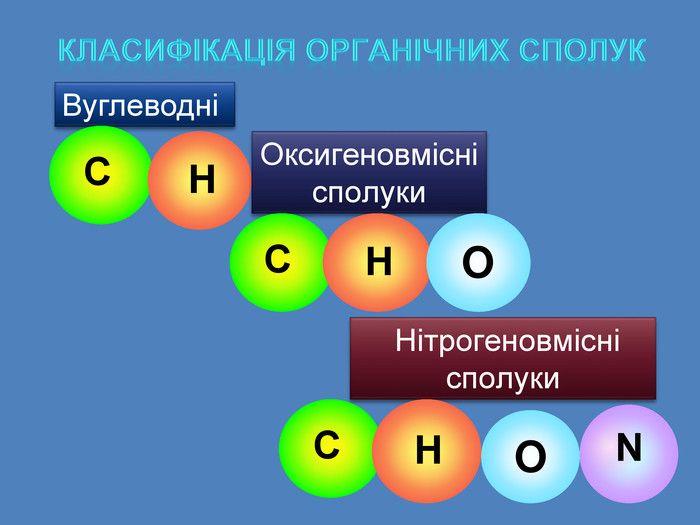


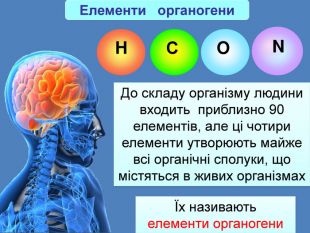
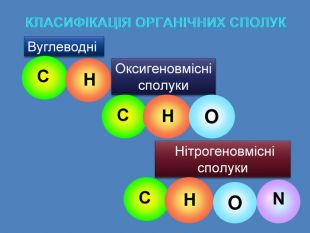
Сполуки в яких атом Карбону перебуває у зв'язку з металевими елементами, або з неметалічними, називаються елементорганічними сполуками Органічні сполуки складаються з невеликої кількості елементів До їх складу, крім Карбону, майже завжди входить Гідроген, часто Оксиген і Нітроген, іноді Сульфур і Фосфор H O С N Na Cl Аl S К P As Si
Тривалий час вчені вважали, що речовини живих організмів утворюються завдяки таємничої життєвої сили “vis vitalis" Засновником теорії “віталізму” й органічної хімії як науки вважають шведського вченого. Й. Я. Берцеліуса Теорія “віталізму” особливо наголошувала на істотних відмінностях між органічними й неорганічними речовинами і неможливості їх створення штучним шляхом
Теорія хімічної будови органічних сполук О. М. Бутлерова. Олександр Михайлович Бутлеров (1828 – 1886)Головною метою вчених був пошук шляхів синтезу нових речовин. Для цього була необхідна теорія, що дозволяла б пояснити відомі факти і нові відкриття. Такою теорією в органічній хімії є теорія хімічної будови основні положення якої О. М. Бутлеров доповів 19 вересня 1861 року на зїзді німецьких натуралістів і лікарів
Теорія хімічної будови органічних сполук О. М. Бутлерова1. Атоми елементів у складі молекули з’єднуються між собою у певній послідовності відповідно до їхньої валентності. При цьому всі валентності мають бути задіяні в утворенні зв’язків з іншими атомами. 2. Властивості органічних речовин залежать не тільки від якісного і кількісного складу, а й від послідовності та характеру сполучення між атомами у молекулі, тобто від будови молекули речовини. 3. Атоми, що утворили молекули, взаємовпливають один на одного, визначаючи хімічні властивості речовини
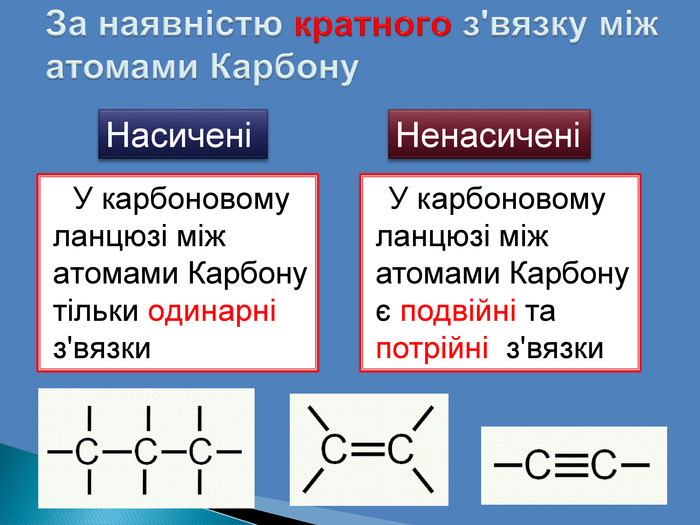
Теорія хімічної будови органічних сполук О. М. Бутлерова. Теорія хімічної будови враховує особливості елемента Карбону. Атом Карбону можуть утворювати між собою міцні ковалентні звязкиі сполучатися в довгі карбонові ланцюги: нерозгалужені,розгалужені та циклічніАтом Карбону можуть утворювати між собою та атомами інших елементів міцні хімічні з'вязки різної кратності
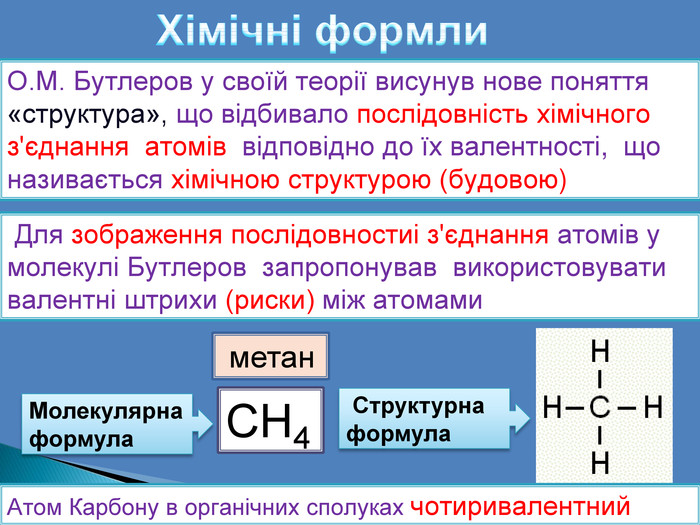
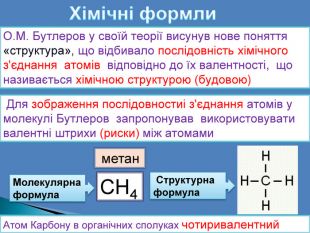
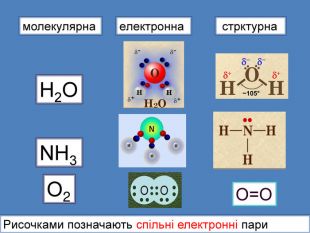
Хімічні формли. О. М. Бутлеров у своїй теорії висунув нове поняття «структура», що відбивало послідовність хімічного з'єднання атомів відповідно до їх валентності, що називається хімічною структурою (будовою) Для зображення послідовностиі з'єднання атомів у молекулі Бутлеров запропонував використовувати валентні штрихи (риски) між атомами. СН4 метан. Молекулярнаформула Структурнаформула. Атом Карбону в органічних сполуках чотиривалентний
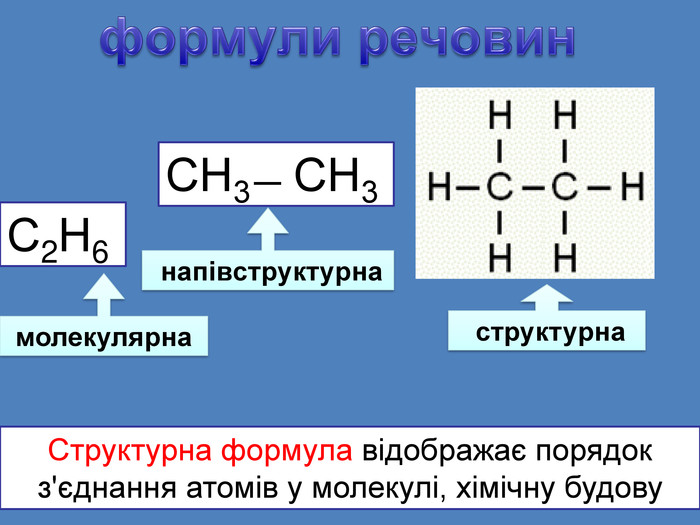
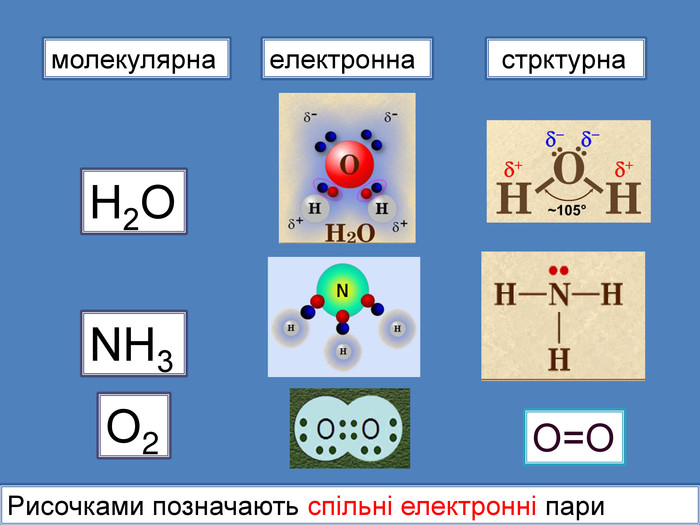
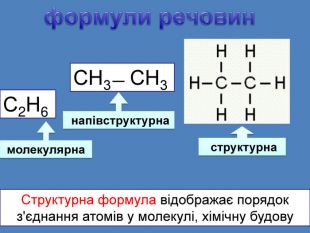
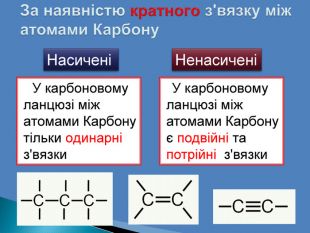
Хімічні формули. С2 Н4 молекулярна формула. В молекулярній формулі записують якісний і кількісний склад молекул без зазначення хімічних зв'язків у ній. Структурна (графічна) формула. В структурних формулах прийнято позначати одинарні, подвійні і потрійні хімічні зв'язки між атомами відповідною кількістю рисок
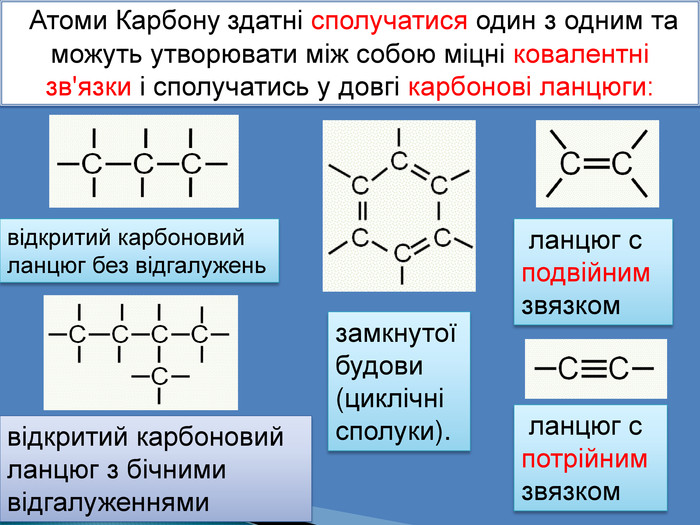
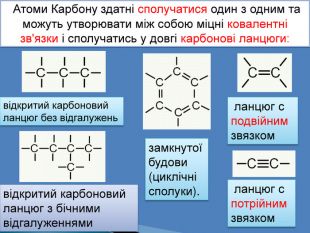
Атоми Карбону здатні сполучатися один з одним та можуть утворювати між собою міцні ковалентні зв'язки і сполучатись у довгі карбонові ланцюги:відкритий карбоновий ланцюг без відгалуженьвідкритий карбоновий ланцюг з бічними відгалуженнями ланцюг с подвійним звязком ланцюг с потрійнимзвязкомзамкнутої будови (циклічні сполуки).
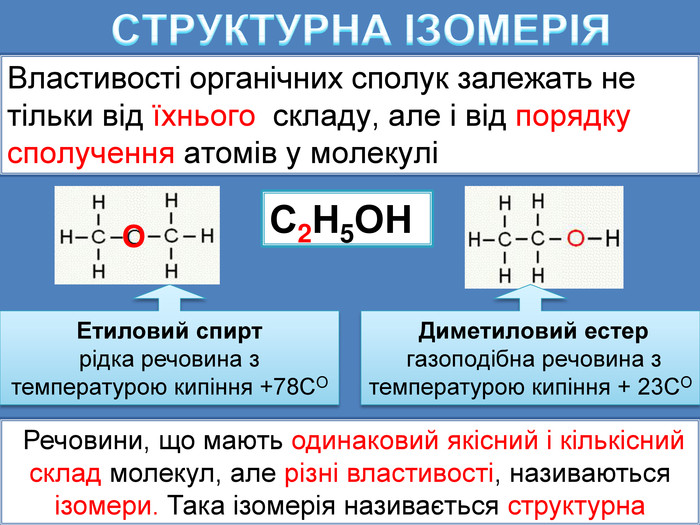
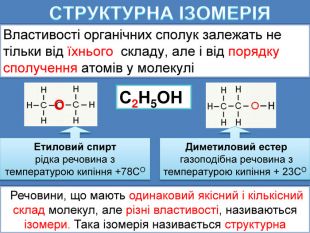
СТРУКТУРНА ІЗОМЕРІЯВластивості органічних сполук залежать не тільки від їхнього складу, але і від порядку сполучення атомів у молекуліС2 Н5 ОНЕтиловий спиртрідка речовина з температурою кипіння +78 СO Диметиловий естер газоподібна речовина з температурою кипіння + 23 СO Речовини, що мають одинаковий якісний і кількісний склад молекул, але різні властивості, називаються ізомери. Така ізомерія називається структурна. О
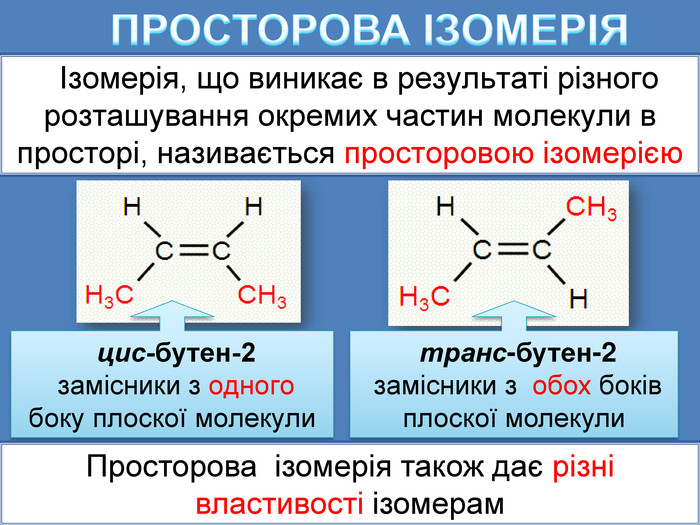
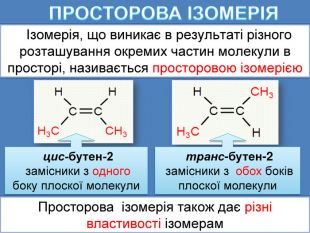
ПРОСТОРОВА ІЗОМЕРІЯ Ізомерія, що виникає в результаті різного розташування окремих частин молекули в просторі, називається просторовою ізомерією цис-бутен-2 замісники з одного боку плоскої молекули транс-бутен-2 замісники з обох боків плоскої молекули. Просторова ізомерія також дає різні властивості ізомерам
Григорович О. В. Хімія: підруч. для 9 класу загальноосвіт. навч.закл./ О. В. Григорович .̶ Харків: Вид-во «Ранок», 2017 Шаповалов С. А. Хімія. Довідник старшокласника та абітурієнта. Харків. Торсінг, 2005. Строойтова І. Ю. Усі уроки імії. 9 клас ̶ Х.: вид. група «Основа», 2009 Абрамович С.І. Левитська О. В. Хімія. Розвязування задач, відповіді на питання, підказки до практичних робіт до підручника Н. М. Буринської Харків: Веста 2002 Джерела


про публікацію авторської розробки
Додати розробку















-

Переверзева Інна Євгенівна
08.01.2024 в 17:59
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Дзевенко Марія Віталіївна
11.02.2023 в 16:34
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Теребіленко Людмила Володимирівна
26.01.2023 в 21:33
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Бондаренко Наталія Богданівна
22.01.2023 в 17:24
Загальна:
4.7
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
4.0
-

Світлична Алла Вікторівна
15.01.2023 в 19:01
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Сергєєнкова ірина Станіславівна
16.12.2021 в 06:25
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

фертак наталя
18.01.2021 в 19:46
Дякую за цікаву презентацію
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Загурська Надія
09.01.2020 в 12:17
Загальна:
4.3
Структурованість
4.0
Оригінальність викладу
4.0
Відповідність темі
5.0
-

Кудлай Наталія Олександрівна
17.09.2019 в 17:14
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Паращак Наталія Миколаївна
04.04.2018 в 14:49
Дякую за корисний матеріал!!!
Загальна:
4.3
Структурованість
4.0
Оригінальність викладу
4.0
Відповідність темі
5.0
Показати ще 7 відгуків