Презентація "«Взаємодія води з оксидами. Поняття про кислоти й основи. Поняття про індикатори»."
Про матеріал
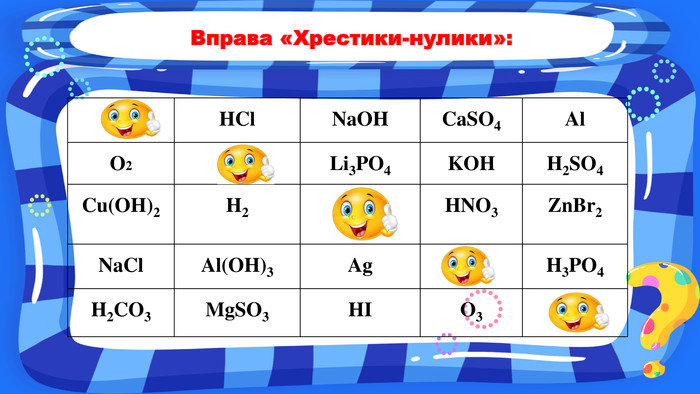
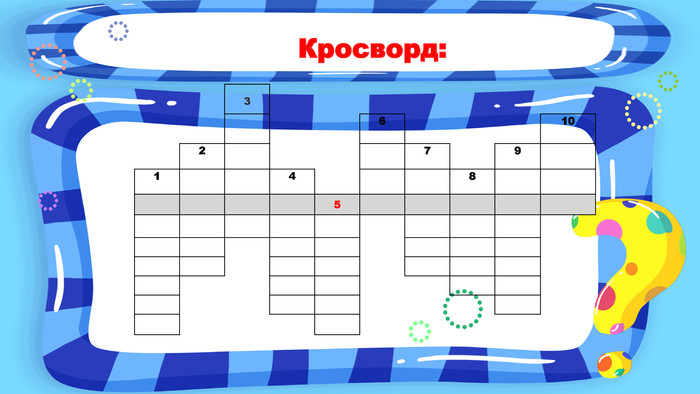
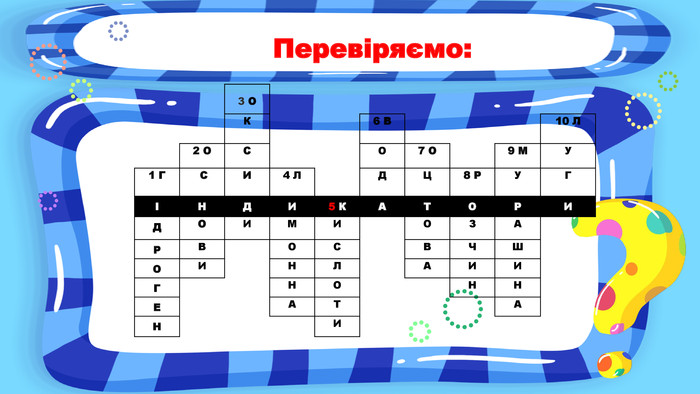
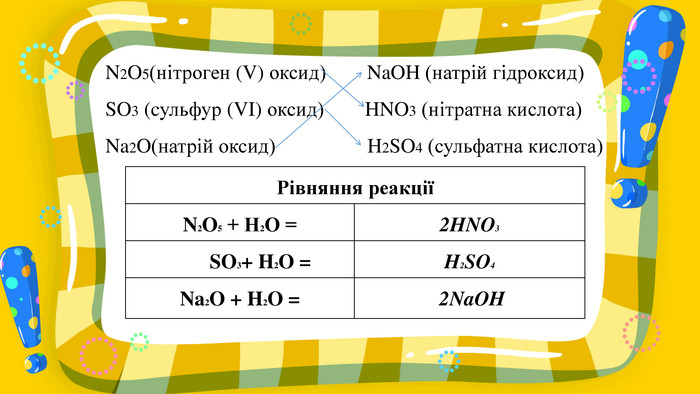
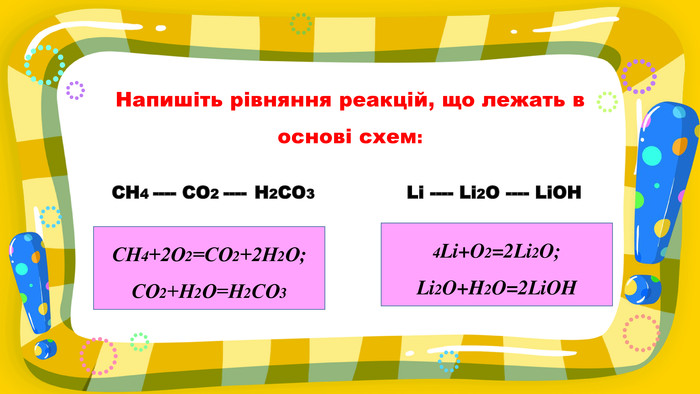
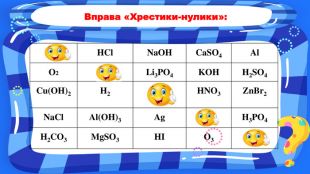
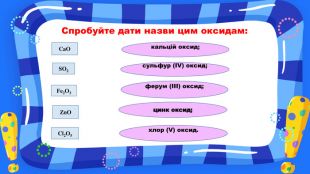
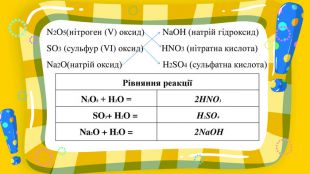
Презентація до уроку для 7 класу з теми «Взаємодія води з оксидами. Поняття про кислоти й основи. Поняття про індикатори». У презентаціх представлені вправи на повторення раніше засвоєного матеріалу та вивчення нового. Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку