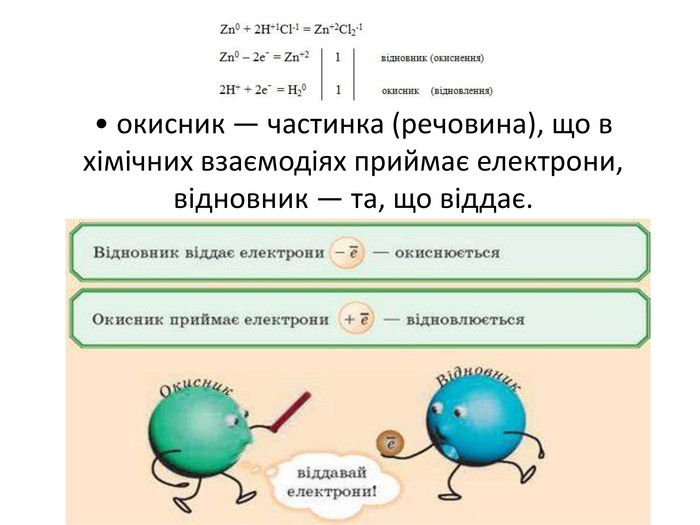
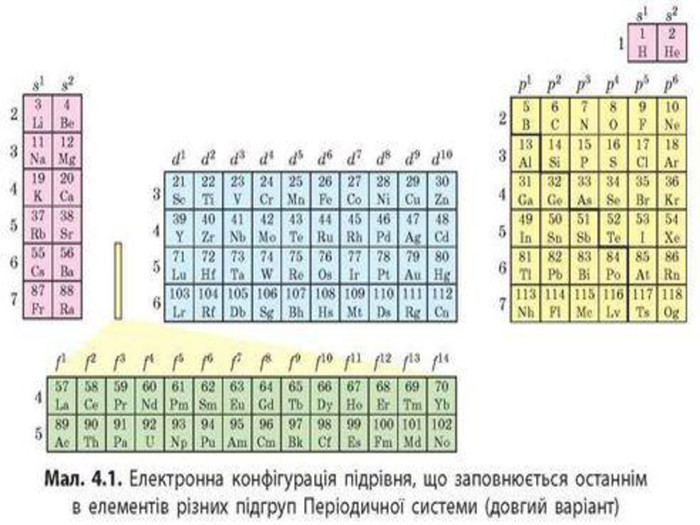
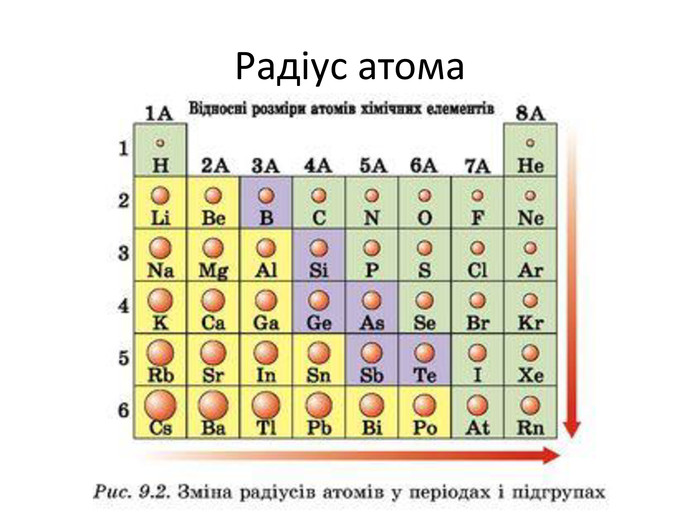
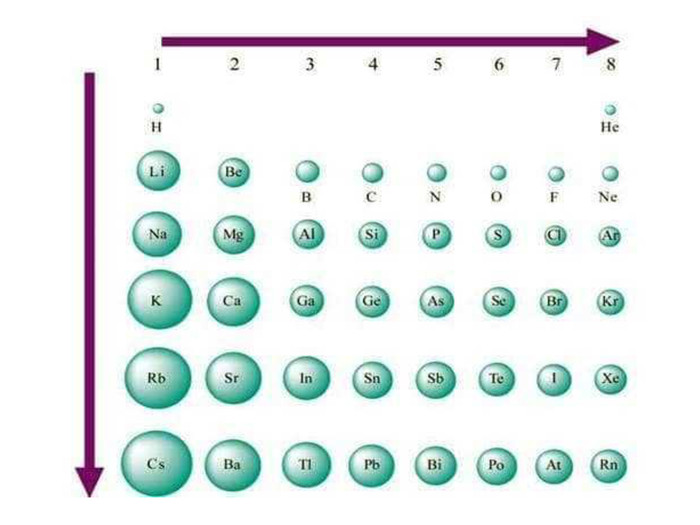
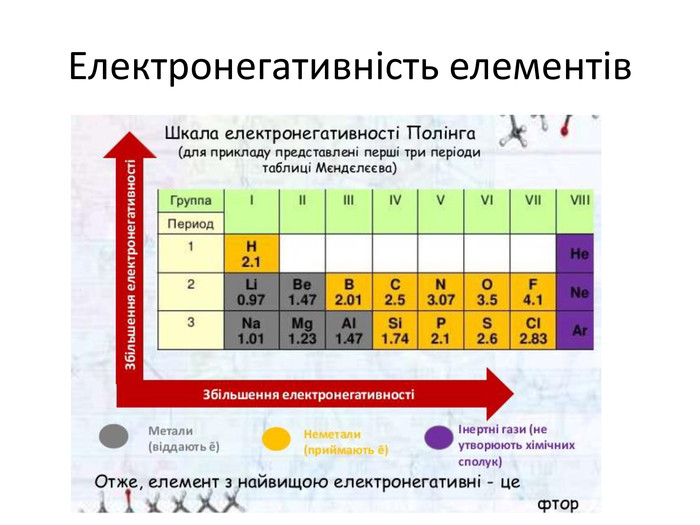
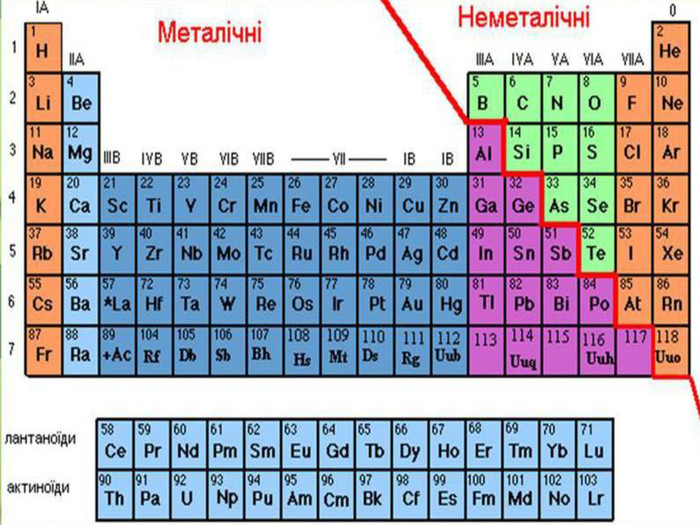
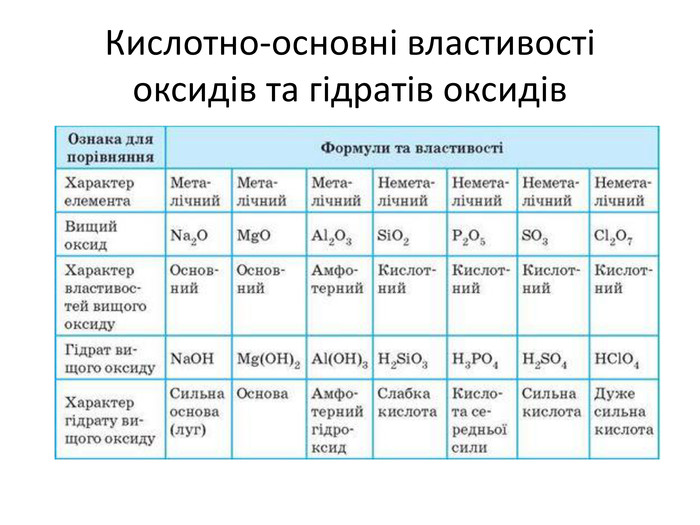
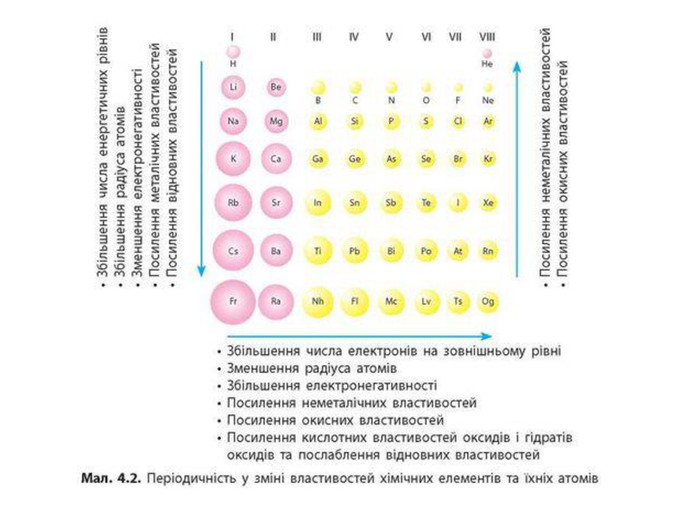
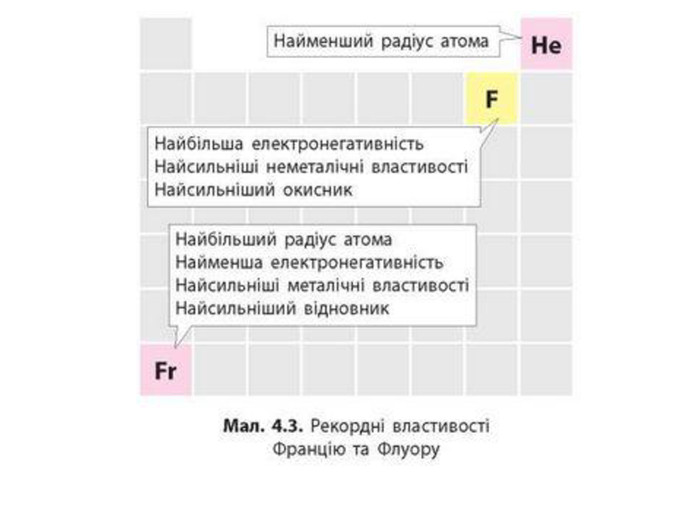
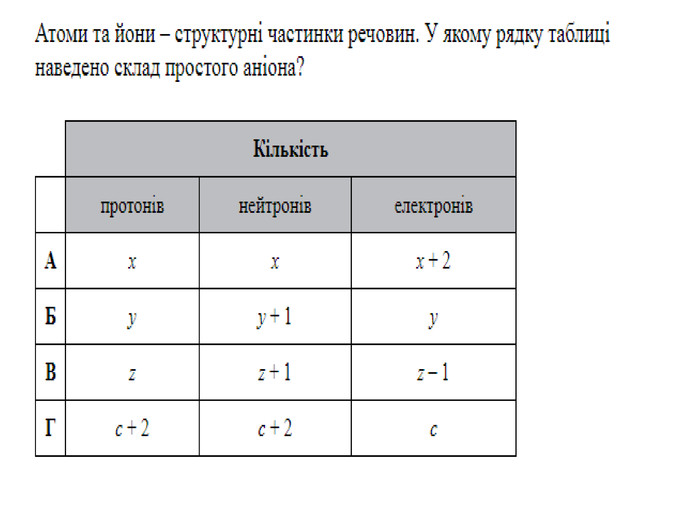
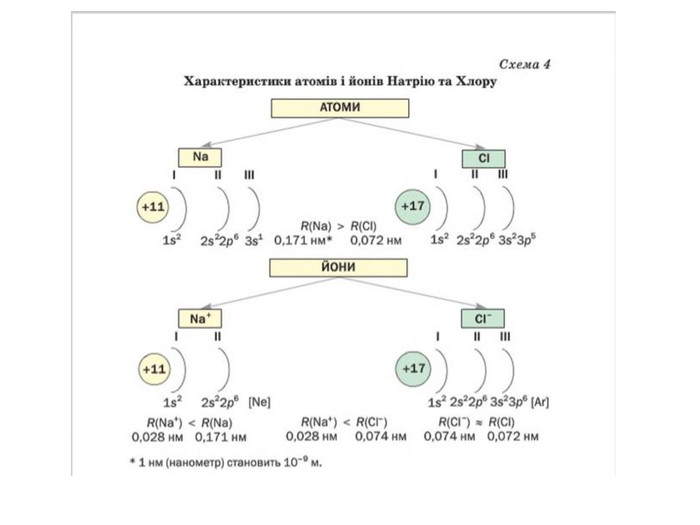
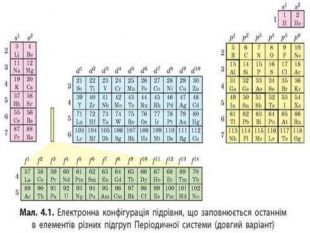
Презентація "Явище періодичної зміни властивостей елементів та їхніх сполук на основі уявлень про електронну будова атомів"
Про матеріал
Презентація до уроку "Явище періодичної зміни властивостей елементів та їхніх сполук на основі уявлень про електронну будова атомів". Містить підбірку тестів ЗНО з даної теми. Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки
ppt
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку