Презентація з біології та екології для учнів 10 класу (рівень стандарту) "Медична генетика"
Про матеріал
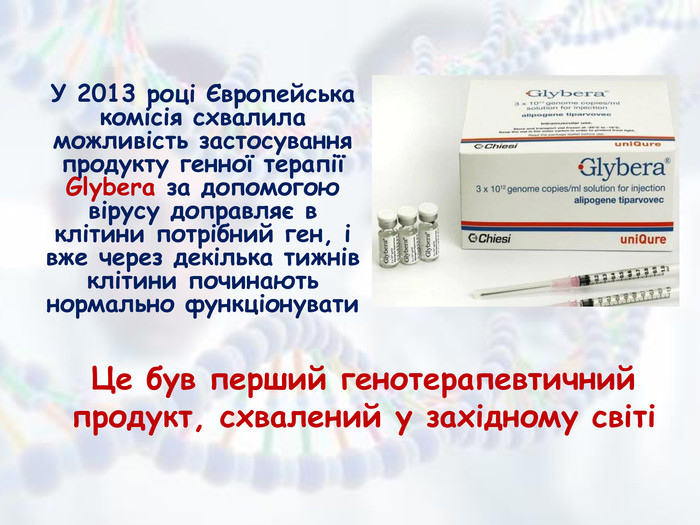
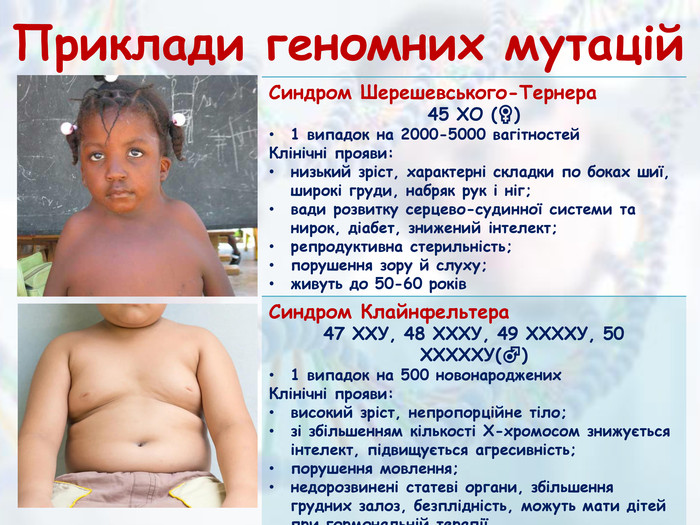
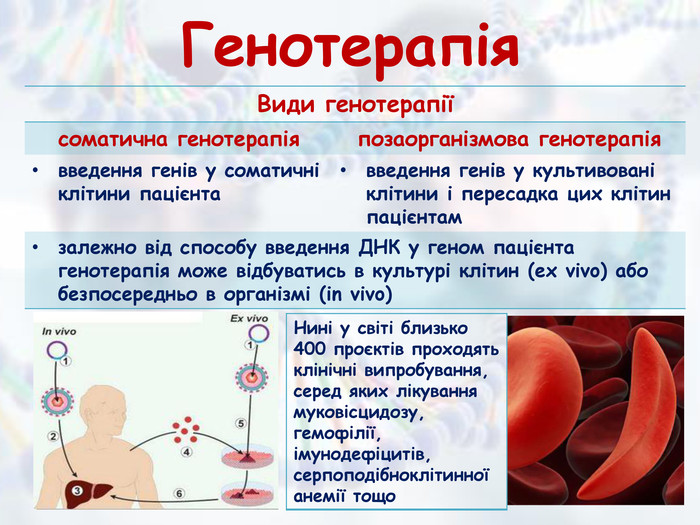
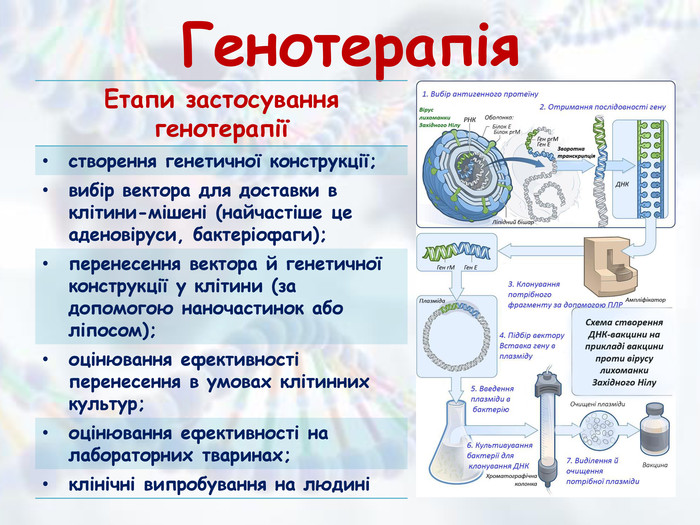
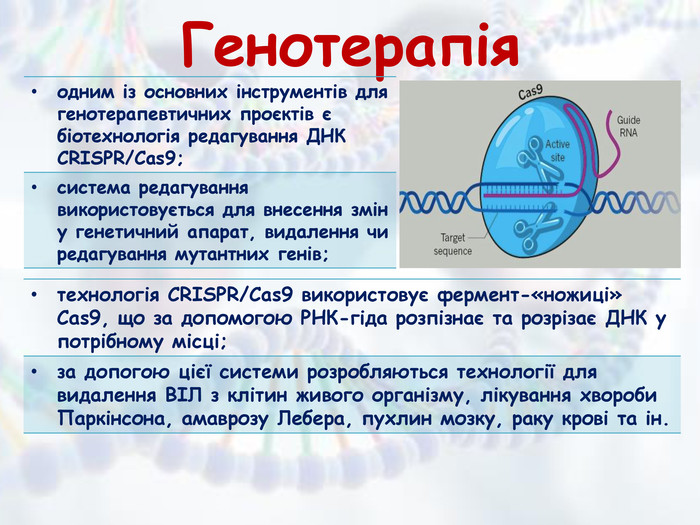
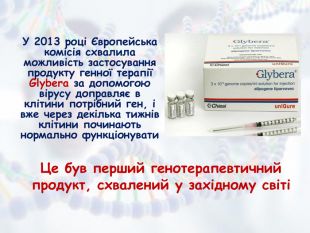
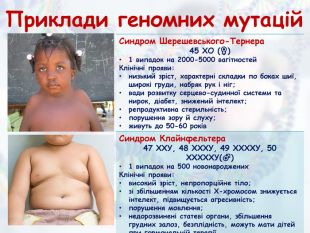
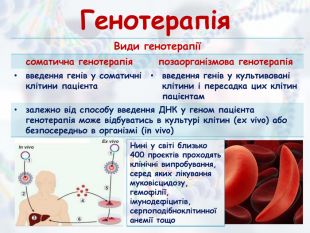
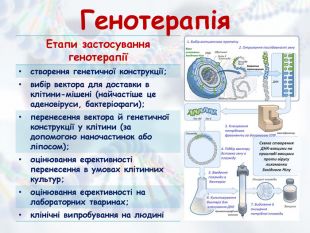
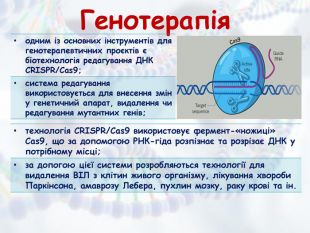
Презентація з біології та екології для учнів 10 класу (рівень стандарту) "Медична генетика" допоможе роз'яснити наступні питання: медична генетика, основні завдання медичної генетики, спадкові захворювання та хвороби зі спадковою схильністю, медико-генетичне консультування, генотерапія
Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки
-
Дякую за чудову презентацію!!!!
-
Дякую!
-


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку