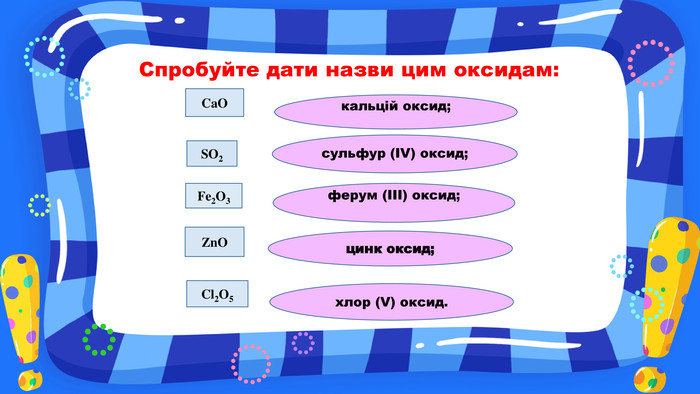
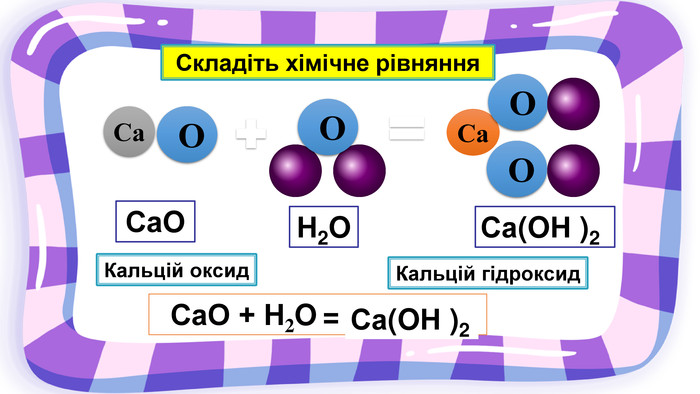
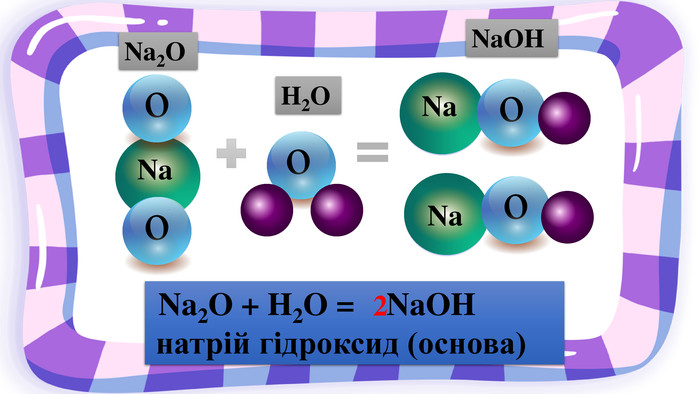
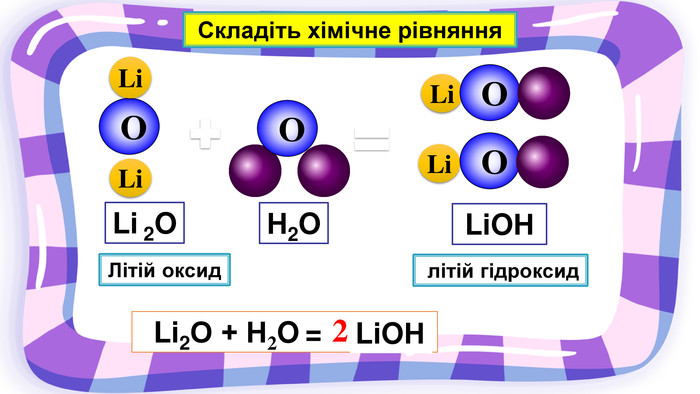
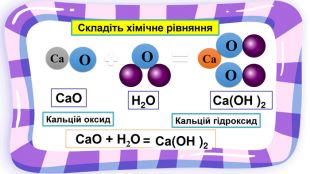
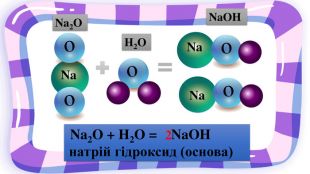
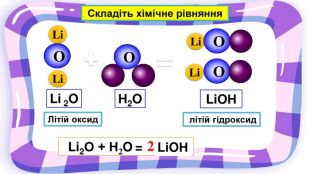
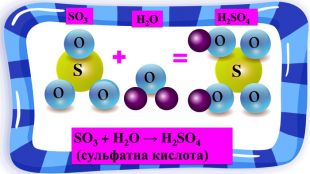
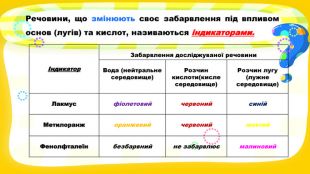
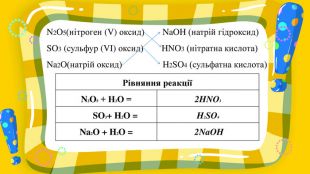
Презентація з хімії на тему "Взаємодія води з оксидами" для учнів 7 класу
Про матеріал
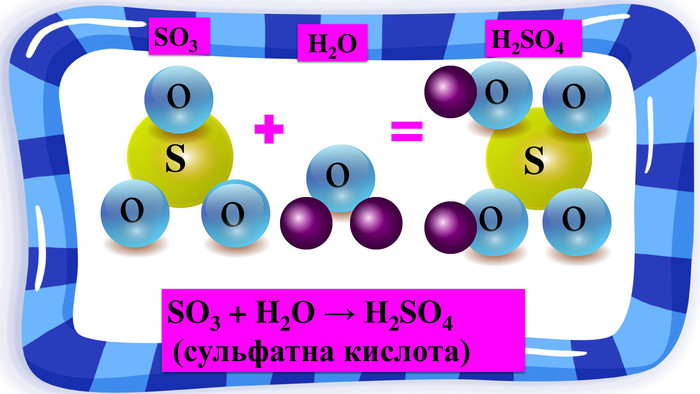
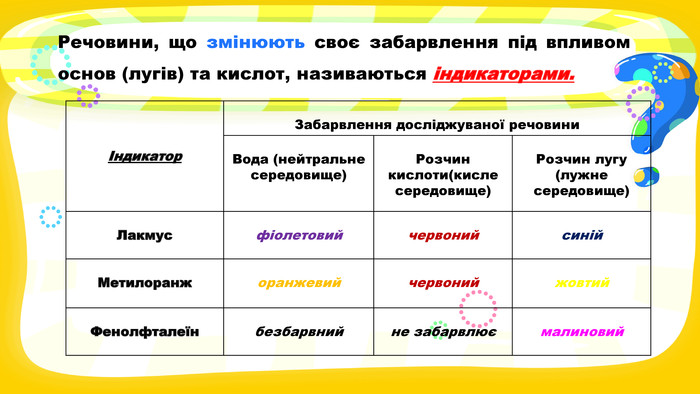
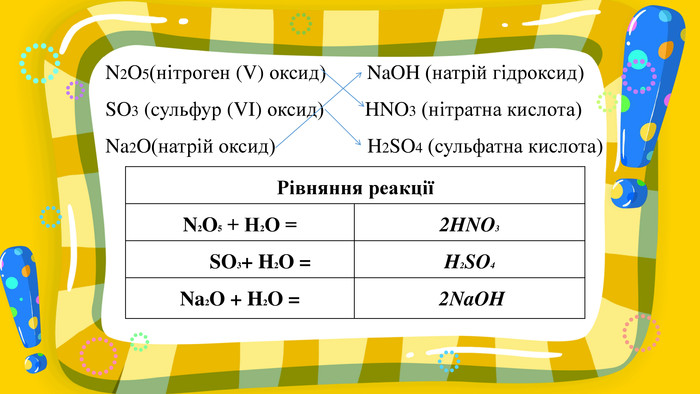
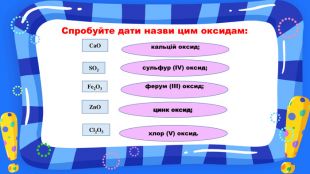
Презентація з хімії на тему "Взаємодія води з оксидами" для учнів 7 класу
Вчитель хімії та інформатики Шпилівської філії Опорного закладу Садівська загальноосвітня школа І-ІІІ ст. Мірошниченко Наталія Олександрівна Перегляд файлу
Зміст слайдів
pptx
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку