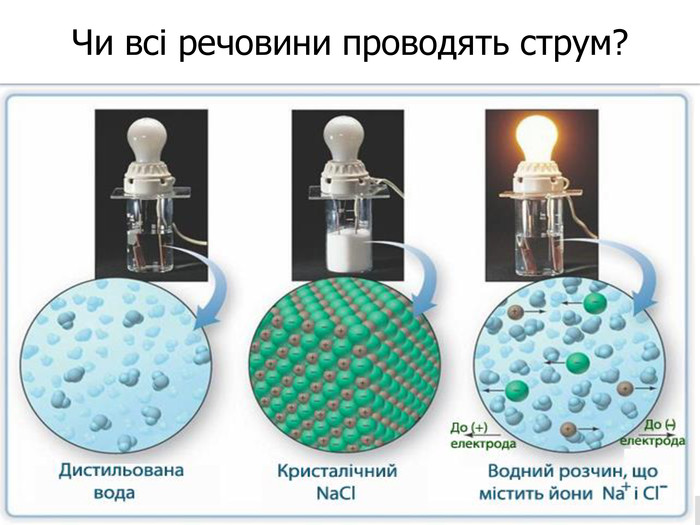
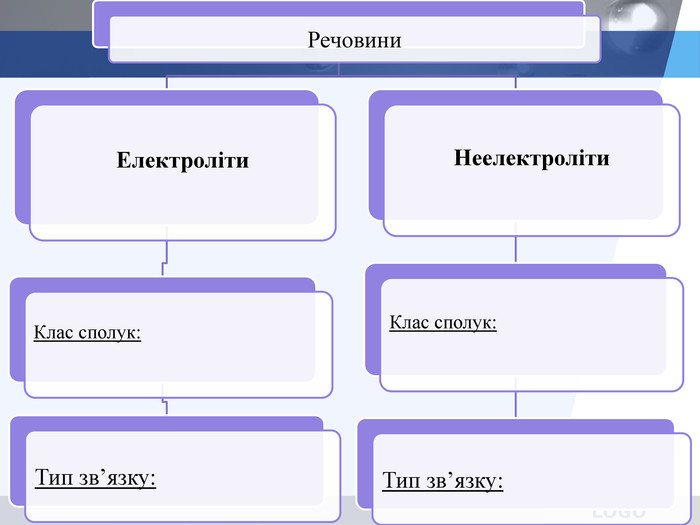
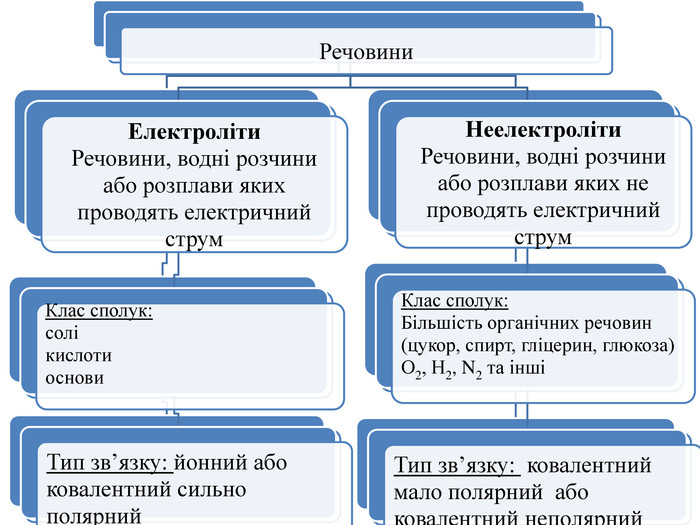
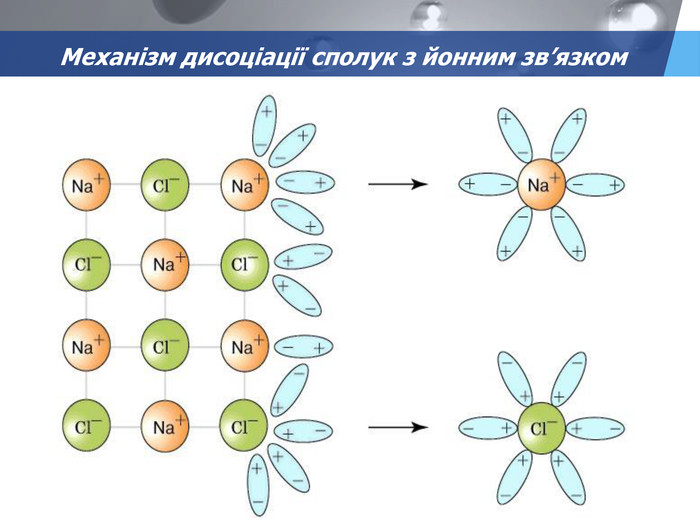
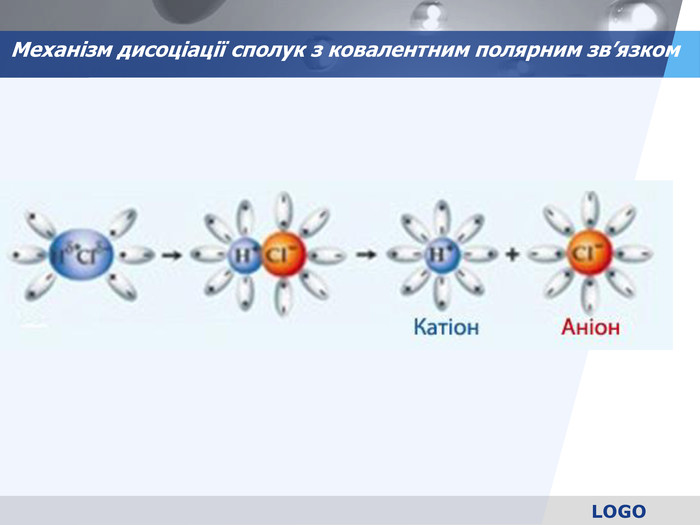
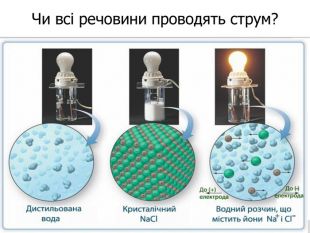
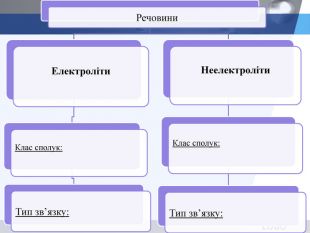
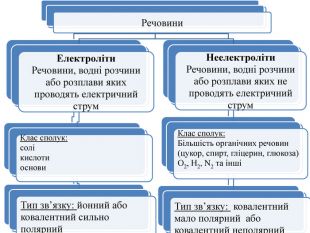
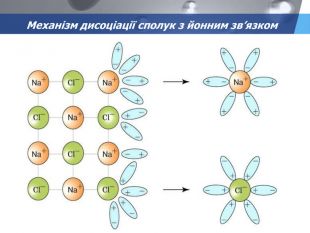
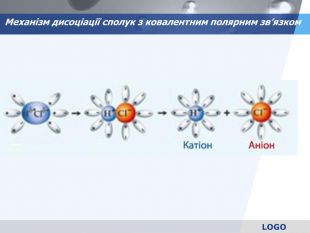
презентація з теми: Електролітична дисоціація. Електроліти і неелектроліти.
Про матеріал
презентація до уроку в 9 класі з теми: Електролітична дисоціація. Електроліти і неелектроліти. Перегляд файлу
Зміст слайдів


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку