Презентація з теми: "Карбонові кислоти"






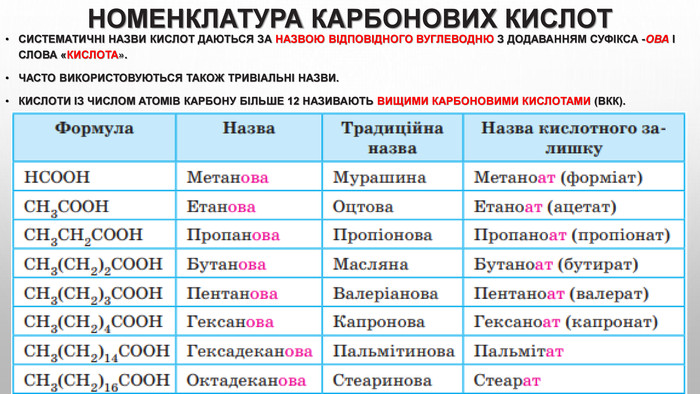


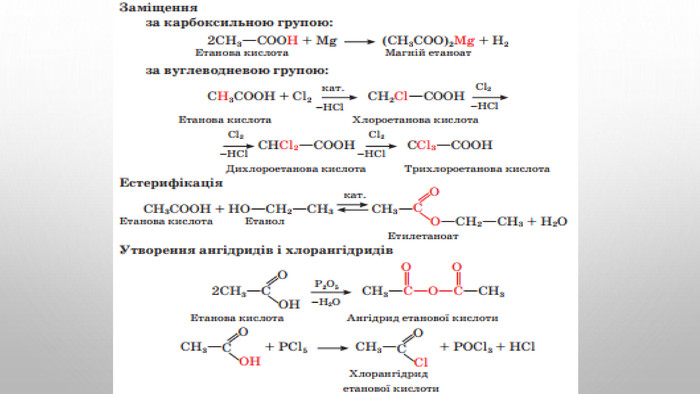
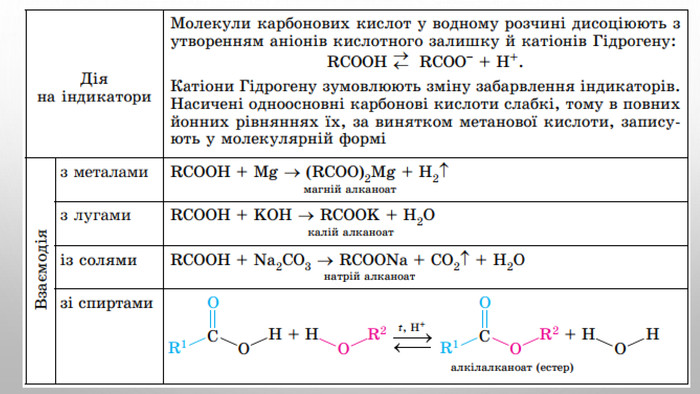

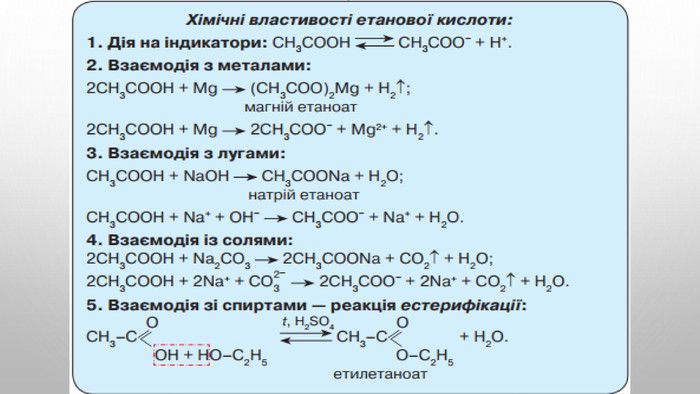

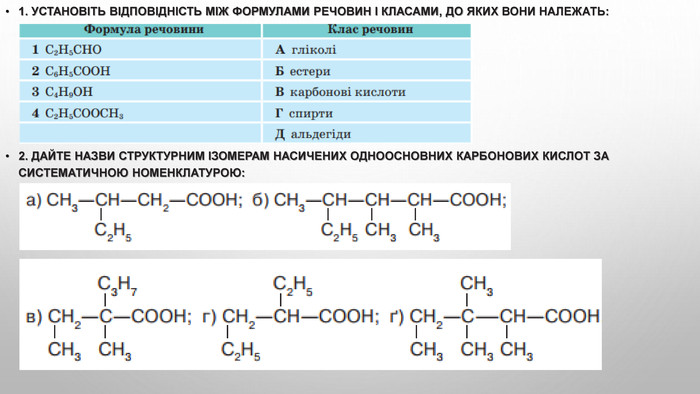



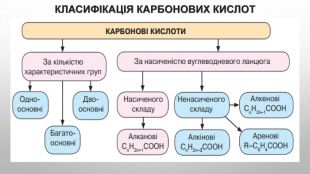
Карбонові кислоти, їхній склад, поширення в природі та класифікація. Карбоксильна характеристична (функціональна) група. Фізичні властивості. Будова молекул насичених одноатомних карбонових кислот, їхня загальна та структурні формули, ізомерія, систематична номенклатура. Хімічні властивості насичених одноосновних карбонових кислот. Реакція етерифікації. Одержання етанової кислоти. Лабораторний дослід:1. Виявлення органічних кислот у харчових продуктах. R-cooh
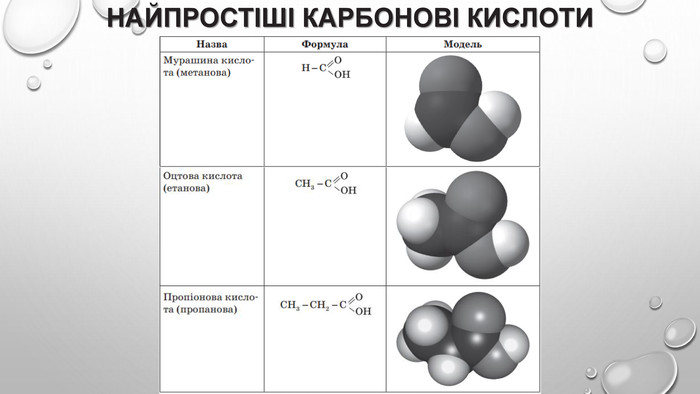
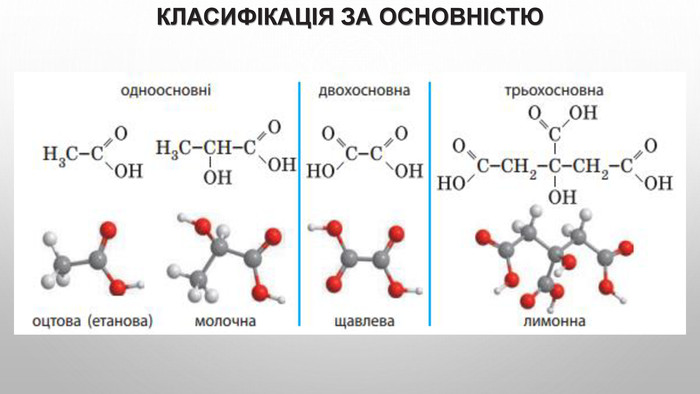
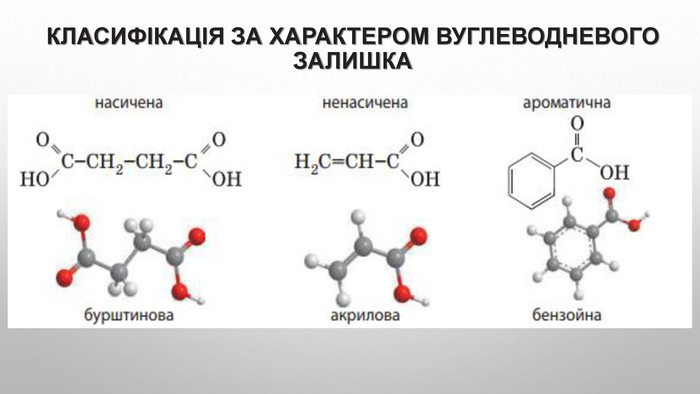
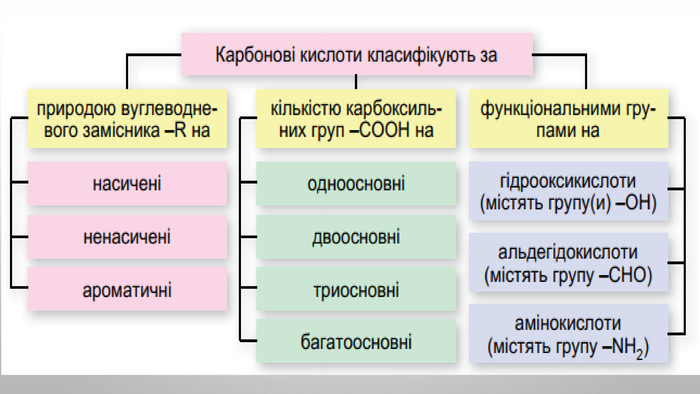
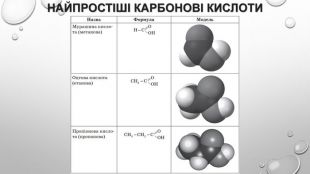
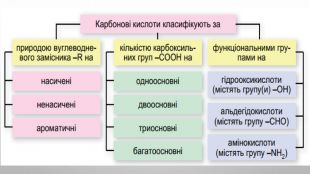
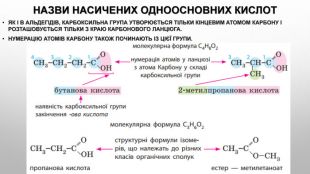
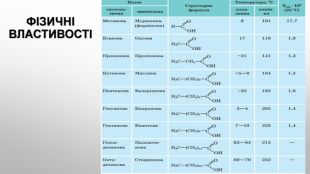
Поняття про карбонові кислоти. Карбонові кислоти — похідні вуглеводнів, молекули яких містять одну або кілька карбоксильних груп. карбоксильна група: , або – соон. Слово «карбоксильна» складається із частин назв груп атомів С=О і О–Н: «карбонільна», «гідроксильна». Загальна формула карбонових кислот з однією карбоксильною групою в молекулі: , або r – cooh.
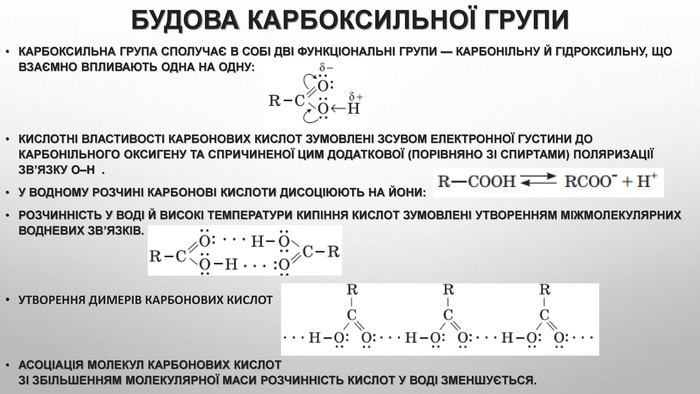
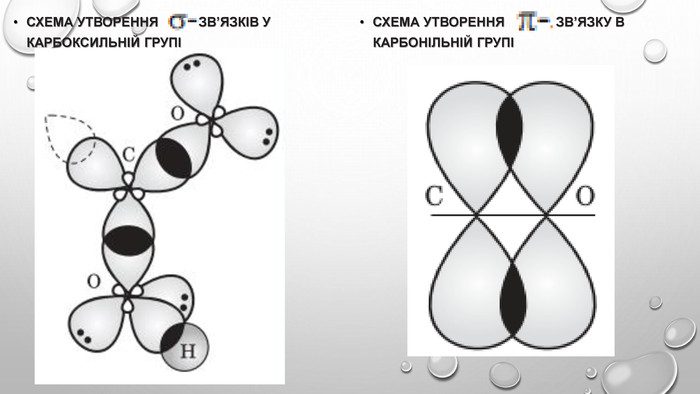
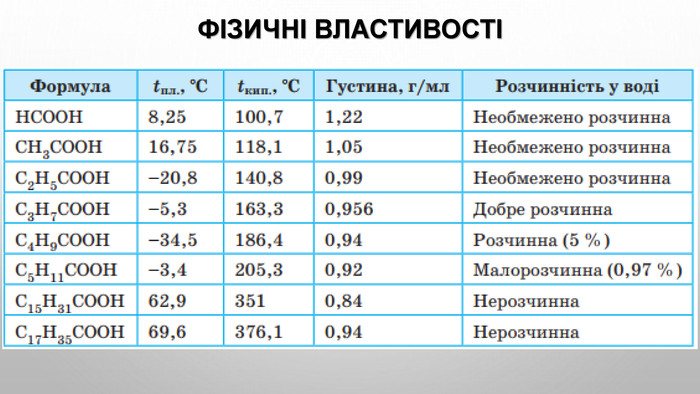
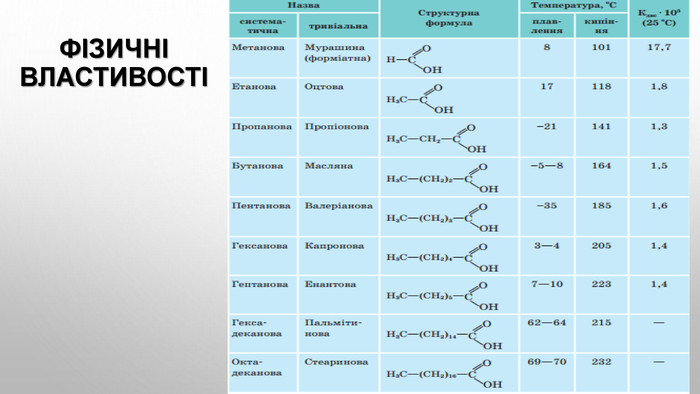
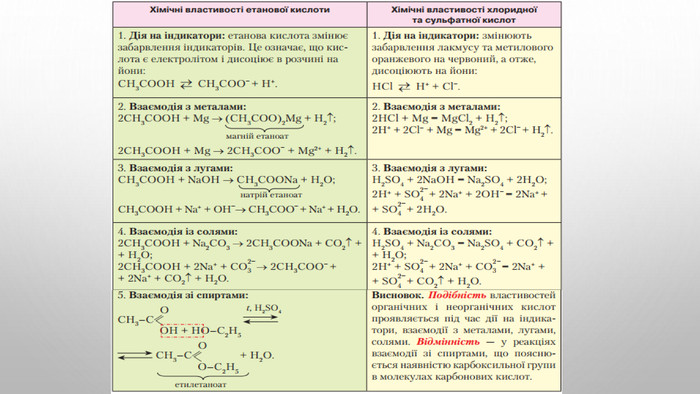
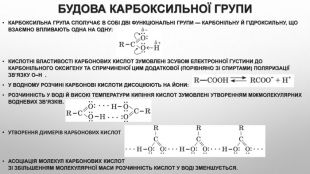
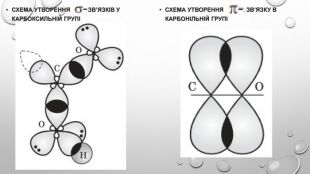
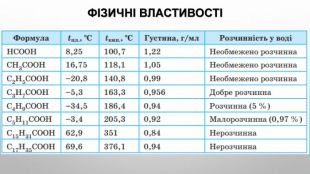
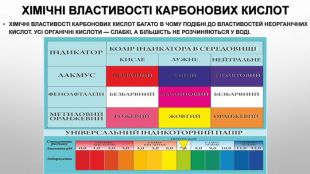
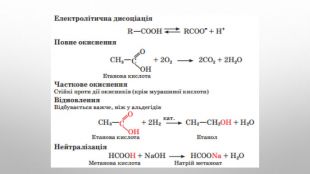
Будова карбоксильної групи Карбоксильна група сполучає в собі дві функціональні групи — карбонільну й гідроксильну, що взаємно впливають одна на одну: Кислотні властивості карбонових кислот зумовлені зсувом електронної густини до карбонільного Оксигену та спричиненої цим додаткової (порівняно зі спиртами) поляризації зв’язку O–H . У водному розчині карбонові кислоти дисоціюють на йони:розчинність у воді й високі температури кипіння кислот зумовлені утворенням міжмолекулярних водневих зв’язків. Утворення димерів карбонових кислот асоціація молекул карбонових кислот. Зі збільшенням молекулярної маси розчинність кислот у воді зменшується.
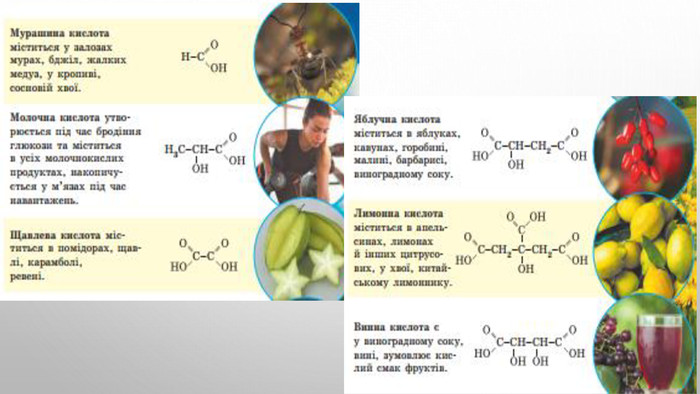
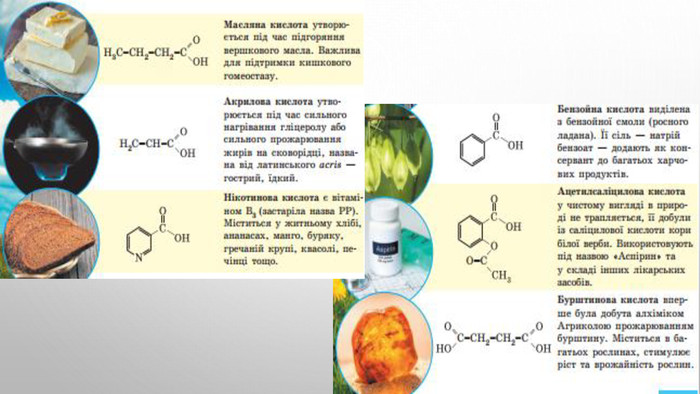
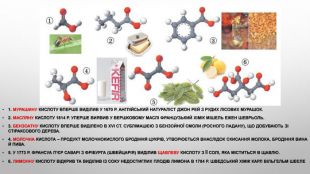
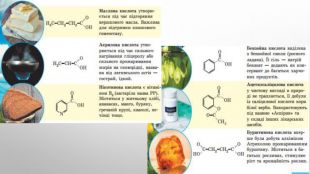
1. Мурашину кислоту вперше виділив у 1670 р. англійський натураліст Джон Рей з рудих лісових мурашок. 2. Масляну кислоту 1814 р. уперше виявив у вершковому маслі французький хімік Мішель Ежен Шеврьоль. 3. Бензоатну кислоту вперше виділено в XVI ст. сублімацією з бензойної смоли (росного ладану), що добувають зі стіраксового дерева. 4. Молочна кислота – продукт молочнокислого бродіння цукрів, утворюється внаслідок скисання молока, бродіння вина й пива. 5. У 1773 р. Франсуа П’єр Саварі з Фрібурга (Швейцарія) виділив щавлеву кислоту з її солі, яка міститься в щавлю. 6. Лимонну кислоту відкрив та виділив із соку недостиглих плодів лимона в 1784 р. шведський хімік Карл Вільгельм Шеєле
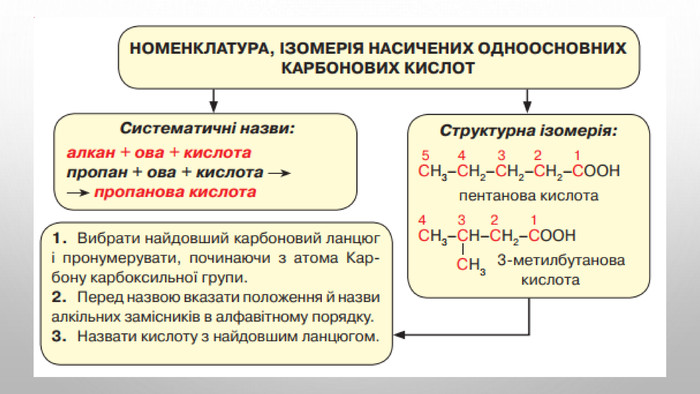
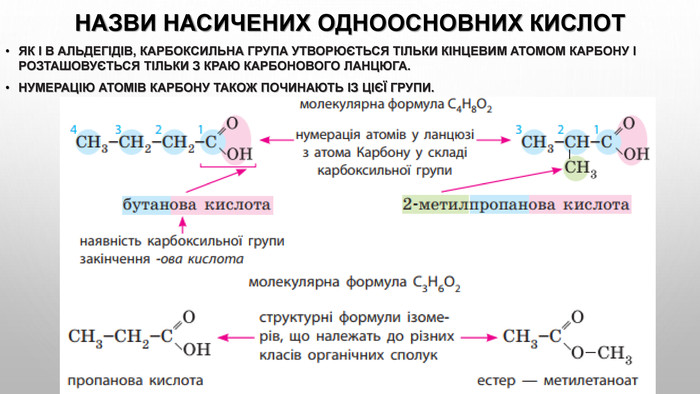
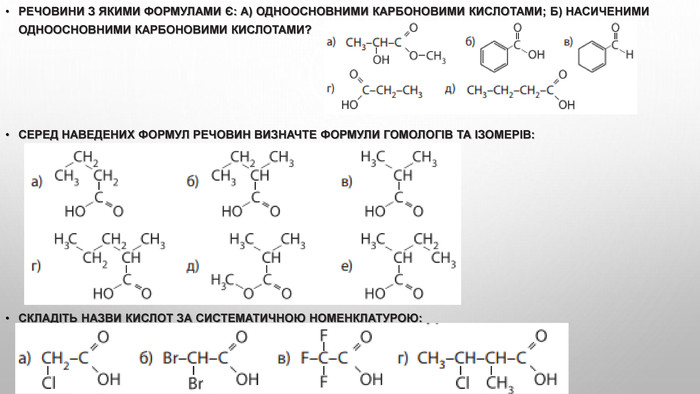
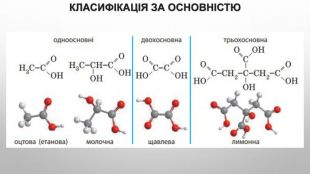
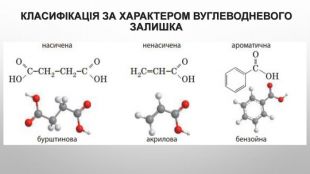
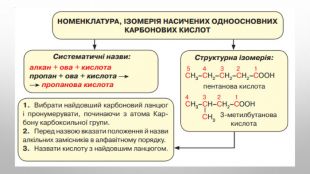
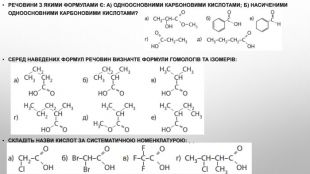
Ізомерія карбонових кислот Структурна ізомерія- Ізомерія скелета у вуглеводневому радикалі (починаючи із C4);- міжкласова ізомерія, починаючи із C2. Наприклад, формулі C2 H4 O2 відповідають три ізомери, що належать до різних класів органічних сполук. Просторова ізомерія можлива цис - транс - ізомерія в разі ненасичених карбонових кислот. Наприклад:
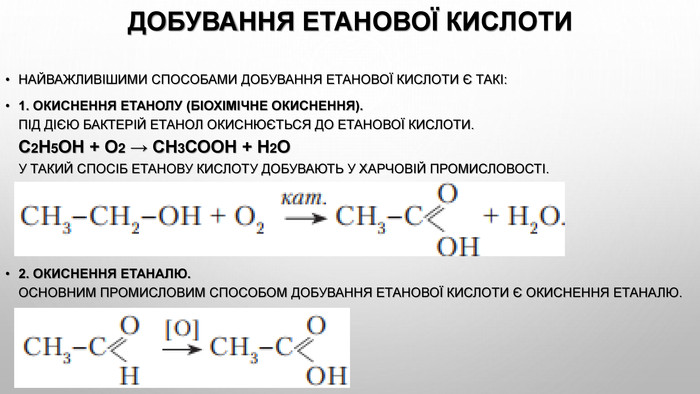
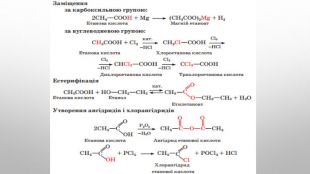
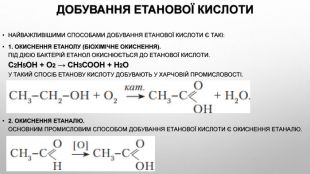
До. БУвання етановоЇ кислоти Найважливішими способами добування етанової кислоти є такі:1. окиснення етанолу (біохімічне окиснення). Під дією бактерій етанол окиснюється до етанової кислоти. С2 Н5 ОН + О2 → СН3 СООН + Н2 ОУ такий спосіб етанову кислоту добувають у харчовій промисловості.2. окиснення етаналю. Основним промисловим способом добування етанової кислоти є окиснення етаналю.
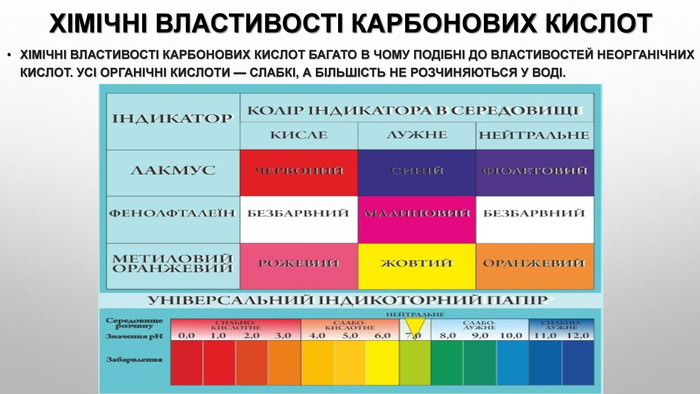
ЛАБОРАТОРНИЙ ДОСЛІД № 1 Виявлення органічних кислот у харчових продуктах За допомогою піпетки або скляної палички нанесіть по 1—2 краплі рідкого молочнокислого продукту, соку квашеної капусти, яблучного або лимонного соку на універсальні індикаторні папірці. Чи змінюється забарвлення індикатора в кожному випадку? Якщо так, то як саме?Зробіть відповідні висновки. Відео до уроку:http://interactive.ranok.com.ua/theme/contentview/serednya-ta-starsha-shkola/hmya-10-klas/14109-laboratorn-dosldi/laboratorniyi-dosld-1-viyavlennya-organchnih-kislot-y-harchovih-prodyktah
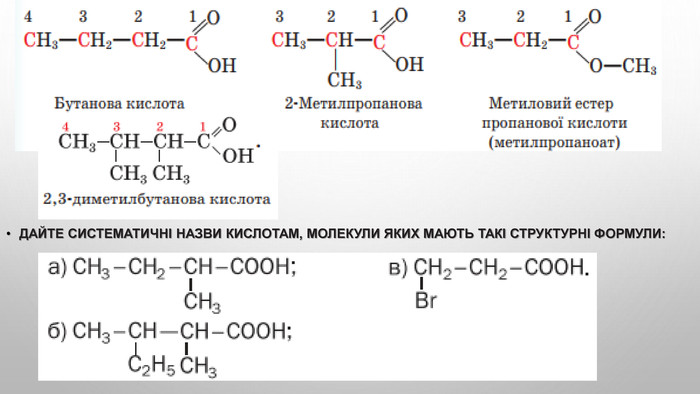
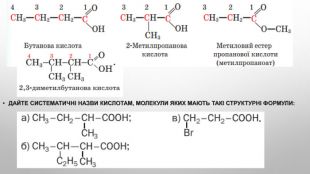
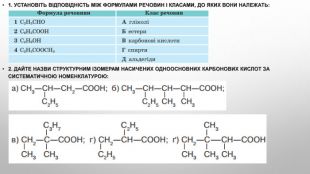
3. Складіть структурні формули кислот за їхніми назвами: а) 2,2-диметилбутанова кислота; б) 2-метил-3-хлоро-пентанова кислота; в) 2-етил-3-метилпентанова кислота.4. Складіть рівняння реакцій між речовинами: 5. Дано речовини: етанол, натрій гідроксид, калій карбонат, кальцій оксид, купрум(ІІ) гідроксид, водень. Установіть, з якими з них реагуватимуть етанова й сульфатна кислоти. Напишіть молекулярні та, де можливо, йонні рівняння хімічних реакцій.
6. Складіть рівняння хімічних реакцій за схемою. Назвіть речовини, позначені літерами А, Б і В.7. Обчисліть масу етанової кислоти, що прореагувала з магнієм, якщо виділився водень об’ємом 33,6 л (н. у.) 8. Етанову кислоту кількістю речовини 0,3 моль повністю нейтралізували розчином натрій гідроксиду. Обчисліть масу утвореної солі. Назвіть її. 9. У побуті розчин етанової кислоти з масовою часткою 9 % застосовують як смаковий засіб і консервант. Обчисліть, яку масу розчину з масовою часткою кислоти 85 % треба взяти, щоб отримати оцет масою 8 кг. 10. Визначте масову частку оцтової кислоти в розчині, виготовленому додаванням до 100 г 80% розчину кислоти:а) 100 мл води;б) 100 г 9% розчину цієї кислоти;в) 100 мл 20% розчину цієї кислоти, густина якого 1,026 г / мл
11. Яка маса розчину натрій гідроксиду з масовою часткою лугу 20% витрачається на нейтралізацію 50 г розчину пропанової кислоти з масовою часткою кислоти 7,4%?12. Яким об’ємом води потрібно розбавити 150 мл оцтової есенції (розчин оцтової кислоти з її масовою часткою 70% і густиною 1,07 г / см3), щоб виготовити розчин із масовою часткою оцтової кислоти 5%?13. У суміш мурашиної та оцтової кислот масою 15,2 г добавили над лишок цинку. При цьому виділилося 3,36 л газу (н. у.). Визначте масові частки кислот у суміші. 14. Запишіть у схемах перетворень замість крапок формули сполук і складіть рівняння відповідних реакцій: 15. Наведіть рівняння реакцій, що підтверджують слушність порад:«Щоб очистити чайник від накипу – суміші карбонатів Кальцію і Магнію – приблизно на дві третини заповніть його водою, на одну третину – столовим оцтом. Розчин закип’ятіть, потім залиште його в чайнику до повного охолодження. Після цього воду злийте, а чайник промийте від залишків накипу». «Гіркоту вершковому маслу надає бутанова кислота, що утворюється в ньому внаслідок окиснення. Щоб позбавитися неприємного присмаку й запаху, згіркле масло потрібно ретельно промити водним розчином харчової соди».


про публікацію авторської розробки
Додати розробку
















-

Теребіленко Людмила Володимирівна
28.01.2024 в 18:09
Дякую
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Евсеєнко Інна Геннадіївна
08.02.2022 в 10:04
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Слобідчук М С
25.11.2021 в 11:57
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Аніщенко Олена Валеріївна
15.02.2021 в 10:46
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
Показати ще 1 відгук