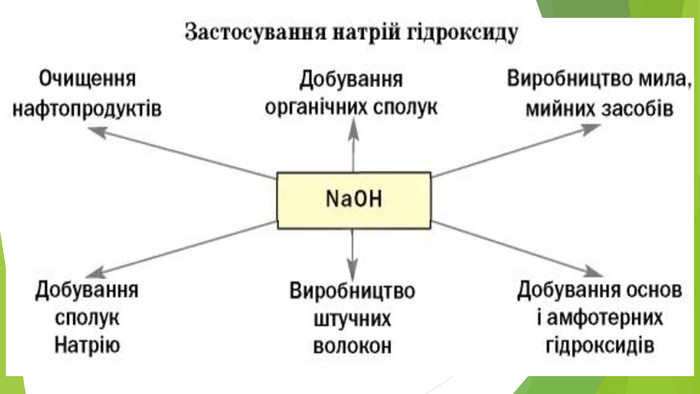
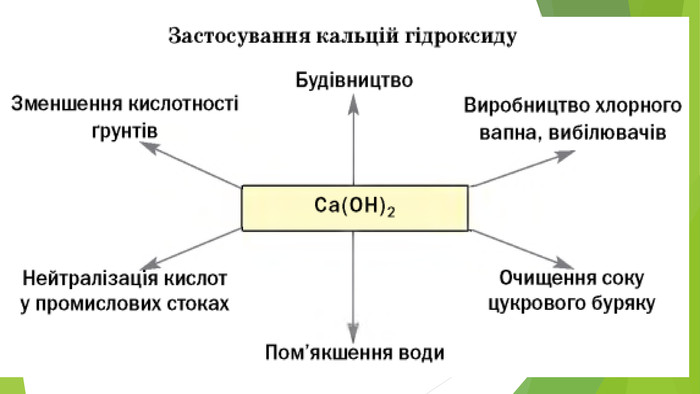
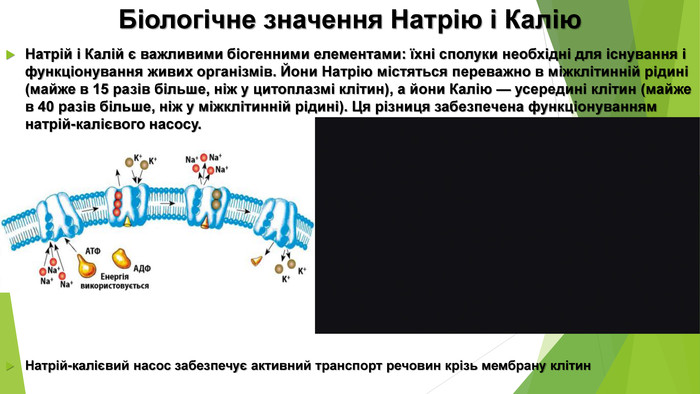
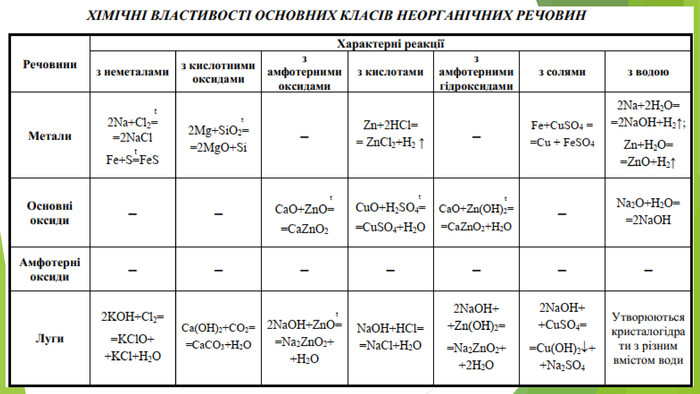
Презентація з теми: "Основи. Властивості, застосування гідроксидів Натрію і Кальцію"
Про матеріал
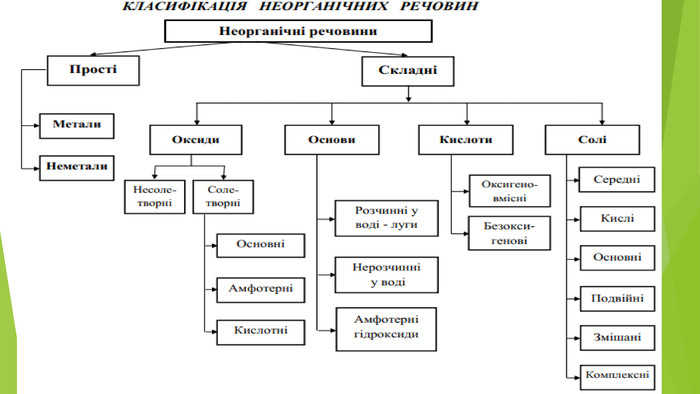
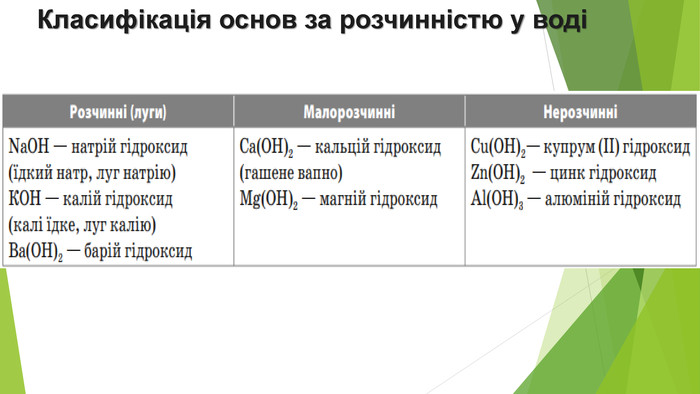
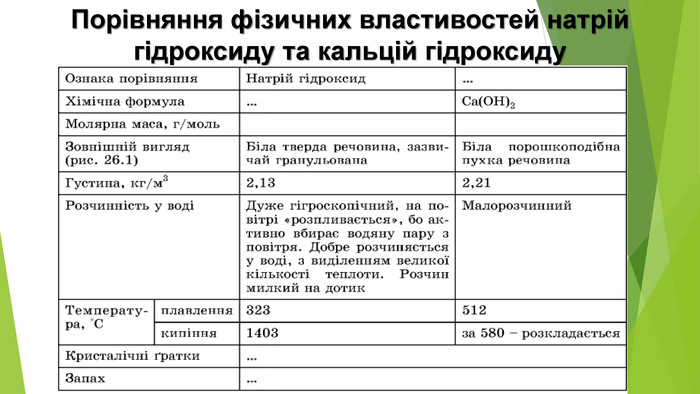
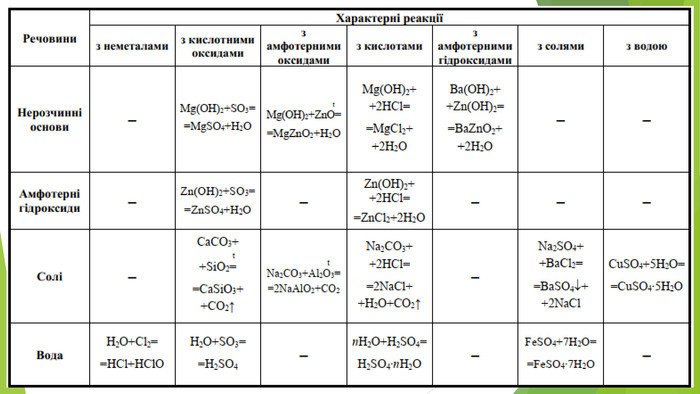
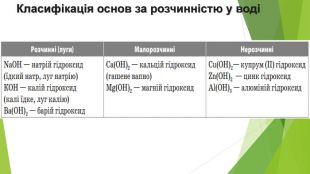
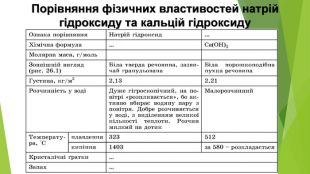
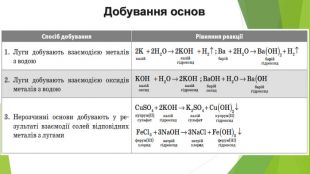
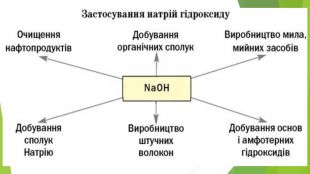
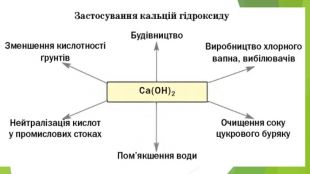
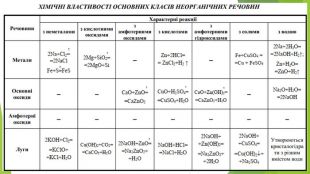
Презентація з теми: "Основи. Властивості, застосування гідроксидів Натрію і Кальцію."
За матеріалами шкільних підручників та довідників. Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки
pptx
Оцінка розробки

Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку