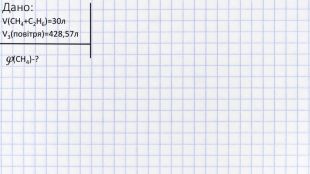
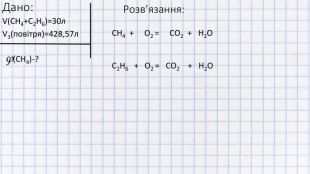
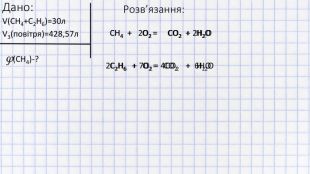
Рішення задач на суміш газів
Про матеріал
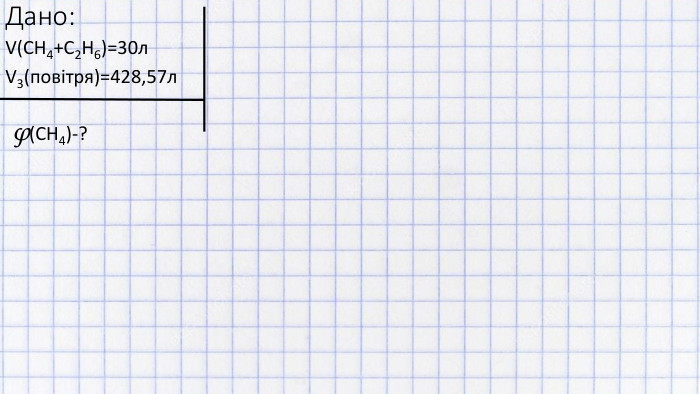
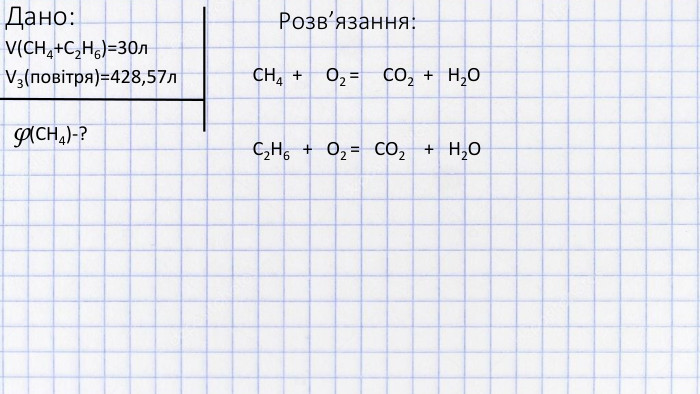
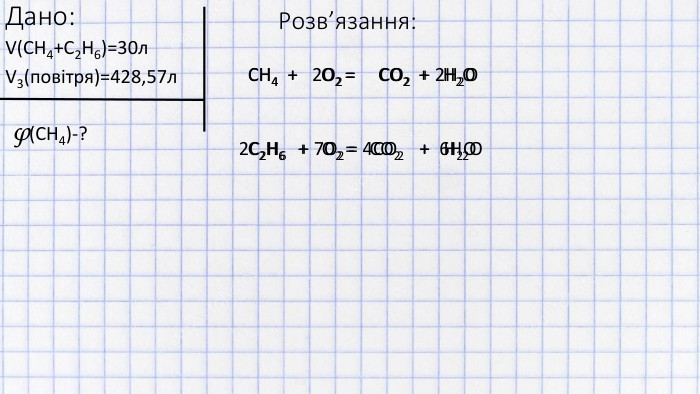
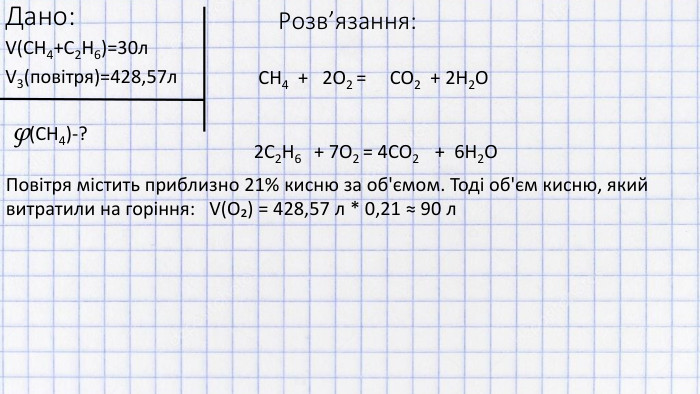
Дане відео показує, як вирішувати задачі на визначення об'ємної частки компонента газової суміші, котра спалюється при тому, що обидва гази горять (н.у.)
Також на основі презентації створене відео:
https://youtu.be/vjY98aqqZCU Перегляд файлу
Зміст слайдів


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку