Розробка конспекту для дитини з інклюзією



22 листопада
Класна робота
Тема:”Хімічні формули речовин. Прості та складні речовини. Багатоманітність речовин”
Проста речовина - хімічна сполука, утворена атомами ОДНОГО хімічного елементу.
Складна речовина – хімічна сполука, утворена атомами РІЗНИХ хімічних елементів
Проста речовина має формулу О3.
О3: Три - це ІНДЕКС, вказує на кількість АТОМІВ оксигену в молекулі озону.
2О3 : Два – КОЕФІЦІЄНТ, вказує на кількість МОЛЕКУЛ озону.
Формула води Н2О, вода – складна речовина, до її кількісного складу входять 2 атоми гідрогену та 1 атом оксигену, якісний склад – атоми гідрогену та атоми оксигену, об’єм газу у одній пробірці у два рази менше тому, що у цій пробірці виділявся кисень, а його лише один атом у молекулі води, тоді як гідрогену в два рази більше атомів. Цей опит можна віднеси до реакції розкладу.
Багатоманітність речовин.
Прості та складні речовини. Метали та неметали
Зараз відомо понад 20 мільйонів речовин. Хіміки щодня синтезують нові сполуки. Речовини можуть бути простими та складними. До складу простих речовин входять атоми тільки одного елемента. Речовини, молекули яких складаються з атомів різних елементів, пов’язаних між собою постійними співвідношеннями, називають складними речовинами. Складні речовини також називають хімічними сполуками. Наприклад, до складу кисню O2 входять атоми тільки елемента Оксигену. Кисень належить до простих речовин. До складу вуглекислого газу CO2 входять атоми різних елементів: один атом Карбону та два атоми Оксигену. Вуглекислий газ належить до складних речовин.
Дуже важливо розрізняти поняття “хімічний елемент” і “проста речовина”. Наприклад, Карбон як хімічний елемент – це просто вид атомів, який має заряд ядра плюс шість, він може входити до складу простих речовин (графіт, алмаз та ін.) або складних речовин (харчова сода NaHCO3 , крейда CaCO3 . Крім того, необхідно розрізняти поняття “суміш” і “складна речовина”. Речовини, які входять до складу суміші, зберігають свої індивідуальні властивості, тоді як властивості складної речовини суттєво відрізняються від властивостей простих речовин, утворених тими ж самими хімічними елементами.
За своїми властивостями прості речовини поділяються на метали та неметали. Чіткої межі між металами та неметалами не існує.
Метали – це ковкі, пластичні речовини, що мають металічний блиск, здатні проводити тепло та електричний струм. Спільні властивості металів пояснюються їх подібною внутрішньою будовою. Їх атоми утворюють особливий тип атомних кристалів, які називаються металічними кристалами.
Неметали – це хімічні елементи, які утворюють у вільному стані прості речовини, що не виявляють фізичних властивостей металів. Неметали не мають такої схожості у властивостях, як метали. Наприклад, такі метали як алюміній, залізо, срібло мають сріблясто-білий або сірий колір, металічний блиск. Порівняємо деякі неметали: водень – газ, сірка – тверда речовина, алмаз– дуже міцний, але крихкий.
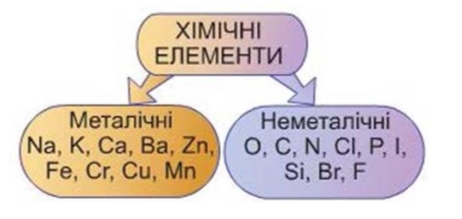
Для всіх металів характерна немолекулярна будова. Для неметалів найбільш характерна молекулярна будова, але зустрічаються неметали й атомної будови (алмаз та силіцій). У періодичній системі металічних елементів значно більше, ніж неметалічних. Неметалічні елементи переважно розміщені у правій частині періодичної системи.
Домашнє завдання (Записати у щоденник)
Опрацювати параграф 13, 14, 15. Запитання №80 на сторінці 84 (письмово).


про публікацію авторської розробки
Додати розробку
