Самостійна робота "Неорганічні речовини і їхні властивості"
Варіант № 1
1. В який ряд формул ввійшли формули простих речовин неметалів:
а) CuO, O2, BaSO4, N2; б) CaO, Zn, H3PO4, CaSO4.
2. Вкажіть забарвлення лакмусу в розчині натрій гідроксиду:
а) синій; б) червоний; в) оранжевий.
3. Вкажіть порядкові номери елементів, що належать до однієї групи: 6, 16, 22
а) 6 і 16; б) 6 і 22; в) 16 і 22.
4. Назвіть газ, шар якого захищає живі організми нашої планети від ультрафіолетових променів сонячного світла, є сильним окисником:
а) озон; б) кисень; в) азот; г) амоніак.
5. Укажіть реагент, за допомогою якого можна відрізнити солі амонію від інших речовин:
а) барій хлорид; б) натрій гідроксид; в) гідроген хлорид; г) кальцій гідроксид.
6. У будові атомів елементів з порядковими номерами №2 і №12 спільними є:
а) кількість електронів на зовнішньому енергетичному рівні; б) кількість всіх електронів;
в) кількість енергетичних рівнів.
Відповідь підтвердити схемами будови атомів цих елементів
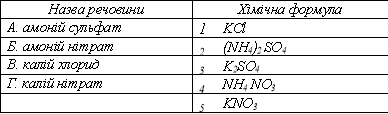 7. Установіть відповідність між назвою речовини та хімічною формулою:
7. Установіть відповідність між назвою речовини та хімічною формулою:

8. Складіть рівняння реакцій за поданою схемою:
(NH4)2CO3 → NH4Cl → NH3 → (NH4)2SO4 → NH4NO3
9. Доберіть коефіцієнти методом електронного балансу:
Hg + HNO3 (розбавл) → Hg(NO3)2 + NO + H2O
10. Обчисліть масу амоніаку, який можна добути з азоту об’ємом 448 л (н.у.), якщо вихід продукту реакції від теоретично можливого складає 62,5%.
Варіант № 2
1. В який ряд формул ввійшли формули простих речовин неметалів:
а) MgCl2, O3, P, NH3; б) K2SiO3 , CaC2, Mg, H2O.
2. Вкажіть забарвлення фенолфталеїну в розчині хлоридної кислоти:
а) синій; б) малиновий; в) безбарвний.
3. Вкажіть порядкові номери елементів, що належать до однієї підгрупи: 14, 32, 22
а) 14 і 32; б) 14 і 22; в) 22 і 32.
4. Назвіть речовину. За звичайних умов безбарвний газ, без запаху, не отруйний, є окисником, має високу реакційну здатність:
а) озон; б) кисень; в) азот; г) аміак.
5. Укажіть реагент, яким можна скористатися для того, щоб виявити амоній хлорид:
а) натрій гідроксид; б) гідроген хлорид; в) натрій нітрат; г) ферум (III) хлорид.
6. У будові атомів елементів з порядковими номерами №3 і №9 спільними є:
а) заряд ядра; б) кількість електронів; в) кількість енергетичних рівнів.
Відповідь підтвердити схемами будови атомів цих елементів
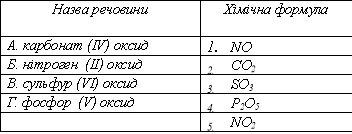 7. Установіть відповідність між назвою речовини та хімічною формулою:
7. Установіть відповідність між назвою речовини та хімічною формулою:

8. Складіть рівняння реакцій за поданою схемою:
SO2 → SO3 → H2SO4 → MgSO4 → K2SO4.
9. Доберіть коефіцієнти методом електронного балансу:
Zn + H2SO4 (конц) → ZnSO4 + S + H2O
10.При взаємодії сірки масою 144 г з воднем було одержано гідроген сульфід об’ємом 75,6 л (н.у.). Обчисліть масову частку виходу продукту реакції від теоретично можливого.
Варіант № 3
1. В який ряд формул ввійшли формули простих речовин неметалів:
а) Cu(OH)2 , Na2SO4 , Na, BaO; б) AgNO3, PH3, S, Cl2.
2. Вкажіть забарвлення метилового оранжевого в розчині натрій гідроксиду:
а) рожевий; б) оранжевий; в) жовтий.
3. Вкажіть порядкові номери елементів, що належать до однієї групи: 12, 20, 21
а) 12 і 20; б) 20 і 21; в) 12 і 21.
4. Назвіть речовину. Кристалічна, тугоплавка, хімічно малоактивна, не проводить електричного струму, має атомні кристалічні гратки в яких кожний атом карбону з’єднується міцними ковалентними зв’язками з чотирма сусідніми атомами:
а) алмаз; б) графіт; в) фулерен; г) білий фосфор.
5. Укажіть реагент, за допомогою якого можна відрізнити хлориди від інших речовин:
а) барій хлорид; б) кальцій гідроксид; в) арґентум нітрат; г)гідроген хлорид.
6. У будові атомів елементів з порядковими номерами №3 і №19 спільними є:
а) кількість енергетичних рівнів; б) кількість всіх електронів;
в) кількість електронів на зовнішньому енергетичному рівні.
Відповідь підтвердити схемами будови атомів цих елементів
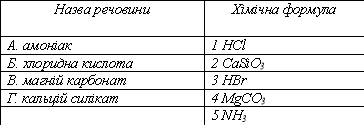 7. Установіть відповідність між назвою речовини та хімічною формулою:
7. Установіть відповідність між назвою речовини та хімічною формулою:

8. Складіть рівняння реакцій за поданою схемою:
S → SO2 → SO3 → H2SO4 → BaSO4.
9. Доберіть коефіцієнти методом електронного балансу:
Al + H2SO4 (конц) → Al2(SO4)3 + S + H2O
10. При взаємодії амоніаку об’ємом 28 л з розчином нітратної кислоти утвориться амоній нітрат масою 90 г. Яку масову частку це складає від теоретичного?
Варіант № 4
1. В який ряд формул ввійшли формули простих речовин неметалів:
а) Li2O, Ba, NaOH, Ni; б) CaCO3, P2O5 , S, Si.
2. Вкажіть забарвлення лакмусу в розчині хлоридної кислоти:
а) синій; б) червоний; в) оранжевий.
3. Вкажіть порядкові номери елементів, що належать до одного періоду: 19, 18, 29
а) 19 і 18; б) 19 і 29; в) 18 і 29.
4. Назвіть просту речовину Карбону із 60 атомами в молекулі – С60:
а) алмаз; б) графіт; в) фулерен; г) чорний фосфор.
5. Укажіть реагент, за допомогою якого можна визначити вуглекислий газ:
а) вапняна вода; б) тліюча тріска; в) горюча тріска; г) метилоранж.
6. У будові атомів елементів з порядковими номерами №11 і №17 спільними є:
а) кількість електронів на зовнішньому енергетичному рівні;
б) кількість енергетичних рівнів; в) кількість всіх електронів.
Відповідь підтвердити схемами будови атомів цих елементів
7. Установіть відповідність між назвою речовини та хімічною формулою:


8. Складіть рівняння реакцій за поданою схемою:
P → P2O5 → H3PO4 → Ca3(PO4)2 → H3PO4
9.Доберіть коефіцієнти методом електронного балансу:
Al + HNO3 (конц) → Al(NO3)3 + NO2↑ + H2O
10. Яку масу сірки спалено, якщо добуто діоксид сульфуру об’ємом 201,6 л, що становить 85% від теоретичного?
Варіант № 5
1. В який ряд формул ввійшли формули простих речовин неметалів:
а) KCl, NO2, Cu, K; б) S, P, Mg, Hg.
2. Вкажіть забарвлення фенолфталеїну в розчині калій гідроксиду:
а) безбарвний; б) рожевий; в) малиновий.
3. Вкажіть порядкові номери елементів, що належать до однієї групи: 20, 29, 30
а) 20 і 29; б) 20 і 30; в) 29 і 30.
4. Явище існування хімічного елемента у вигляді двох або кількох простих речовин, різних за властивостями і будовою називається:
а) адсорбцією; в) алотропією;
б) парниковим ефектом; г) кислотними дощами.
5. Укажіть реагент, яким можна скористатися, щоб виявити натрію сульфат:
а) барій хлорид; в) розчин лугу;
б) натрій нітрат; г) ферум (III) хлорид.
6. У будові атомів елементів з порядковими номерами №4 і №20 спільними є:
а) кількість всіх електронів; б) кількість електронів на зовнішньому енергетичному рівні;
в) заряд ядра;
Відповідь підтвердити схемами будови атомів цих елементів
7. Установіть відповідність між назвою речовини та хімічною формулою:


8. Складіть рівняння реакцій за поданою схемою:
N2 → NO → NO2 → HNO3 → NaNO3
9. Доберіть коефіцієнти методом електронного балансу:
Mg + HNO3 (розбавл) → Mg(NO3)2 + N2 + H2O
10. При каталітичному окисненні амоніаку масою 17 г одержали нітроген(IV) оксид об’ємом 20 л. Яку масову частку складає цей вихід від теоретичного?


про публікацію авторської розробки
Додати розробку

-

MARG
08.05.2020 в 19:51
Извините, а где ответы взять ?
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Оганян Тетяна Іванівна
08.05.2020 в 14:47
Щиро дякую Вам!
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Ростя Анна Володимирівна
02.04.2020 в 22:21
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Бородій Наталія
23.02.2020 в 15:21
Дякую!!!!!!!!!!
Загальна:
4.7
Структурованість
5.0
Оригінальність викладу
4.0
Відповідність темі
5.0
-

Щеглова Ірина Аркадіївна
13.02.2020 в 02:19
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
Показати ще 2 відгука