Синтетичні високомолекулярні речовини. Полімери. Реакції полімеризації і поліконденсації.







![Розгляд схеми будови полімеру: -A-A-A-A-A-A- \ або скорочено [-A-] n Введемо ключові терміни: Мономер (вихідна речовина) — низькомолекулярна сполука, з якої синтезують полімер. Структурна (елементарна) ланка ( -A- ) — група атомів, що багаторазово повторюється в макромолекулі полімеру. Ступінь полімеризації (n) — число, що показує кількість структурних ланок у макромолекулі. IV. Вивчення нового матеріалу Розгляд схеми будови полімеру: -A-A-A-A-A-A- \ або скорочено [-A-] n Введемо ключові терміни: Мономер (вихідна речовина) — низькомолекулярна сполука, з якої синтезують полімер. Структурна (елементарна) ланка ( -A- ) — група атомів, що багаторазово повторюється в макромолекулі полімеру. Ступінь полімеризації (n) — число, що показує кількість структурних ланок у макромолекулі. IV. Вивчення нового матеріалу](/uploads/files/1569024/500679/560229_images/8.jpg)



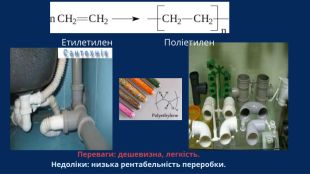
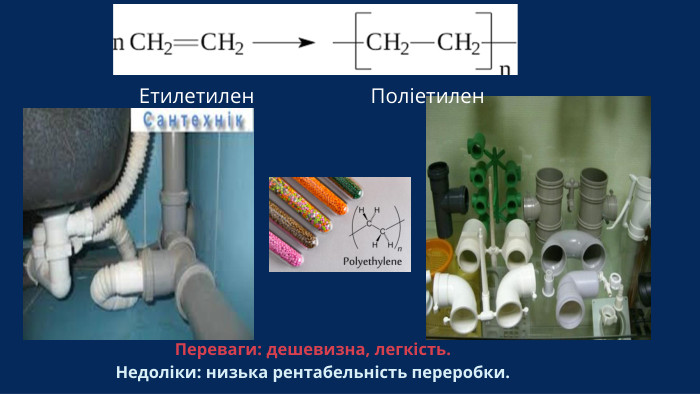
![IV. Вивчення нового матеріалу Приклад 1: Синтез поліетилену Мономер: етен (етилен) n CH 2=CH 2 → [-CH 2-CH 2-] n етен поліетилен Структурна ланка:-CH 2-CH 2 Приклад 2: Синтез полівінілхлориду (PVC) Мономер: вінілхлорид n CH 2=CHCl(хлороетен) n CH 2=CHCl → [-CH 2-CHCl ] n IV. Вивчення нового матеріалу Приклад 1: Синтез поліетилену Мономер: етен (етилен) n CH 2=CH 2 → [-CH 2-CH 2-] n етен поліетилен Структурна ланка:-CH 2-CH 2 Приклад 2: Синтез полівінілхлориду (PVC) Мономер: вінілхлорид n CH 2=CHCl(хлороетен) n CH 2=CHCl → [-CH 2-CHCl ] n](/uploads/files/1569024/500679/560229_images/12.jpg)








![IV. Вивчення нового матеріалу Приклад: Синтез капрону (поліаміду)Мономер для капрону (спрощено) — це амінокислота, яка має на одному кінці аміногрупу (NH2), а на іншому — карбоксильну групу (-COOH). Наприклад, амінокапронова кислота. Схема взаємодії двох молекул (відщеплення води): HOOC-(CH 2) 5-NH2 + HOOC-(CH 2) 5-NH 2 → HOOC-(CH 2) 5-NH-CO-(CH 2) 5 NH 2 + H 2 O Утворюється амідний зв'язок-NH-CO Загальне рівняння поліконденсації: n H 2 N-(CH 2) 5-COOH → -HN-(CH 2) 5-CO-] n + n H 2 O амінокапронова кислота полікапроамід (капрон) + вода IV. Вивчення нового матеріалу Приклад: Синтез капрону (поліаміду)Мономер для капрону (спрощено) — це амінокислота, яка має на одному кінці аміногрупу (NH2), а на іншому — карбоксильну групу (-COOH). Наприклад, амінокапронова кислота. Схема взаємодії двох молекул (відщеплення води): HOOC-(CH 2) 5-NH2 + HOOC-(CH 2) 5-NH 2 → HOOC-(CH 2) 5-NH-CO-(CH 2) 5 NH 2 + H 2 O Утворюється амідний зв'язок-NH-CO Загальне рівняння поліконденсації: n H 2 N-(CH 2) 5-COOH → -HN-(CH 2) 5-CO-] n + n H 2 O амінокапронова кислота полікапроамід (капрон) + вода](/uploads/files/1569024/500679/560229_images/27.jpg)
![V. Узагальнення та систематизація знань 2. Тренувальні вправи Завдання 1. Визначте мономер і структурну ланку для тефлону (політетрафторетилену): [-CF 2-CF 2-] n Відповідь: Структурна ланка: -CF 2-CF 2 . Мономер: тетрафторетен CF 2=CF 2 . (Реакція полімеризації). V. Узагальнення та систематизація знань 2. Тренувальні вправи Завдання 1. Визначте мономер і структурну ланку для тефлону (політетрафторетилену): [-CF 2-CF 2-] n Відповідь: Структурна ланка: -CF 2-CF 2 . Мономер: тетрафторетен CF 2=CF 2 . (Реакція полімеризації).](/uploads/files/1569024/500679/560229_images/30.jpg)




Мета уроку: Навчальна: сформувати поняття про високомолекулярні сполуки (ВМС), полімери, мономери, структурну ланку, ступінь полімеризації; розглянути класифікацію ВМС; вивчити сутність реакцій полімеризації та поліконденсації, їхні механізми та відмінності; навести приклади синтетичних полімерів, добутих цими методами. Розвивальна: розвивати логічне мислення, вміння порівнювати хімічні процеси, складати рівняння реакцій синтезу полімерів; розвивати навички прогнозування властивостей речовин на основі їхньої будови. Виховна: формувати розуміння ролі хімії у створенні нових матеріалів, виховувати екологічну свідомість щодо використання та утилізації синтетичних полімерів.
Тип уроку: комбінований урок засвоєння нових знань та узагальнення раніше вивчених. Обладнання та матеріали: Періодична система хімічних елементів, зразки виробів із полімерів (поліетиленова плівка, пластикові пляшки, зразки синтетичних волокон — капрон, лавсан), мультимедійна презентація зі схемами реакцій. Базові поняття та терміни: високомолекулярні сполуки (ВМС), полімер, макромолекула, мономер, структурна (елементарна) ланка, ступінь полімеризації, реакція полімеризації, реакція поліконденсації.
ХІД УРОКУІ. Організаційний етап ІІ. Мотивація навчальної діяльності та повідомлення теми уроку ІІІ. Актуалізація опорних знань. IV. Вивчення нового матеріалу1. Основні поняття хімії ВМС2. Класифікація полімерів. V. Узагальнення та систематизація знань VI. Підбиття підсумків уроку. VII. Домашнє завдання
ХІД УРОКУІ. Організаційний етап Привітання, перевірка готовності учнів до уроку, налаштування на робочу атмосферу.ІІ. Мотивація навчальної діяльності та повідомлення теми уроку . Озирніться навколо. Ми живемо у світі, який часто називають "пластиковим віком". Корпуси ваших телефонів та ноутбуків, одяг, який ви носите (синтетика), пакування для їжі, труби водопостачання, деталі автомобілів і навіть штучні органи — все це створено з матеріалів, яких не існувало в природі ще 100 років тому. Ці матеріали називають синтетичними високомолекулярними сполуками, або полімерами. Як хімікам вдається створювати такі гігантські молекули? Які механізми лежать в основі їх синтезу? Сьогодні ми відкриємо "кухню" створення сучасних матеріалів.
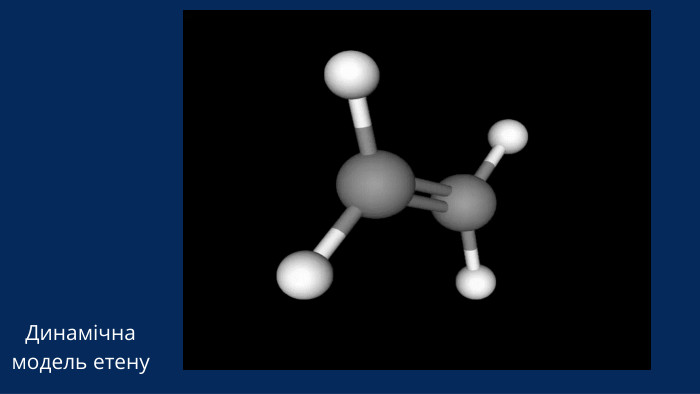
ІІІ. Актуалізація опорних знань Фронтальна бесіда Які речовини вивчає органічна хімія? Пригадайте, що таке ненасичені вуглеводні. Наведіть приклади. Який тип реакцій найбільш характерний для алкенів Які функціональні групи ви знаєте? Назвіть групи, характерні для спиртів, карбонових кислот, амінів.
IV. Вивчення нового матеріалу 1. Основні поняття хімії ВМС Досі ми переважно вивчали низькомолекулярні сполуки (вода, етанол, глюкоза), молярна маса яких рідко перевищує кілька сотень г/моль. Високомолекулярні сполуки (ВМС) — це речовини, молекули яких складаються з тисяч або мільйонів атомів, сполучених ковалентними зв’язками, і мають дуже велику молярну масу (від кількох тисяч до мільйонів г/моль). Їх молекули називають макромолекулами. Більшість ВМС є полімерами. Полімер (від грец. POLy— багато, meros — частина) — це високомолекулярна сполука, макромолекула якої складається з великої кількості повторюваних угруповань атомів.
Розгляд схеми будови полімеру: -A-A-A-A-A-A- \ або скорочено [-A-] n Введемо ключові терміни: Мономер (вихідна речовина) — низькомолекулярна сполука, з якої синтезують полімер. Структурна (елементарна) ланка ( -A- ) — група атомів, що багаторазово повторюється в макромолекулі полімеру. Ступінь полімеризації (n) — число, що показує кількість структурних ланок у макромолекулі. IV. Вивчення нового матеріалу
IV. Вивчення нового матеріалу 2. Класифікація полімерів За походженням: Природні (біополімери): білки, полісахариди (крохмаль, целюлоза), нуклеїнові кислоти. Штучні (модифіковані природні): ацетатне волокно, віскоза. Синтетичні (добуті хімічним синтезом із низькомолекулярних речовин): поліетилен, полівінілхлорид, капрон. (Саме на них ми зосередимося сьогодні).
IV. Вивчення нового матеріалу А) Реакція полімеризаціїВизначення: Це процес сполучення багатьох молекул мономерів у макромолекулу полімеру, який відбувається за рахунок розриву кратних зв’язків (подвійних або потрійних) і не супроводжується виділенням побічних продуктів. Умова: Мономери повинні мати кратні зв'язки (C=C, C≡C) або нестійкі цикли. Механізм (спрощено): Розрив менш міцного π-зв’язку і утворення нових σ-зв’язків між молекулами мономеру. Це багаторазова реакція приєднання. Особливість полімеризації: Маса утвореного полімеру точно дорівнює сумі мас мономерів, що вступили в реакцію. Елементний склад не змінюється.
IV. Вивчення нового матеріалу Поліетилен. Прозора речовина із середньою щільністю 910 ... 970 кг/м3,• Температурою плавлення 105...135°•Міцність на розтяг 12-40 М Па. •Зберігає еластичність до температури - 70°. •Для поліетилену характерна низька розчинність в органічних розчинниках і стійкість до дії кислот, лугів і солей, висока водостійкість.• Недоліками поліетилену є низька теплостійкість, низька адгезія до клеїв, схильність до старіння і ушкодження гризунами. На основі поліетилену виготовляють труби, плівки, пінопласти, деталі санітарно-технічних улаштувань і електроізоляцію
Полівінілхлорид -•Один із найпоширеніших полімерів, застосовуваних у будівництві, - прозорий, жорсткий і міцний при кімнатній температурі.• Густина полівінілхлориду 1350-1460 кг/м3.• Водопоглинання за 24 г 0,1-0,5•Температура розм’якшення близько 80°•Теплостійкість 60°.• Полімер стійкий до дії кислот, лугів, спирту, бензину, тому його застосовують для виробництва труб, захисних покриттів, місткостей. •Цей полімер добре зарекомендував себе при одержанні лінолеумів , погонажних виробів, гідроізоляційних плівок, пінопластів .• Недоліком ПВХ є різке зниження міцність при підвищенні температури, повзучість, низька морозостійкість.
Поліпропілен•Найлегших полімерів із середньою густиною 900 ... 905кг/м3, •Випускається у вигляді гранул, рідше у вигляді порошку. •Має гарну прозорість і блиск. •За водостійкістю і хімічною стійкістю не поступається поліетилену, за теплостійкістю і механічними властивостями перевершує його. •Недоліком поліпропілену єне стійкість до низьких температур і чутливість до окислювання.•Цей полімер поки не знайшов широкого застосування в промисловості будівельних матеріалів, але є дуже перспективним для виготовлення труб, фітингів, листів, плівок, санітарно-технічного устаткування.• Вироби з цих полімерів легко зварюються і піддаються механічній обробці.
Полістирол •Прозорий, досить крихкий полімер, що добре забарвлюється і легко перероблюється, із середньою густиною 1100 кг/м3.• Границя міцності при стиску до 110 МПа, при вигині до 95 МПа.• Полімер водо- і атмосферостійкий, стійкий проти кислот і лугів, бензину, рослинних масел, спирту, розчинів солей. •Для полістиролу характерна висока міцність, він пропускає до 90% сонячного світла .•Основні недоліки полістиролу – його крихкість і недостатня стійкість до дії ряду органічних розчинників. •В зоні вогню він легко займається і горить яскравим полум'ям, що коптить.• Із полістиролу виготовляють пінопласти, лицювальні плитки, вентиляційні решітки, раковини .
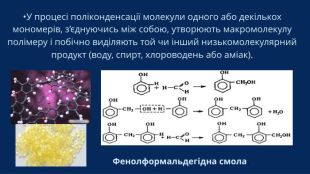
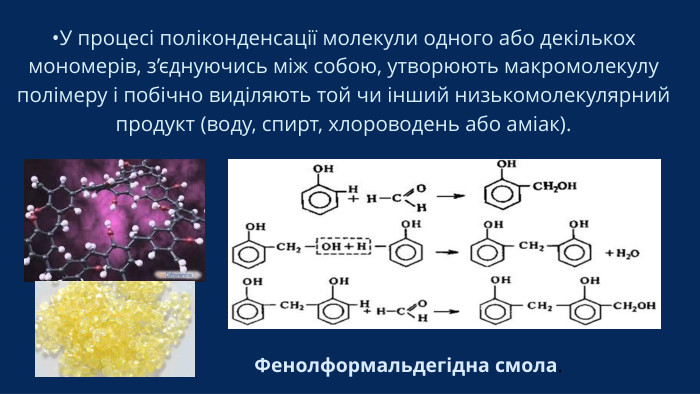
IV. Вивчення нового матеріалу Реакція поліконденсації Це процес утворення полімерів із низькомолекулярних сполук, що супроводжується виділенням побічних низькомолекулярних продуктів (найчастіше води, амоніаку, хлороводню). Умова: Молекули мономеру повинні мати мінімум дві функціональні групи, здатні до взаємодії (наприклад, -OH, -COOH, -NH₂). Особливість поліконденсації: Маса утвореного полімеру менша за суму мас вихідних мономерів, оскільки частина речовини виділяється у вигляді побічного низькомолекулярного продукту. Елементний склад полімеру відрізняється від складу мономеру.
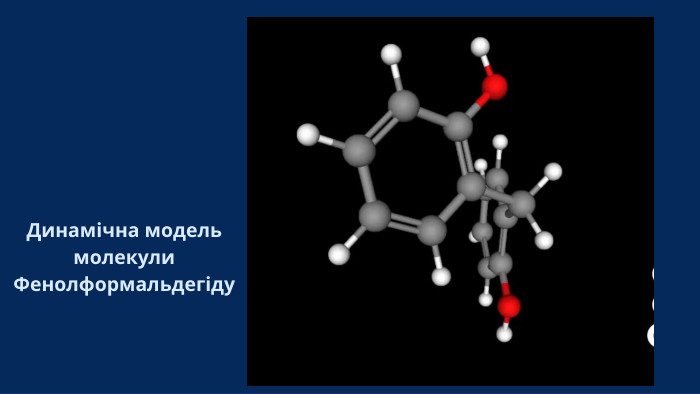
IV. Вивчення нового матеріалу Приклад: Синтез капрону (поліаміду)Мономер для капрону (спрощено) — це амінокислота, яка має на одному кінці аміногрупу (NH2), а на іншому — карбоксильну групу (-COOH). Наприклад, амінокапронова кислота. Схема взаємодії двох молекул (відщеплення води): HOOC-(CH 2) 5-NH2 + HOOC-(CH 2) 5-NH 2 → HOOC-(CH 2) 5-NH-CO-(CH 2) 5 NH 2 + H 2 O Утворюється амідний зв'язок-NH-CO Загальне рівняння поліконденсації: n H 2 N-(CH 2) 5-COOH → -HN-(CH 2) 5-CO-] n + n H 2 O амінокапронова кислота полікапроамід (капрон) + вода
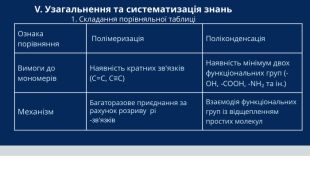
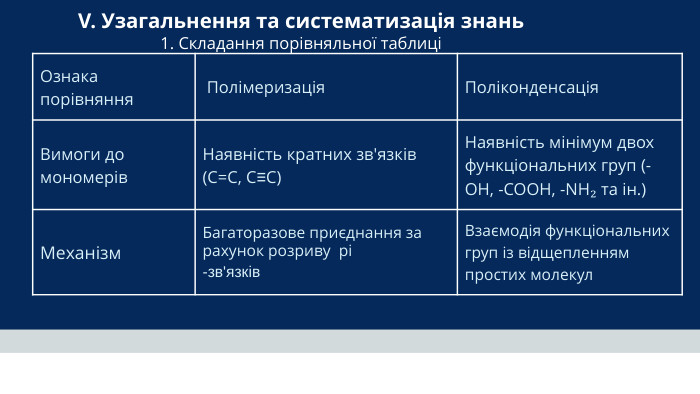
Ознака порівняння Полімеризація Поліконденсація. Вимоги до мономерів. Наявність кратних зв'язків (C=C, C≡C)Наявність мінімум двох функціональних груп (-OH, -COOH, -NH₂ та ін.)Механізм. Багаторазове приєднання за рахунок розриву pi -зв'язків. Взаємодія функціональних груп із відщепленням простих молекул. V. Узагальнення та систематизація знань 1. Складання порівняльної таблиці
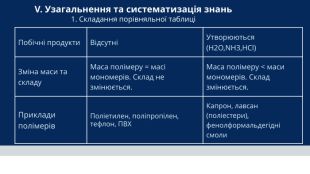
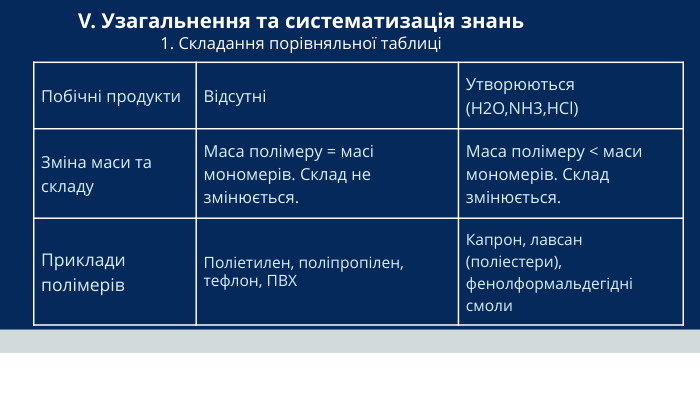
Побічні продукти. ВідсутніУтворюються (H2O,NH3,HCl)Зміна маси та складу. Маса полімеру = масі мономерів. Склад не змінюється. Маса полімеру < маси мономерів. Склад змінюється. Приклади полімерів. Поліетилен, поліпропілен, тефлон, ПВХКапрон, лавсан (поліестери), фенолформальдегідні смоли. V. Узагальнення та систематизація знань 1. Складання порівняльної таблиці
V. Узагальнення та систематизація знань 2. Тренувальні вправи Завдання 3 . Середня відносна молекулярна маса поліетилену становить 280 000. Визначте середній ступінь полімеризації (n). Розв'язання: Формула мономеру (етену) — C 2 H 4 Формула структурної ланки — -CH 2-CH 2- Молярна маса структурної ланки: M(ланки) = = 28г/моль (або M r = 28 Mr(полімеру) = n Mr(ланки)n = Mr(полімеру) / Mr(ланки) = 280000 / 28 = 10000. Відповідь: Середній ступінь полімеризації — 10 000.
VI. Підбиття підсумків уроку, рефлексія Слово вчителя: Сьогодні ми заклали фундамент розуміння хімії високомолекулярних сполук. Ми з'ясували, чим полімеризація відрізняється від поліконденсації. На наступних уроках ми детальніше розглянемо властивості та застосування цих матеріалів, пластмас і волокон, а також поговоримо про екологічні проблеми, пов'язані з ними. Рефлексія: Що сьогодні було найскладнішим для розуміння?Чи зможете ви тепер, дивлячись на формулу полімеру, сказати, яким методом його отримали?
VII. Домашнє завдання Опрацювати матеріал параграфа підручника (відповідно до програми). Вивчити визначення нових термінів. Письмово: Написати рівняння реакції полімеризації стиролу (вінілбензену)C6 H5-CH=CH2для отримання полістиролу. Творче завдання (на випередження): Підготувати коротке повідомлення про одну з екологічних проблем, пов'язаних із використанням синтетичних полімерів (наприклад, "Велике тихоокеанське сміттєва пляма" або "Мікропластик").


про публікацію авторської розробки
Додати розробку