Тест « Електронна формула»
Тест: «Електронна формула»
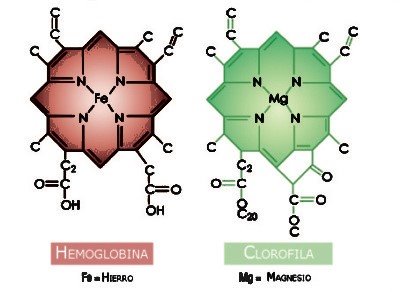
Атом феруму, завдяки своїй електронній будові, створює гемоглобін, що переносить кисень в організмі. Вміст гемоглобіну у крові людини: чоловіки-130-160г/л; жінки-120/160г/л.
«Функція феруму - підтримувати життя на планеті».
Атом магнію, завдяки своїй електронній будові, створює зелений пігмет хлорофіл, за допомогою якого рослини поглинають сонячну енергію та здійснюють фотосинтез.
«Функція магнію- колообіг кисню у природі »
Електронна формула атому визначає функції мікросистеми- атом.
Завдання: виконай тест та опиши один із хімічних елементів,що відіграє важливу роль у біосфері.
На що вказує електронна формула?
Електронна формула.
Порядковий номер
Положення в Періодичній системі
Кількість протонів та нейтронів
Формула нукліду
Формула вищого оксиду
Формула гідриду
Формула гідроксиду
1)Укажіть відповідність між електронною формулою та порядковим номером атому:
А)1S22S22P63S23P63d0 1) 12 4) 8
Б)1S22S22P63S23P03d0 2) 13
В)1S22S22P4 3)18
2)Укажіть відповідність між електронною формулою атому та положенням елементу в Періодичній системі:
А)1S22S2P63S13P03d0 1) 3 малий , I А 4) 3 малий, II А
Б)1S22S22P63S23P03d0 2) 4великий, IIIБ;
В)1S22S22P63S23P64S2d1 3)1 малий, V А;
3)Укажіть відповідність між електронною формулою атому та зарядом ядра,кількістю електронів,протонів та нейтронів в ньому:
А)1S22S22P63S23P23d0 1) +30,е 30 р=30 n=30;
Б)1S22S22P63S23P63d104S2 2) +31, e 31 р=31 n=31;
В)1S22S22P63S23P63d3 3) +14, e 14 р=14 n=14;
4) + 21, e 21 р= 21 n=21;
4)Установіть відповідність між електронною формулою атому та загальною формулою гідроксиду хімічного елементу:
А)1 S22S22P0 1) ЕОН 4)Н3ЕО4
Б)1S22S22P63S23P63d04s1 2)Е(ОН)3
В)1S22S22P63S23P33d0 3)Е(ОН)2
5)Установіть відповідність між електронною формулою атому та формулою гідриду.
А)1S22S22P63S1 1)CaH2; 4) H2O;
Б) 1S22S22P4 2)NH3;
В) 1S22S22P3 3)NaH;
6)Установіть відповідність між електронною формулою атому та формулою нукліду:
А) 1S22S22P6 1) 94Be; 4) 2010Ne;
Б) 1S22S22P63S23P64S1 2) 3919K;
В) 1S22S22P0 3)2713Al;
7) Установіть відповідність між електронною формулою атому та загальною формулою вищого оксиду елементу:
А) 1S22S22P63S23P23d0 1)Е2О3
Б) 1S22S22P63S13P03d0 2)ЕО2
В) 1S22S22P63S23P63d04S2 3)Е2О
4)ЕО


про публікацію авторської розробки
Додати розробку
