Урок №1 "Вода, склад молекули, поширеність у природі, фізичні властивості"
Розробки уроків складені відповідно нової програми з хімії. Дані матеріали можна використати для підготовки і проведення занять з хімії у 7 класі по темі «Вода».
7 клас Тема «Вода» Урок №1
Тема: Вода, склад молекули, поширеність у природі, фізичні властивості
Мета: Ознайомити учнів з будовою та складом молекули води, фізичними властивостями та поширеністю у природі, формувати в учнів знання про роль води у природі, колообіг води.
Тип уроку: засвоєння нових знань
Обладнання: Схема будови молекули води, склянка з водою, комп’ютер.
Хід уроку
І Організація класу
ІІ. Актуалізація опорних знань (бесіда з учнями).
1. Які речовини називаються простими?
2. Які речовини називаються складними?
3. Які речовини називаються оксидами?
4. Який найпоширеніший оксид на землі?
Отже, як ви зрозуміли тема нашого уроку: «Вода та її властивості».
ІІІ Вивчення нового матеріалу.
(Розповідь вчителя з елементами бесіди)
Вода, Н2O — хімічна речовина у вигляді прозорої безбарвної рідини без запаху і смаку, (в нормальних умовах). У природі існує у трьох агрегатних станах — твердому (лід), рідкому (вода) і газоподібному (водяна пара). Молекула води складається з одного атома Оксигену і двох атомів Гідрогену. Атоми Гідрогену розташовані в молекулі так, що напрямки до них утворюють кут 104,45º із вершиною в центрі атома Оксигену. При заміні атомів Гідрогену (протонів) на атоми дейтерію утворюється модифікація, яка називається важкою водою.
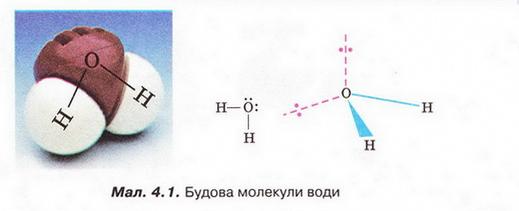
Фізичні властивості води (температура, прозорість, колір, смак, запах) та вплив цих властивостей на здоров'я людини.
Прозорість. Це важливий показник чистоти води. Під прозорістю води розуміється її здатність пропускати світло і робити видимими предмети, що знаходяться на певній глибині. Прозорість води визначається кількістю містяться в ній механічних і хімічних домішок.
Прозорість питної води повинна бути не менше 30 см, а води плавальних басейнів - 20 см.
Колір. Питна вода повинна бути безбарвною. Забарвлення води, як і її каламутність, робить воду неприємною для пиття. Абсолютно безбарвна вода зустрічається рідко, наприклад в підземних водоносних шарах. У відкритих водоймах вода зазвичай має той чи інший відтінок. Жовтуватий відтінок найчастіше свідчить про наявність у воді солей заліза або гумінових речовин. Він характерний для води боліт. Зеленавий колір воді надають мікроводорості.
Запах. Чиста питна вода не повинна мати ніякого запаху.
Будь запах вказує на присутність у воді або продуктів біологічного розпаду рослинних або тваринних організмів, або будь-яких хімічних сполук, сторонніх для питної води. Хоча іноді це лише наслідок надмірної кількості у воді солей сірчаної кислоти, наприклад сірчистого заліза. Це найчастіше характерно для певних мінеральних вод. Фенольний, смоляний та інші запахи свідчать про можливе забруднення води промисловими стічними водами, запах хлору - про надлишкові концентраціях залишкового хлору, який використовується для знезараження питної води і води в плавальних басейнах (вище 0 ,5-0, 6 мг в 1 л води).
Смак. Питна вода не повинна мати сторонніх присмаків. Смак води залежить від її мінерального складу, температури, концентрації розчинених у ній газів (кисню і вуглекислого газу). Кип'ячена вода менш смачна внаслідок втрати газів і двовуглекислого солей кальцію і магнію. Зміни смаку води або поява неприємного смаку свідчать про можливу наявність в ній органічних речовин, продуктів розпаду різних органічних речовин тваринного або рослинного походження.
Температура. Найбільш сприятливою для питної води вважається температура +7 ... +12 ° С. Така вода ефективніше втамовує спрагу, сприяє охолодженню слизової оболонки порожнини рота і стравоходу і викликає посилення діяльності слинних залоз.
Прийом води, що має температуру 5 ° С і нижче, приводить до придушення шлункової секреції, порушення травлення. Дуже холодна вода може привести до місцевого переохолодження носоглотки і простудних захворювань.
Температура води має велике гігієнічне значення і при купанні і плаванні. Відповідно до гігієнічними нормативами вода в закритих плавальних басейнах (для дорослих) повинна мати температуру +25 ... +26 ° С, а для дітей - не менше +26 ° С. Температура води в природних водоймах НЕ нормується.
Вода — одна із найголовніших речовин, потрібних для органічного життя. Рослини та тварини містять понад 60 % води за масою. На Землі водою покрито 70,9% поверхні. Значна її кількість у вигляді льоду і снігу вкриває високі гори і величезні простори Арктики і Антарктиди. Багато води в атмосфері — пара, туман і хмари. Значні кількості води містяться і в земній корі у вигляді підземних вод. У природі вода перебуває не тільки у вільному стані, а і в хімічно зв'язаному. Об'єм прісної води складає лише 3% від всього об’єму води на Землі. Без їжі людина може прожити 30 днів, а без води лише 3-4 дні.
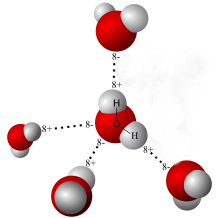
Вона здійснює у природі постійний кругообіг, випаровуючись з поверхні й повертаючись на неї у вигляді опадів. Вода має велике значення для економіки: сільського господарства й промисловості.
ІV. Узагальнення і закріплення вивченого.
1.Яка формула води?
2. Які елементи входять до складу води?
3. Обчислити відносну молекулярну масу води.
4. Знайти масові частки елементів у молекулі води.
5. Скласти схему коло обігу води у природі.
V. Домашнє завдання:
опрацювати параграф. Підібрати цікаві факти про воду та її поширення у природі.
VІ. Підсумок
Що нового дізнались на уроці? Що найбільше сподобалось
Цікаві факти про воду
1. Вода - найбільш проста і звична речовина на планеті. Але в той же час вода таїть в собі безліч загадок. Її досі продовжують досліджувати вчені, знаходячи все більше цікавих фактів…
2. На нашій планеті вода це основа життя. Всі живі істоти і рослини складаються з води: тварини - на 75%, риби - на 75%,медузи - на 99%, картопля - на 76%, яблука - на 85%, помідори - на 90%, огірки - на 95%.
3. Людський організм на 60-70% складається з води, а дитячий на 80%. П'ятимісячний ембріон складається з води на 94%.
4. Один з найбільш водянистих продуктів - це кавун. Кавун на 93% складається з води.
5. Хімічна сполука H2O в чистому вигляді в природі не існує. Вода – універсальний розчинник, вона розчиняє в собі все, що зустрічає на шляху. Наприклад, насолоджуючись смаком колодязної води, ми вливаємо в себе «компот», склад якого не зміг би відтворити,мабуть, ніхто.
6. Вода - єдина субстанція, яка зустрічається в природі в трьох формах: твердій (лід), рідкій і у вигляді газу. До речі, всього 3%води на землі прісна, але при цьому велика частина прісної води міститься в замерзлому стані в льодовиках.
7. У кубічному сантиметрі морської води міститься 1,5 грама білка і немало інших поживних речовин. Учені підрахували, що Атлантичний океан "по поживності" оцінюється в 20 тисяч урожаїв, що збираються в рік на всій суші.
8. Людина за своє життя випиває в середньому 35 тонн води.
9. Вода може знизити ризик виникнення серцевого нападу,якщо людина випиває більше п'яти склянок води в день. Однак такими властивостями володіє лише чиста питна вода.
10. Письменник Грибоєдов в одному зі своїх творів говорив:«Важко забути смак талої води високогірних струмків». Вважається, що саме завдяки талій воді горяни живуть так довго.
11. Потреба людини у воді стоїть на другому місці після кисню. Вода необхідна нам для життя! Як відомо, людина може прожити до 6 тижнів без їжі, але тільки один тиждень без води.
12. 2 % скорочення рівня води в тілі може призвести до 20%-го зменшення розумових і фізичних показників.
13. Як стверджують фахівці, досить випити дві склянки чистої води, щоб подолати депресію і втому.
14. Приблизно 70% Землі вкрито водою. Але тільки 1% з цієї води придатний для пиття.
15. Якщо наш організм втратить 2% води від своєї маси, то виникне відчуття сильної спраги. Якщо рівень втраченої води дійде до 10%,то у людини починаються галюцинації. А вже при втраті 12%рідини, людина не зможе обійтися без допомоги лікаря. При втраті20% рідини людина помирає.
1

про публікацію авторської розробки
Додати розробку
