Урок "Хімічні властивості лугів"
Урок № 46
Тема: Хімічні властивості лугів: дія на індикатори, взаємодія з кислотами, кислотними оксидами, солями.
Мета:
Освітня: закріпити знання про основи; сформувати вміння складати формули основ, давати їм назви та вміння виявляти луги за допомогою індикаторів; вивчити хімічні властивості лугів, розглянути правила техніки безпеки під час роботи з лугами, розвивати навички складання рівнянь хімічних реакцій;
Виховна: виховувати витримку, уміння співпрацювати та об’єктивно оцінювати свою роботу та роботу інших учнів; сприяти формуванню наукового світогляду, ідей матеріальної єдності світу, виховувати толерантне ставлення учнів у процесі групової роботи.
Розвиваюча: активізувати пізнавальну діяльність учнів на всіх етапахуроку, розвивати їх логічне мислення та творчі здібності, продовжитиформувати і розвивати прийоми розумової діяльності (аналізу, порівняння,
абстрагування, конкретизації).
Тип уроку: урок засвоєння нових знань, вмінь і навичок.
Методи навчання: пояснювально-ілюстративні – бесіда, розповідь; наочні – демонстрація; практичні – виконання завдань; репродуктивні, частково – пошукові, творчі; інтерактивні.
Обладнання: таблиця розчинності, періодична система хімічних елементів Д.І.Менделєєва, інтерактивна дошка, мультимедійний проектор, програмне забезпечення - презентація до урокуMicrosoftPowerPoint, опорна схема.
Матеріали:луги, індикатори – універсальний, лакмус, метилоранж і фенолфталеїн, пробірки, хлоридна кислота, купрум(ІІ) сульфат.
Наскрізні змістові лінії: здоров’я і безпека: заходи безпеки під час роботи з лугами.
Хід уроку:
Девіз нашого уроку: Навчаємось не заради школи, а задля життя.
Сенека
(давньоримський філософ)
І. Організаційний момент
а) Привітання;
ДЕВІЗ НАШОГО УРОКУ:
“Навчаємося не заради школи, а задля життя… ”
б) Ще давньоримський філософ Сенека говорив, що навчатися потрібно не заради школи, а задля життя. Тож я запрошую вас до навчання і, сподіваюсь, що сьогодні воно буде для вас цікавим та пізнавальним, а отримані знання знадобляться у житті.
ІІ. Актуалізація опорних знань
Давайте пограємо з вами у гру "Морський бій"
|
|
а |
б |
в |
г |
д |
е |
є |
ж |
з |
|
1 |
|
|
|
|
|
|
KOH |
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
3 |
|
Cu(OH)2 |
|
|
|
|
|
|
|
|
4 |
|
|
|
|
NaOH |
|
|
|
|
|
5 |
|
|
|
|
|
|
|
|
|
|
6 |
|
|
Ca(OH)2 |
|
|
Fe(OH)3 |
|
|
|
|
7 |
|
|
|
|
|
|
|
|
|
|
8 |
|
|
|
|
|
|
|
|
|
|
9 |
|
|
|
|
|
|
|
|
|
Бесіда.
Які ви знаєте основні класи неорганічних сполук?
Що таке основи?
Як класифыкують основи?
ІІІ. Мотивація навчальної діяльності
Учням пропонується на презентації розглянути такі побутові засоби хімії: «Доместос», «Кріт», «Милам»,. «Містер Мускул» – універсальний засіб для кухні, «Кріт» – засіб для прочищення каналізаційних труб та «SAMA» – засіб для чищення кухонних плит, а також медичний препарат «Альмагель», який призначають у разі захворювання шлунку.
Всі ці засоби різні у використанні, а деякі з них є дуже небезпечними для здоров’я. Як ви гадаєте, що входить до їхнього складу? Та об’єднує їх одне: до їхнього складу входять основи.
Проблемні запитання.
- Чому, застосовуючи засоби побутової хімії, необхідно користуватись гумовими рукавичками?
- Чому одні засоби викликають опіки шкіри і є небезпечними для здоров’я людини, а інші – лікують?
Відповідь на ці запитання можна отримати, розглянувши тему сьогоднішнього уроку. Тому, діти, сформулюйте тему нашого з вами уроку. Тема уроку:Хімічні властивості лугів: дія на індикатори, взаємодія з кислотами, кислотними оксидами, солями.
ІV. Вивчення нового матеріалу
На основі фізичних властивостей основ пригадати правила техніки безпеки. Наголосити учням, як себе поводити з лугами.
Хімічні властивості основ
1. Лабораторний дослід № 2. Дія лугів на індикатори(робота в лабораторному зошиті)
Для проведення цієї лабораторної роботи ми використаємо індикатори (складні органічні речовини, що змінюють своє забарвлення взалежності від середовища)
Наливаємо у три посудини натрій гідроксид, а у другу кальцій гідроксид, а в третю – дистильовану воду. Далі в перше заглиблення з кислотами додаємо одну краплю метилового оранжевого, у друге — одну краплю лакмусу, у третє — одну краплю фенолфталеїну. Записуємо спостереження в лабораторному зошиті, ст. 8-9.
Висновок. У розчинах лугів метиловий оранжевий набуває жовтого забарвлення, лакмус — синього, фенолфталеїн — малинового. Отже, розчини лугів можна визначити з допомогою індикатора.
2. Демонстрація. Хімічні властивості основ
Подивимося практично, які властивості повинні мати основи.
Дослід 1. Безпека під час роботи з лугами (папір, тканина, деревина)
Луги – їдкі речовини, вони роз’їдають шкіру, деревину, папір. Треба оберігати очі захисними окулярами, а при потраплянні на шкіру, промити великою кількістю проточної води та змастити розчином оцтової кислоти.
Дослід 2. Взаємодія лугів з кислотами
• Такі реакції називаються реакціями нейтралізації
Реакції між кислотою та основою, у результаті якої утворюється сіль та вода, називають реакціями нейтралізації.
• Що реакція відбулася, нам допоможе побачити індикатор. У дві пробірки наливаємо NaOH і Са(ОН)2, додаємо фенолфталеїн.
А потім по краплях знебарвлюємо розчин хлоридною кислотою. Пропонуємо учням записати рівняння реакцій:
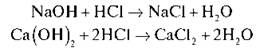
Укажіть тип реакції. (Реакція обміну)
Реакція обміну – це реакція у яких дві речовини обмінюються своїми частинами.
Запишіть самостійно: Ca(OH)2 + HCl =
Дослід 3. Взаємодія лугів з кислотними оксидами.
Збираємо прилад для одержання вуглекислого газу. Одержаний газ пропускаємо крізь розчин кальцій гідроксиду.
— Яку ознаку реакції спостерігаємо? (Випадіння осаду) Записуємо рівняння реакції:
СO2 + Са(ОН)2 ![]() СаСO3 + Н2O
СаСO3 + Н2O
Укажіть тип реакції. (Реакція обміну)
Дослід 4. Взаємодія лугів із солями
У дві пробірки наливаємо CuSO4, Al2(SO4)3, потім по краплях додаємо розчин їдкого натру.
— Які ознаки реакції спостерігаємо? (Утворення нерозчинного осаду)
Напишемо рівняння реакції:
2NaOH +CuSO4 =Na2SO4 +Cu(OH)2↓
Запишіть самостійно: NaOH + Al2(SO4)3 =
Дослід 5. Розкладання нерозчинних основ у процесі нагрівання.
Нерозчинні основи за нагрівання розкладаються на оксид і воду. Перевіримо це на практиці.
Одержіть Сu(OH)2, закріпіть пробірку в пробірко-тримачі.
• Як правильно нагріти пробірку?
• В якій частині полум'я необхідно нагрівати пробірку? (У верхній, найбільш гарячій)
• Що спостерігаємо? Напишемо рівняння реакції:
Cа(OH)2 ![]() СаO + Н2O
СаO + Н2O
Укажіть тип реакції. (Реакція розкладу)
Запишіть самостійно: 2Al(OH)3 = Аl2O3 + 3H2O
Висновок.
З якими властивостями основ ми познайомилися на цьому уроці.
- Реакція нейтралізації.
- Реакція обміну.
- Розклад нерозчинних основ.
- Взаємодія лугів з солями.
- Взаємодія лугів з кислотними оксидами.
V. Узагальнення і систематизації знань
1. Миючі засоби для очищення труб та дезінфекції містять в своєму складі речовини на основі лугів. При неправильному використанні такі засоби можуть спричинити опіки. Якими речовинами потрібно надати першу медичну допомогу при опіках лугами, ґрунтуючись на їх хімічних властивостях?
2. Закінчіть рівняння реакції. Завдання виконується на швидкість у групах
Містер Мускул
1. Be(OH)2+HCl=
2. NaOH+ СuSO4=
3. Ba(OH)2+H2CO3=
4. LiOH + SO3=
ФрекенБок
1. Mn(OH)2+HF=
2. LiOH+ СuSO3=
3. Ca(OH)2+H2SO3=
4. KOH + CO2 =
VІ. Домашнє завдання


про публікацію авторської розробки
Додати розробку
