Урок "Кисень. Узагальнення 1"
Урок "Кисень. Узагальнення 1".
Має презентацію для унаочнення повторення першої частини теми за посиланням:
https://naurok.com.ua/prezentaciya-kisen-uzagalnennya-1-329908.html
Тема: Кисень. Узагальнення
Предметні компетентності:
Учні:
- знають склад повітря; характеристику Оксигену за періодичною системою хімічних елементів; прості речовини, утворені Оксигеном;
- вміють характеризувати фізичні властивості простих речовин;
- розуміють біологічну роль кисню та озону для живих організмів.
Ключові компетентності:
спілкування державною мовою, математична компетентність, основні компетентності у природничих науках і технологіях, інформаційно-цифрова компетентність, соціальна та громадянська компетентності, екологічна грамотність і здорове життя, уміння вчитися упродовж усього життя, ініціативність і підприємливість.
Хід уроку:
Кисень – це речовина, навколо якої обертається земна хімія.
Я. Берцеліус
І. Актуалізація опорних знань:
- Чи знаєте ви, що?..
- Що людина без їжі може прожити кілька тижнів, без води – кілька днів, а без повітря – кілька хвилин.
- Кисень в нас і навколо нас
- Я скрізь навколо тебе є,
- Бо оксиген ім’я моє,
- Я у деревах, у траві,
- В твоїх я жилах, у крові.
- Правда чи ні?
- Кисень є активною речовиною. (так)
- При взаємодії кисню з простими і складними речовинами утворюються оксиди. (так)
- При взємодії кисню з кальцієм утворююється оксид Са2O. (ні)
- При взаємодії водню з киснем утворюється гідроген оксид. (так)
- Вугілля в атмосфері кисню горить яскравим полумʼям. (так)
- Fe2O3 - формула залізної окалини, яка утворюється при горінні заліза в атмосфері кисню. (ні)
- При прожарюванні мідної пластинки над полумʼям пальника спостерігаємо утворення купрум (ІІ) оксиду чорного кольору. (так)
- Сума всіх коефіцієнтів в рівнянні реакції С + О2 = СО2 дорівнює 2. (ні)
- Кількість атомів Оксигену, що беруть участь у реакції 2Mg + O2 = 2MgO дорівнює 2. (так)
- Реакція горіння сірки відповідає рівнянню 2S + 3O2 = 2SO2. (ні)
- Згідно рівняння реакції 4Р + 5О2 = 2Р2О5 , під час реакції утворюється фосфор (ІІІ) оксид. (ні)
- Взаємодія простих речовин з киснем – це реакція сполучення. (так)
ІІ. Узагальнення знань:
1. Походження назви
2. Будова атома
- N ( р+) = +8
- N ( ē ) = -8
- N ( n0) = Ar - N ( р+)
- N ( n0) = 8
3. Характеристика хімічного елемента
|
Характеристика хімічного елемента Оксигену |
|
|
Хімічний символ |
|
|
Металічний – неметалічний елемент |
|
|
Розміщення у періодичній системі хімічних елементів |
|
|
Порядковий номер елемента |
|
|
Період |
|
|
Група, підгрупа |
|
|
Склад атома: |
|
|
Заряд ядра |
|
|
Кількість протонів |
N ( р+) = |
|
Кількість нейтронів N ( n0) = Ar - N ( р+) |
N ( n0) = |
|
Кількість електронів |
N ( ē ) = |
|
Відносна атомна маса елемента |
Аr (О) = |
|
Валентність в сполуках |
|
|
Формула простої речовини, її назва |
|
4. Хімічний елемент – проста речовина
|
Оксиген |
Кисень |
||
|
Хімічний символ |
|
Хімічна формула |
|
|
Порядковий номер |
|
Тип речовини |
|
|
Відносна атомна маса |
|
Відносна молекулярна маса |
|
|
Період |
|
Фізичні властивості |
|
|
Група |
|
Колір |
|
|
Кількість електронів |
|
Запах |
|
|
Заряд ядра |
|
Смак |
|
|
Валентність |
|
Агрегатний стан |
|
|
Характер |
|
Tкип |
|
|
Прості речовини |
|
Tпл |
|
5. Склад повітря
Поширеність у природі:
- літосфера – 46,6 %
- гідросфера – 85,6 %
- атмосфера – 20,91 %
6. Кисень та озон
-
Хімічні елементи у вільному стані існують у формі простих речовин. Так, елемент Оксиген утворює дві прості речовини — кисень
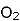 та озон
та озон 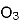 .
.
- Обидві прості речовини утворені одним і тим самим хімічним елементом, а властивості у них різні.
- Отже, кисень і озон — алотропні форми елемента Оксигену. Алотропія зумовлена різною кількістю атомів Оксигену в молекулах речовин.
Складіть речення, вставивши замість крапок слова «Оксиген», «кисень», «озон» у відповідних відмінках
1) … - проста речовина
2) Вода утворена Гідрогеном і …
3) Молекула… складається із двох атомів….
4) У результаті фотосинтезу рослини поглинають вуглекислий газ і виділяють …
5) Найбільший уміст… у гірських породах і мінералах
6) У воді розчиняється погано…
7) В акваріумі риби дихають …, розчиненим у воді
8) … – газ без смаку і запаху
9) … – захищає живі організми від згубного ультрафіолетового проміння
10) … підтримує горіння
11) … займає 1/5 повітря
12) Життєвим газом називають…
7. Фізичні властивості кисню
Серед запропонованого переліку фізичних властивостей виберіть ті, що характерні для кисню.
|
Безбарвний газ
|
У рідкому стані притягується магнітом |
З різким запахом
|
Безбарвна рідина
|
|
Добре розчинний у воді |
Легший за повітря
|
Малорозчинний у воді |
Важчий за повітря
|
|
Тверда речовина
|
Солодкий |
Проводить струм
|
Без запаху
|
8. Явища фізичні та хімічні (відео)
Графічний диктант
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
|
+ |
+ |
- |
+ |
+ |
+ |
- |
+ |
+ |
- |
- |
+ |
- Під час фізичних явищ склад речовини не змінюється.
- Хімічні явища супроводжуються руйнуванням одних молекул і утворенням інших.
- Під час хімічних явищ змінюється агрегатний стан речовини.
- Хімічні явища ще називають хімічними реакціями.
- Під час хімічних явищ атоми елементів зберігаються.
- Зміни, що відбуваються із перегрупуванням атомів і утворенням нових речовин називають хімічними перетвореннями.
- Розчинення цукру у воді – хімічне явище.
- Утворення інею на деревах – фізичне явище.
- Виділення тепла і свічення - ознака хімічного явища.
- Утворення білкової піни – фізичне явище.
- Утворення суміші тирси і залізних ошурок – хімічне явище.
- Хімічні явища завжди супроводжуються фізичними.
9. Типи хімічних реакцій
- А + В = АВ сполучення
- АВ = А + В розкладу
- А + ВС = АС + В заміщення
- АВ + СD = АD + СВ обміну
ІІІ. Систематизація знань:
1. Знайдіть та виправте неточності:
1) N2 + H2 = NH3
2) CuCl2 + KOH = KCl + Cu(OH)2
3) CO + H2O = CO2 + H2
4) SO2 + O2 = 2SO3
5) CuSO4 + Fe = FeSO4 + Cu
6) C + O2 = CO2
7) CuSO4 + NaOH = Na2SO4 + Cu(OH)2
8) 2NO = N2 + O2
2. Складіть рівняння реакцій за поданими схемами:
|
а) P + O2 → P2O5 Na + Br2 → NaBr Ba + O2 → BaO H2 + S → H2S Al + Cl2 → AlCl3 Al + Br2 → AlBr3 Al + O2 → Al2O3 Cu + O2 → CuO |
б) Zn + O2 → ZnO Zn + Cl2 → ZnCl2 H2O → H2 + O2 K + Cl2 → KCl Fe + Cl2 → FeCl2 K + І2 → KІ Li + O2 → Li2O Al + Br2 → AlBr3 |
в) Mg + O2 → MgO Cu + S → CuS CaCO3 → CaO + CO2 Mg + HCl → MgCl2 + H2 Fe2O3 + Al → Al2O3 + Fe Na + S → Na2S Al + S → Al2S3 Na + O2 → Na2O |
3. Розв’яжіть задачі:
- Обчисліть масову частку Оксигену у воді.
- Обчисліть, який об'єм кисню міститься у повітрі об'ємом 250л, якщо повітря на 21% за об'ємом складається з кисню.
4. Інтерактивна вправа “Хрестики - нулики”
Завдання: закресліть лінію, виграшний шлях – формули оксидів.
|
КОН |
SiO2 |
H2O |
|
HCl |
CuO |
K2CO3 |
|
Fe2O3 |
AlCl3 |
H2SO4 |
5. Гра «Дай мені назву»
Робота в групах
Назви мій оксид. Я маю наступний вид:
- NO, Аl2O3, Cu2O, MnO2, FeO,
- Cao, Cl2O7, MgO, Fe2O3, Р2O5.
6. Що потрібно робити людству, аби запобігти екологічній катастрофі?
Повітря щоб чисте, здорове довкілля…
Не мусить людина чинити свавілля!
Бо дихає небо та дихають річки,
на повнії груди хай дихає вічно
планета моя, та, що ненькою зветься.
Життя її хай після нас не зірветься!
Ю.О. Левіна
7. Рефлексія та самооцінювання
Чого б ти не навчився, ти навчаєшся для себе.
Петроній
8. Чомусики
ІV. Домашнє завдання:
- Повторити §§ 21-27;
- Виконати тест;
- Купон на звільнення від домашнього завдання.


про публікацію авторської розробки
Додати розробку
