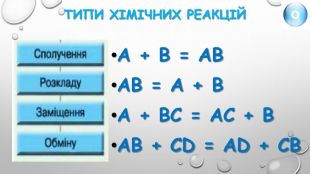
Презентація "Кисень. Узагальнення 1"
Презентація "Кисень. Узагальнення 1".
Має конспект уроку для повторення першої частини теми за посиланням:






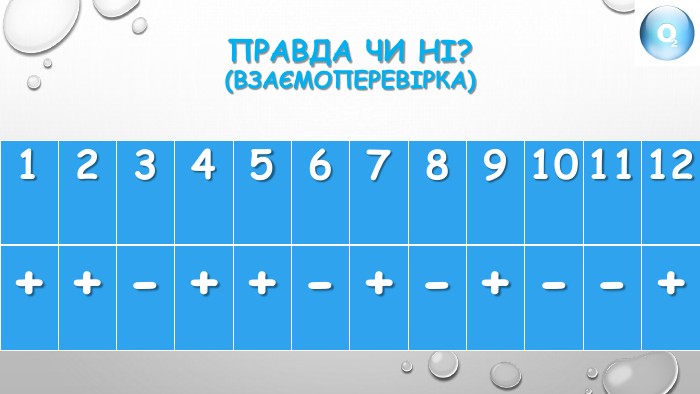



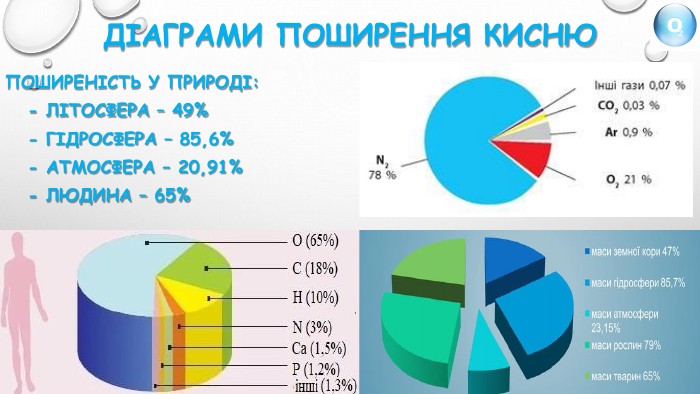
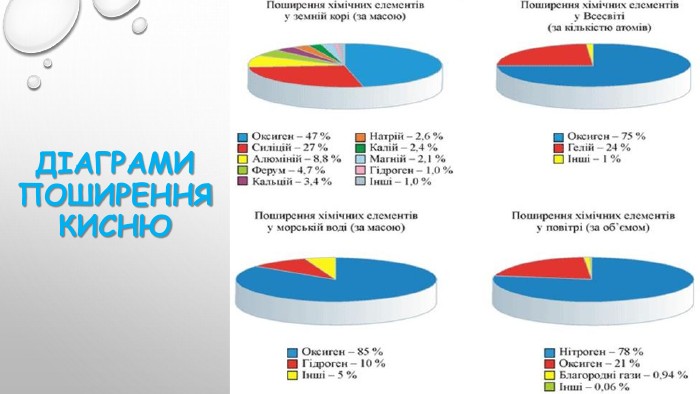


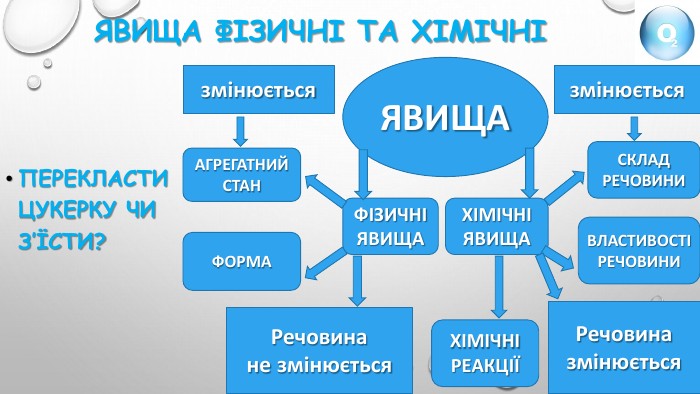


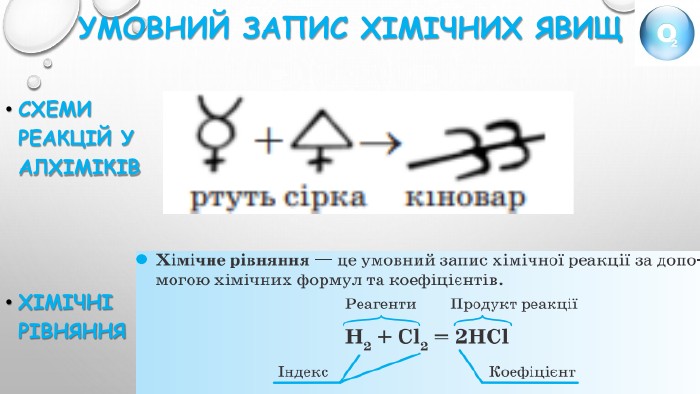
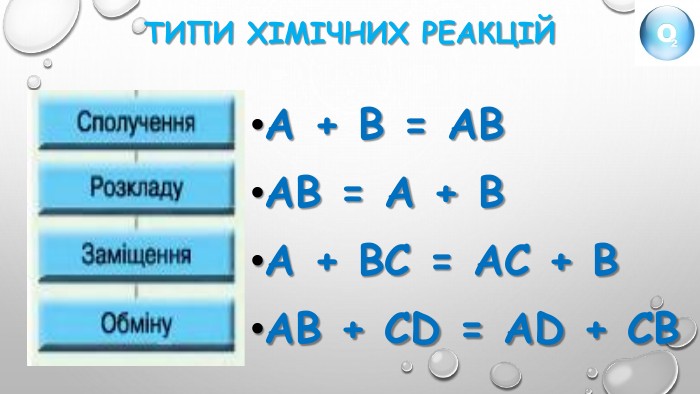







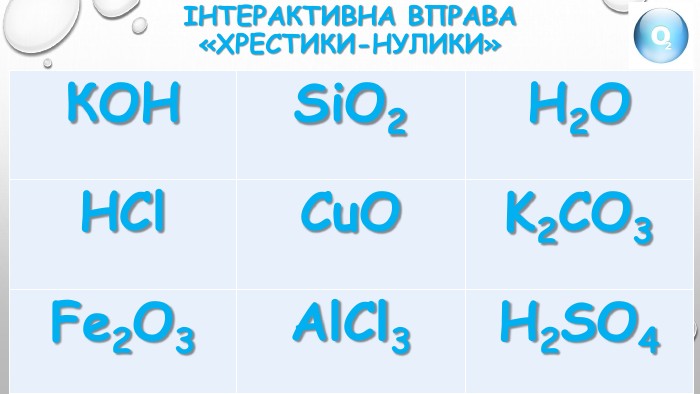














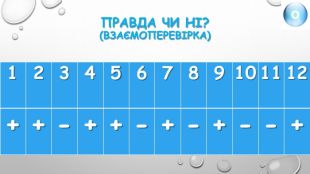
Правда чи ні?1. Кисень є активною речовиною.2. При взаємодії кисню з простими і складними речовинами утворюються оксиди.3. При взємодії кисню з кальцієм утворююється оксид Са2 O.4. При взаємодії водню з киснем утворюється гідроген оксид.5. вугілля в атмосфері кисню горить яскравим полумʼям.6. Fe2 O3 - формула залізної окалини, яка утворюється при горінні заліза в атмосфері кисню .7. При прожарюванні мідної пластинки над полумʼям пальника спостерігаємо утворення купрум (ІІ) оксиду чорного кольору.8. Сума всіх коефіцієнтів в рівнянні реакції С + О2 = СО2 дорівнює 2.9. Кількість атомів Оксигену, що беруть участь у реакції 2 Mg+O2 = 2 Mg. O дорівнює 2.10. Реакція горіння сірки відповідає рівнянню 2 S+3 O2 = 2 SO2.11. Згідно рівняння реакції 4 Р+5 О2 = 2 Р2 О5 , під час реакції утворюється фосфор(ІІІ) оксид.12. Взаємодія простих речовин з киснем – це реакція сполучення.
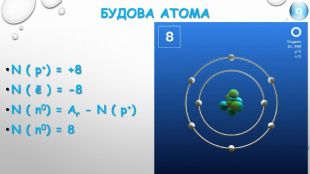
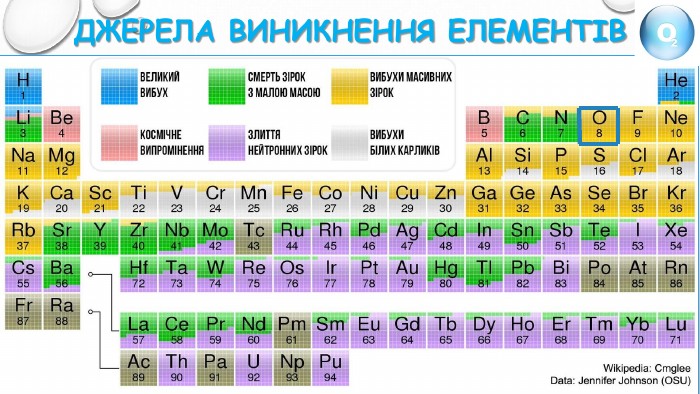
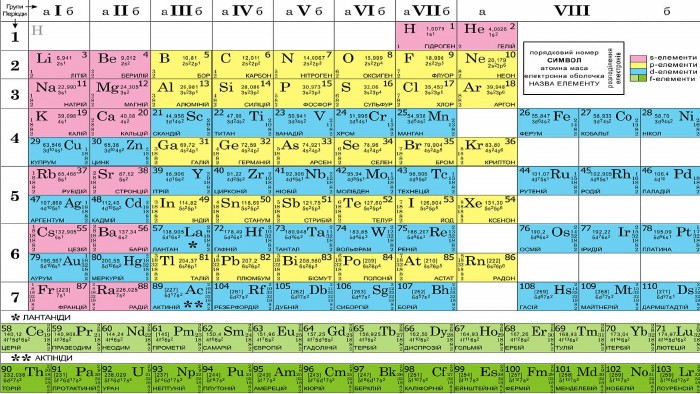
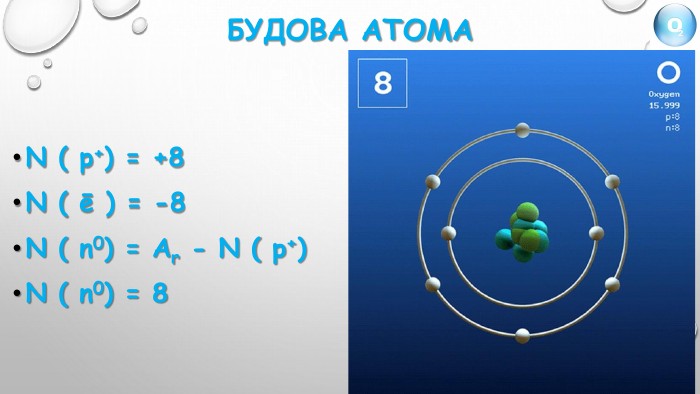
{5 C22544 A-7 EE6-4342-B048-85 BDC9 FD1 C3 A}Характеристика хімічного елемента Оксигену. Хімічний символ ОМеталічний – неметалічний елемент неметал. Розміщення у періодичній системі хімічних елементів. Порядковий номер елемента 8 Період 2 Група, підгрупа VIСклад атома. Заряд ядра +8 Кількість протонів. N ( р+) = +8 Кількість нейтронів N ( n0) = Ar - N ( р+)N ( n0) = 8 Кількість електронів. N ( ē ) = -8 Відносна атомна маса елемента. Аr (О) = 16 Валентність в сполуках ІІФормула простої речовини, її назва О2 - кисень
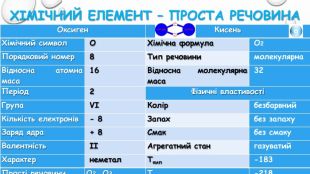
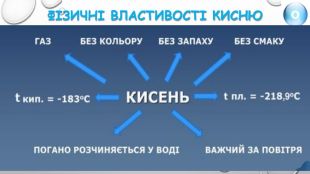
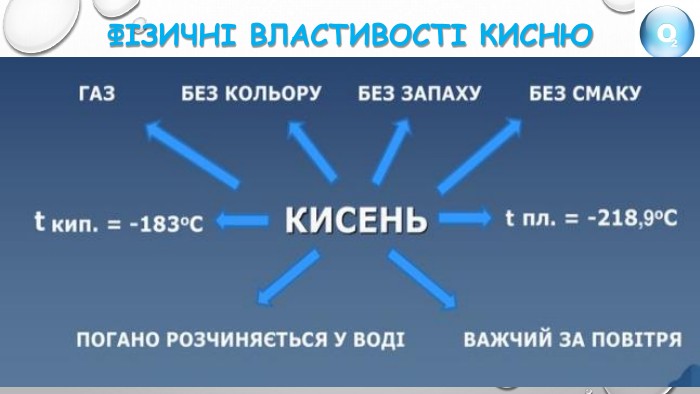
Хімічний елемент – проста речовина{5 C22544 A-7 EE6-4342-B048-85 BDC9 FD1 C3 A}Оксиген. Кисень. Хімічний символ ОХімічна формула О2 Порядковий номер 8 Тип речовини молекулярна. Відносна атомна маса 16 Відносна молекулярна маса 32 Період 2 Фізичні властивостіГрупа VIКолір безбарвний. Кількість електронів - 8 Запах без запаху. Заряд ядра + 8 Смак без смаку. Валентність ІІАгрегатний стан газуватий. Характер неметал. Tкип -183 Прості речовини. О2, О3 Tпл -218
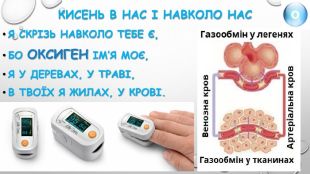
Кисень та озон. Хімічні елементи у вільному стані існують у формі простих речовин. Так, елемент Оксиген утворює дві прості речовини — кисень О2 та озон О3. Обидві прості речовини утворені одним і тим самим хімічним елементом, а властивості у них різні. Отже, кисень і озон — алотропні форми елемента Оксигену. Алотропія зумовлена різною кількістю атомів Оксигену в молекулах речовин.
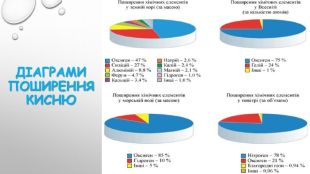
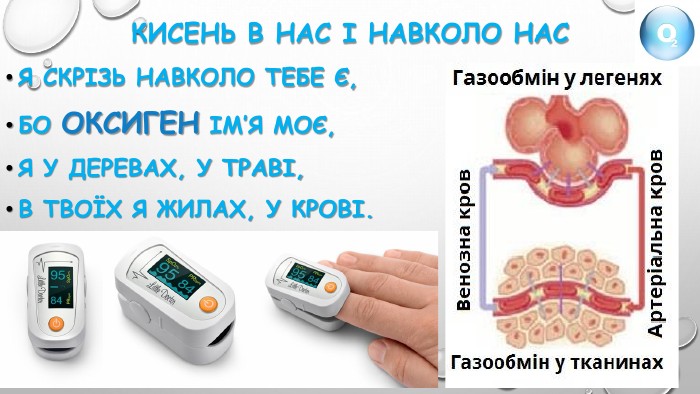
Складіть речення, вставивши замість крапок слова «Оксиген», «кисень», «озон»1) … - проста речовина2) Вода утворена Гідрогеном і …3) Молекула… складається із двох атомів ….4) У результаті фотосинтезу рослини поглинають вуглекислий газ і виділяють …5) Найбільший уміст … у гірських породах і мінералах6) У воді розчиняється погано …7) В акваріумі риби дихають …, розчиненим у воді8) … – газ без смаку і запаху9) … – захищає живі організми від згубного ультрафіолетового проміння10) … підтримує горіння11) … займає 1/5 повітря12) Життєвим газом називають …
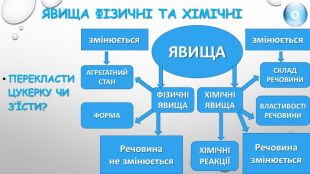
Графічний диктант (+ чи -) 1. Під час фізичних явищ склад речовини не змінюється.2. Хімічні явища супроводжуються руйнуванням одних молекул і утворенням інших.3. Під час хімічних явищ змінюється агрегатний стан речовини.4. Хімічні явища ще називають хімічними реакціями. 5. Під час хімічних явищ атоми елементів зберігаються.6. Зміни, що відбуваються із перегрупуванням атомів і утворенням нових речовин називають хімічними перетвореннями.7. Розчинення цукру у воді – хімічне явище.8. Утворення інею на деревах – фізичне явище.9. Виділення тепла і свічення - ознака хімічного явища.10. Утворення білкової піни – фізичне явище.11. Утворення суміші тирси і залізних ошурок – хімічне явище.12. Хімічні явища завжди супроводжуються фізичними.
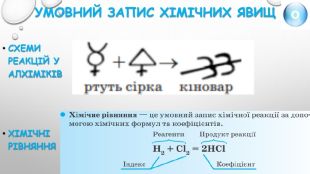
Складіть рівняння реакцій за поданими схемами {5 C22544 A-7 EE6-4342-B048-85 BDC9 FD1 C3 A}а) P + O2 → P2 O5 Na + Br2 → Na. Br. Ba + O2 → Ba. O H2 + S → H2 SAl + Cl2 → Al. Cl3 Al + Br2 → Al. Br3 Al + O2 → Al2 O3 Cu + O2 → Cu. Oб) Zn + O2 → Zn. OZn + Cl2 → Zn. Cl2 H2 O → H2 + O2 K + Cl2 → KCl. Fe + Cl2 → Fe. Cl2 K + І2 → KІLi + O2 → Li2 OAl + Br2 → Al. Br3в) Mg + O2 → Mg. OCu + S → Cu. SCa. CO3 → Ca. O + CO2 Mg + HCl → Mg. Cl2 + H2 Fe2 O3 + Al → Al2 O3 + Fe. Na + S → Na2 SAl + S → Al2 S3 Na + O2 → Na2 O
-
 Воронівська Наталья Гуріївна 25.02.2023 в 16:16Дякую!Загальна:5.0Структурованість5.0Оригінальність викладу5.0Відповідність темі5.0
Воронівська Наталья Гуріївна 25.02.2023 в 16:16Дякую!Загальна:5.0Структурованість5.0Оригінальність викладу5.0Відповідність темі5.0


про публікацію авторської розробки
Додати розробку