Урок"Контроль знань: Оксиди. Кислоти."
Усний залік (теоретичні питання)
Оксиди. Кислоти.
- Дайте визначення і наведіть приклади оксидів.
- Дайте визначення і наведіть приклади основ.
- Дайте визначення і наведіть приклади кислот.
- Дайте визначення і наведіть приклади солей.
- Назвіть відому класифікацію оксидів. Наведіть приклади оксидів кожної групи.
- Наведіть приклади оксидів металів (не менше 10) і назвіть їх.
- Наведіть приклади оксидів неметалів (не менше 8) і назвіть їх.
- Наведіть приклади (не менше 10) оксидів елементів зі сталою валентністю.
- З переліку формул: CuO, H2O, H2S, NaOH, Fe2O3, CaS, CO2, Mn2O7, CH4, CO, K2O, P2O5 – випишіть формули: а) основних оксидів; б) кислотних оксидів.
- Складіть формули кислот, що відповідають таким оксидам: P2O5, SO3, CO2.
- Складіть формули і назвіть оксиди таких елементів: Кальцію, Магнію, Плюмбуму, Хрому (VI), Карбону (IV), Сульфуру (VI). Які з них належать до основних? Складіть формули основ, що відповідають цим оксидам.
- Як класифікують кислоти? Наведіть приклади кожної групи.
- Для кислот: нітратної, силікатної, сульфідної, хлоридної, карбонатної, ортофосфатної – вкажіть: а) формули; б) валентність кислотних залишків;
в) назви солей, які вони утворюють.
- Перелічіть хімічні властивості кислот. Напишіть відповідні рівняння реакцій.
- Як можна добути карбонатну кислоту двома способами? Напишіть рівняння реакцій.
- Як класифікують основи? Наведіть конкретні приклади.
- Порівняйте властивості лугів і нерозчинних у воді основ.
- Як можна добути натрій гідроксид? Напишіть рівняння реакцій.
- До якого класу неорганічних сполук належать такі речовини: FeCl2, K2S, Na2CO3, Ca3(PO4)2, AlBr3? Назвіть їх.
- Складіть формули карбонату, фосфату, нітрату, хлориду: а) Натрію;
б) Феруму (II); Хрому (III).
- Як можна добути натрій карбонат ( не менше 4 – х способів). Напишіть відповідні рівняння реакцій.
- Що таке реакція нейтралізації?
- Який з наведених оксидів є найпоширенішим у природі: CO2, CaO, H2O, SO2? Назвіть його.
- До якого класу належать P2O5?
- CаO – це сіль чи оксид? Назвіть речовину.
Оксиди. Кислоти
Письмовий залік ( задачі і вправи)
- Обчисліть об’єм водню (н.у.), що виділяється при взаємодії 0,6 моль хлоридної кислоти з достатньою кількістю магнію.
- Обчисліть об’єм газу (н.у.),що виділяється при взаємодії алюмінію масою 2,7г з достатньою кількістю сульфатної кислоти.
- При взаємодії алюмінію з хлоридною кислотою виділилося 6,72л водню (н.у.). Яка маса хлоридної кислоти прореагувала?
- Який об’єм кисню (н.у.) прореагує з кальцієм масою 8г?
- Яка маса натрію може прореагувати з водою масою 36г?
- При взаємодії калію з водою утворилося 11,2г калій гідроксиду. Який об’єм водню (н.у.) виділився при цьому?
- Яка кількість речовини солі Ферум (III) сульфату утворюється при взаємодії 490г сульфатної кислоти з Ферум (III) оксидом.
- Який об’єм водню можна добути при взаємодії 4 моль кальцію з ортофасфатною кислотою?
- Скільки грамів магнію може прореагувати з 0,5 моль сульфатної кислоти?
- Який об’єм водню можна добути (н.у.), якщо подіяти хлоридною кислотою на цинк кількістю речовини 5 моль?
- Скільки грамів натрію прореагує з водою, якщо внаслідок реакції утворюється водень об’ємом 11,2л (н.у.)?
- Яка маса нітратної кислоти взаємодіє з оксидом кальцію масою 560г?
- При взаємодії 400г кальцію з водою виділяється водень. Обчисліть його об’єм (н.у.).
- При взаємодії 2 моль їдкого натрію з сульфатною кислотою утворюється натрій сульфат. Яка маса солі утворюється?
- З якими із зазначених речовин реагуватиме вода: мідь, калій оксид, кальцій, натрій, магній гідроксид, карбон (IV) оксид? Напишіть відповідні рівняння реакцій.
- Є речовини: силіцій (IV) оксид, вода, натрій, кальцій оксид, фосфор (V) оксид, калій гідроксид. Які з цих речовин можуть взаємодіяти між собою? Напишіть відповідні рівняння реакцій.
- З якими з перелічених речовин реагуватиме хлоридна кислота: мідь, гідраргірум (II)оксид, натрій карбонат, магній, кальцій гідроксид, купрум (II) гідроксид? Напишіть рівняння відповідних реакцій.
- Закінчіть рівняння можливих реакцій, вкажіть типи реакцій, назвіть утворені речовини: а) CuO + HCl →; ґ) SO3 + H2O →;
б) Ba + H2O →; д) SO3 + Ca(OH)2 →;
в) CaO + CO2 →; е) FeO + H2O →;
г) KOH + SO2 →; є) CO2 + MgO →;
- Напишіть формули кислот, що відповідають таким оксидам: CO2, P2O5, CrO3, N2O5, SiO2.
- Складіть рівняння можливих реакцій, назвіть утворені речовини.
а) магній + сульфатна кислота →; б) натрій оксид + нітратна кислота →;
в) алюміній гідроксид + хлоридна кислота →; г) залізо + ортофосфатна кислота →;
- Складіть рівняння реакцій, за допомогою яких можна здійснити перетворення:
а)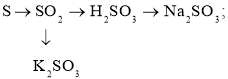 б)
б)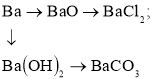
Тематичний контроль
Оксиди. Кислоти
I варіант
- З яких з перелічених речовин реагує калій гідроксид? Літій карбонат, сульфатна кислота, магній, карбон (IV) оксид, барій сульфат, купрум (II) сульфат. Напишіть рівняння реакцій.
- Здійсніть перетворення: H2 → HCl → ZnCl2 → AgCl. Напишіть рівняння реакцій. Вкажіть типи хімічних реакцій.
- Який об’єм водню (н.у.) можна добути під час взаємодії заліза масою 7г з сульфатною кислотою?
- Є такі речовини: натрій хлорид, хлоридна кислота і вода. Як розпізнати ці речовини? Напишіть відповідні рівняння реакцій.
II варіант
- З яких з перелічених речовин реагує сульфатна кислота? Їдкий калій, залізо, мідь, натрій гідроксид, кальцій карбонат, магній оксид, фосфор (V) оксид. Напишіть рівняння реакцій.
- Здійсніть перетворення: Cu → CuO → CuCl2 → Cu(OH)2 → CuO → CuSO4.
- Скільки грамів калію прореагує з водою, якщо при цьому утворюється водень об’ємом 11,2л (н.у.)?
- Як розпізнати речовини: натрій гідроксид і сульфат натрію? Напишіть рівняння реакцій.
III варіант
- Закінчить рівняння можливих реакцій.
а) Cu + HCl →; б) MgCO3 + HCl →;
в) Ca + H2O →; ґ) H2SO4 + CaO →.
д) CO2 + H2O →.
- Внаслідок нейтралізації нітратною кислотою їдкого калію кількістю речовини 2 моль утворюється калій нітрат, зайти його масу?
- Напишіть рівняння реакцій, за допомогою яких можна здійснити перетворення:
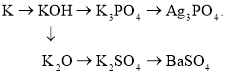
- Як двома способами добути натрій гідроксид? Напишіть рівняння реакцій.
IV варіант
- Закінчить рівняння можливих реакцій.
а) Mg + HCl →; г) Hg + HCl →;
б) ZnO + HNO3 →; ґ) H2O + SO3 →.
в) Ba + H2O →.
- При взаємодії сульфатної кислоти кількістю речовини 0,2 моль з кальцій гідроксидом утворюється сіль, знайти її кількість?
- Напишіть рівняння реакцій, за допомогою яких можна здійснити перетворення:
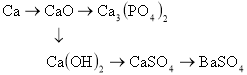
- Як двома способами можна добути хлоридну кислоту? Напишіть рівняння відповідних реакцій.
V варіант (полегшений)
- Закінчить рівняння реакцій.
а) H2O + P2O5 →;
б) K2O + H2O →;
в) NaOH + HCl →.
- З якими речовинами реагує хлоридна кислота?
а) MgO;
б) H2SO4;
в) NaOH;
г) CuO;
д) K;
є) Cu.
- З наведеного переліку речовин виберіть формули оксидів та назвіть їх.
KOH, CuO, CO2, H2S, Na2CO3, Ca(OH)2, NO2, NaNO3, H2O
VI варіант (полегшений)
- Закінчить рівняння реакцій:
а) H2O + SO2 →;
б) Na2O + H2O →;
в) H2O + Ca →.
- З якими речовинами реагує натрій гідроксид?
а) сульфатна кислота;
б) калій гідроксид;
в) вода;
г) купрум (II) сульфат;
ґ) магній.
- З наведеного переліку речовин виберіть формули кислот і назвіть їх.
HCl, H2O, NH3, CuS, H2S, H2SO4, HNO3, NaNO3.


про публікацію авторської розробки
Додати розробку
