Урок "Кристалічні гратки"
Тема: «Кристалічні ґратки. Атомні, молекулярні та йонні кристали. Залежність фізичних властивостей речовин від типів кристалічних ґратки.»
Мета уроку: формування компетентностей: предметної хімічної (з’ясувати поняття «кристалічні ґратки»; ознайомити учнів з типами кристалічних ґраток (атомні, молекулярні, йонні); розкрити зв'язок між типом кристалічних ґраток і фізичними властивостями речовин, визначити залежність властивостей речовин від їхньої будови; сформувати алгоритмічні прийоми розв’язування хімічних задач та евристичні способи пошуку розв’язків практичних життєвих проблем; сформувати й розвинути в учнів експериментальні вміння й дослідницькі навички, уміння описувати й оцінювати результати спостережень, планувати й проводити досліди та експериментальні дослідження, здійснювати вимірювання хімічних величин, робити узагальнення й висновки; розкрити роль хімічного знання в житті людини, суспільному виробництві й техніці, сутність наукового пізнання засобами хімії, сприяти розвитку інтересу школярів до хімії; спонукати учнів критично мислити, застосовувати набуті знання в практичній діяльності; використання наукового знання в життєдіяльності людини); ключових: математична компетентність (розв'язування розрахункових та графічних задач); уміння вчитися (здійснювати самостійну діяльність; самостійно добирати необхідні знання й способи діяльності для виконання навчальних завдань; використовувати інформацію з різних джерел); соціальна (самореалізуватися до виконання завдань у групі); загальнокультурна (адаптуватися у мовному середовищі шляхом активної участі у спілкуванні); інформаційно-комунікаційна (уміння використовувати інформаційно-комунікаційні технології, електронні освітні ресурси та відповідні засоби для виконання творчих завдань, аналізувати інформацію в електронному вигляді); здоров’язбережувальна компетентність ( дбайливе ставлення до власного здоров’я та здоров’я інших людей). Розвивати вміння здійснювати розумові дії, операції різних рівнів складності; формувати наполегливість та старанність у виконанні завдань, охайність у записах, ціннісне ставлення до використання часу.
Цільові завдання: учень (учениця):
називає типи кристалічних ґраток;
наводить приклади сполук із атомними, молекулярними та йонними кристалічними ґратками;
характеризує особливості кристалічної будови речовин з різними видами хімічного зв'язку;
прогнозує фізичні властивості та практичне використання речовин залежно типу кристалічних ґраток;
обґрунтовує фізичні властивості речовин залежно від типів кристалічних ґраток;
робить висновки про тип кристалічних ґраток речовин на основі виду хімічного зв’язку в них.
Засоби та обладнання: підручник (О.В.Григорович«Хімія» підручник для 8 класу загальноосвітніх навчальних закладів «Ранок» 2016); періодична система хімічних елементів, таблиця розчинності.
ХІД УРОКУ
І. ОРГАНІЗАЦІЙНИЙ МОМЕНТ ( привітання, організація класу, перевірка присутності учнів).
ІІ. АКТУАЛІЗАЦІЯ ОПОРНИХ ЗНАНЬ
Фронтальна бесіда
1.Що ми називаємо хімічним зв’язком?
2. Який вид хімічного зв'язку називається ковалентним та йонним?
3. Які частинки називаються йонами? Як вони утворюються?
4. Наведіть приклади речовин з ковалентним полярним, ковалентним неполярним, йонним зв'язком. ( Робота біля дошки)
ІІІ. МОТИВАЦІЯ НАВЧАЛЬНОЇ ДІЯЛЬНОСТІ
На попередніх уроках ми розібрали типи хімічного зв’язку. А як ви гадаєте, чи буде тип зв’язку впливати на властивості речовин? Сьогодні на уроці ми ознайомимося із залежністю властивостей речовин від їхньої будови, навчимося передбачати властивості речовин залежно від виду зв’язку та типу кристалічної ґратки.
ІV. ВИВЧЕННЯ НОВОГО МАТЕРІАЛУ
Будова твердих речовин
Більшість речовин перебувають у твердому агрегатному стані. Тверді речовини різноманітні за фізичними властивостями: мають різний колір, можуть бути міцними чи крихкими, можуть проводити електричний струм, плавитися майже за кімнатної температури або дуже великої. Більшість фізичних властивостей речовин зумовлені їхньою внутрішньою будовою.
За внутрішньою будовою й фізичними властивостями розрізняють два стани твердих речовин — аморфний і кристалічний. У кристалічних речовинах частинки, з яких побудовані кристали, розміщені в просторі в певному чіткому порядку Структурні одиниці в кристалічних речовинах утворюють правильні геометричні фігури. Аморфні речовини не мають чіткої просторової структури, а утворені з невпорядкованих частинок (атомів чи молекул). За внутрішньою будовою вони нагадують рідини, тільки не можуть текти.
На відміну від кристалічних речовин, що мають певну температуру плавлення, аморфні речовини плавляться в широкому інтервалі температур. Під час нагрівання вони поступово розм’якшуються і, нарешті, стають рідкими. Аморфним речовинам, як і рідинам, можна надати будь-якої форми.
Класифікація кристалічних граток
Кристалічні ґратки.– це розташування у просторі атомів, молекул та йонів у певному порядку. (Демонстрація «Моделі кристалічних ґраток)».
Типи кристалічних ґраток:
- Молекулярні;
- Йонні;
- Атомні.
Особливості молекулярних ґраток.

- У вузлах молекулярних кристалічних ґраток розташовані молекули, що зв’язані між собою слабкими міжмолекулярними силами.
- Молекулярні кристалічні ґратки властиві речовинам тільки з ковалентними зв’язками.
- Слабка міжмолекулярна взаємодія і тому їх легко зруйнувати, тому речовини з молекулярними ґратками є крихкими й мають невеликі значення температур плавлення і кипіння.
Отже, речовини з молекулярними ґратками є леткими, завдяки чому деякі з них мають характерний запах. Можна навіть стверджувати, що якщо речовина має запах, то це речовина молекулярної будови. Молекулярні речовини здатні розчинятися. Деякі з них розчиняються у воді, інші — в органічних розчинниках. Молекули не містять вільних носіїв електричного заряду, тому ані в рідкому, ані у твердому стані молекулярні речовини електричний струм зазвичай не проводять.
Особливості атомних ґраток.
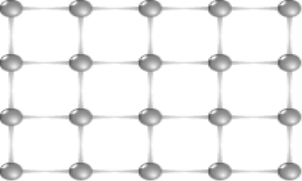
- Атомні кристали мають ґратки, утворені з атомів, що сполучені один з одним міцними ковалентними зв’язками.
- Мають дуже високі температури плавлення й кипіння. Вони нерозчинні у воді та в інших розчинниках.
- Дуже тверді, непластичні й некрихкі.
Особливості йонних ґраток.

- У вузлах йонних кристалічних ґраток розташовані йони. Різнойменні йони, з яких складаються йонні кристали, утримуються разом силами електростатичного притягання. Йонні кристалічні ґратки характерні для речовин з йонним зв’язком.
- Тверді, а плавляться і киплять лише в разі сильного нагрівання
- Нелеткі, тому не мають запаху.
- У твердому стані йонні сполуки не проводять електричний струм, оскільки всі йони жорстко закріплені на певному місці. Але якщо нагріти й розплавити такі речовини або розчинити у воді, то всі йони стають рухливими, і тому розплави та розчини йонних сполук добре проводять електричний струм.
V. ЗАКРІПЛЕННЯ ВИВЧЕНОГО МАТЕРІАЛУ.
Визначити тип кристалічних граток хімічних сполук: Са, О2, SO3, HCl, Н2О, І2, NaCl.
Інструкція з визначення типу кристалічної гратки
Визначити до якої групи відноситься дана речовина:
-
Проста речовина – визначити метал чи неметал:
- Ме – мають металічну кристалічну гратку;
- неМе – мають молекулярну кристалічну гратку;
- винятки – деякі неМе мають атомну кристалічну гратку.
-
Складна речовина – визначити клас речовини:
- МехОу – йонну кристалічну гратку;
- неМехОу – молекулярну кристалічну гратку;
- Ме(ОН)х – йонну кристалічну гратку;
- НхAn – йонну кристалічну гратку;
- MeхAnу – йонну кристалічну гратку.
VI. ПІДБИТТЯ ПІДСУМКІВ УРОКУ
Сьогодні на уроці ми ознайомилися з різними видами кристалічних ґраток і з’ясували, що вид зв’язку в речовинах тісно пов’язаний з їхньою будовою — типом кристалічної ґратки.
VII. ДОМАШНЄ ЗАВДАННЯ
Параграф 23 до підручника О.В.Григорович. Скласти порівняльну таблицю кристалічних граток в зошиті.


про публікацію авторської розробки
Додати розробку
