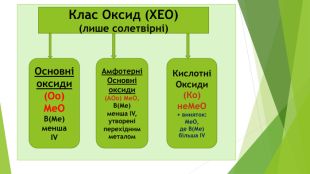
Урок на тему: "Класифікація оксидів та їх властивості"


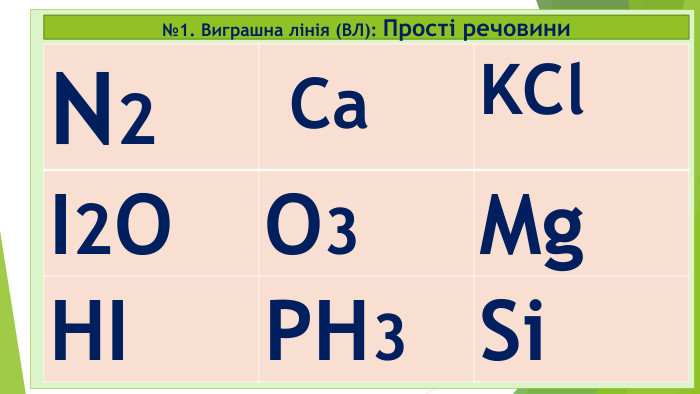
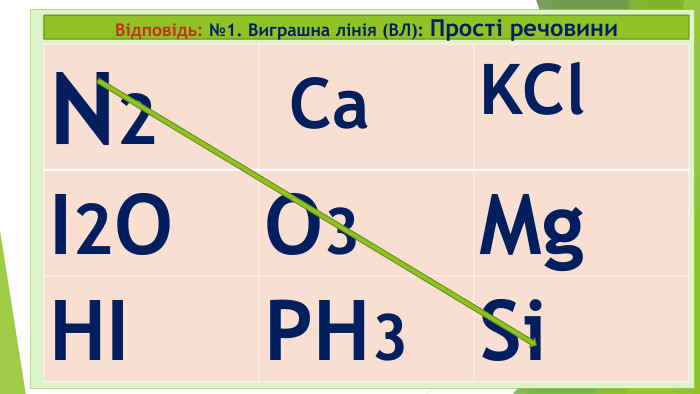
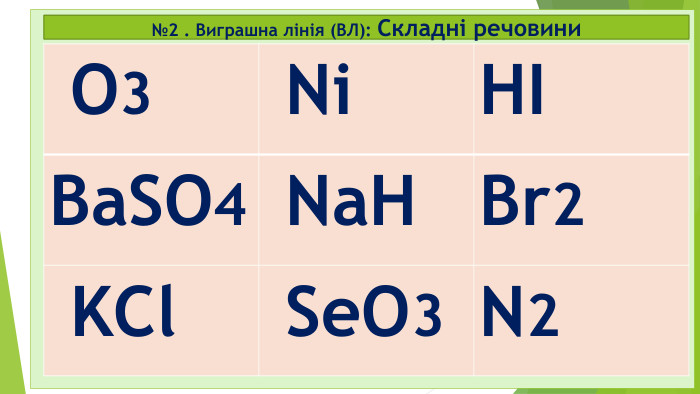






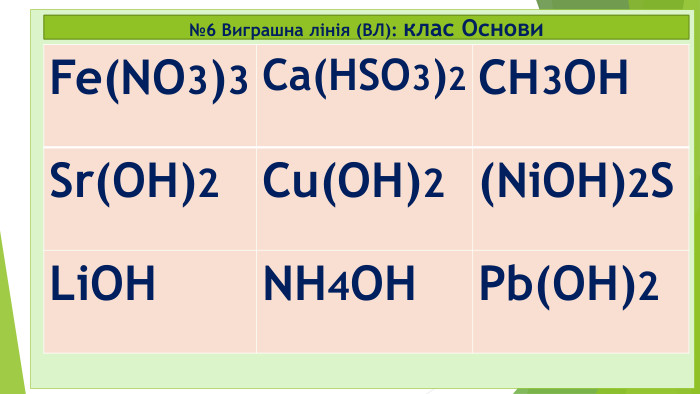

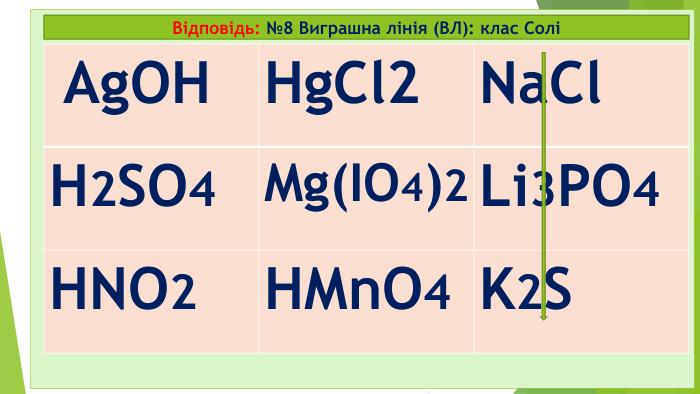






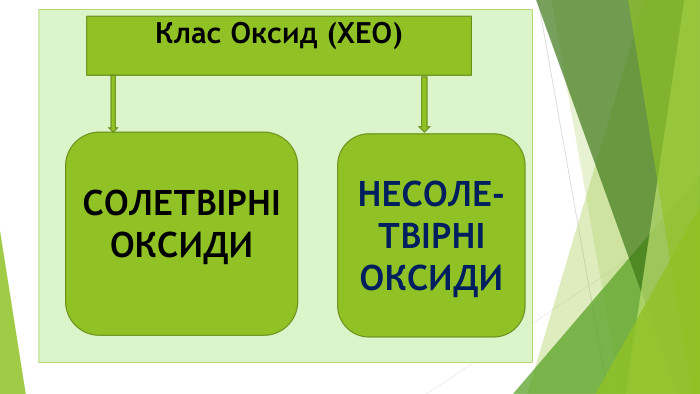



























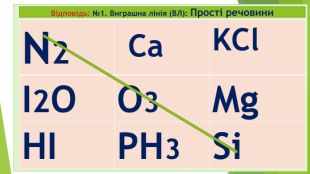
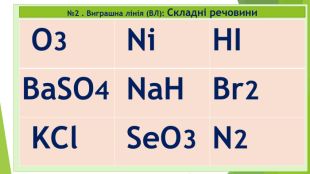
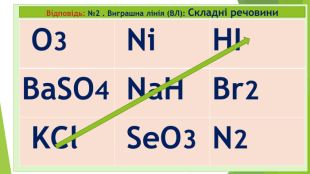
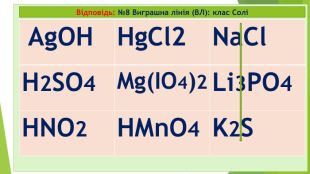
Діти! А чи любите ви таємниці? А наукові таємниці? А чи знаєте, що в перекладі з єгипетської хімія – це «хем» чорний, «таємничий»? А у вільному перекладі хімія - це просто «хамове ремесло»? Хімія – це наука про що? Які бувають речовини? Які речовини поділяються на дві групи? Які є класи простих речовин? На які класи поділяються складні мінеральні чи неорганічні сполуки?
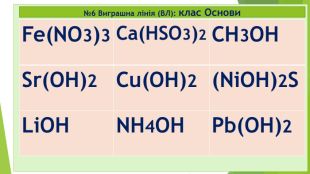
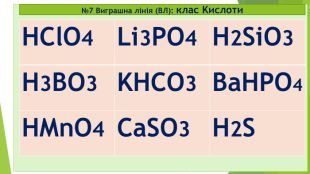
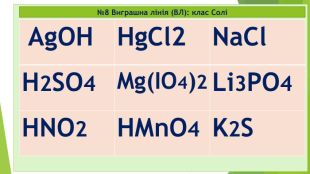
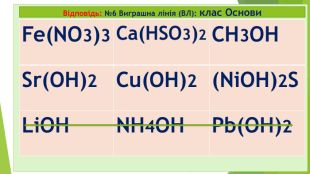
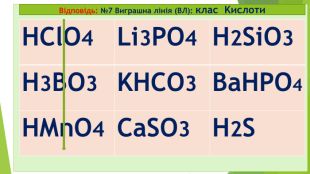
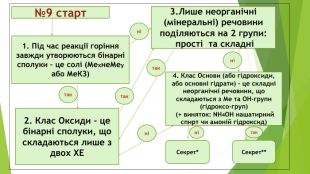
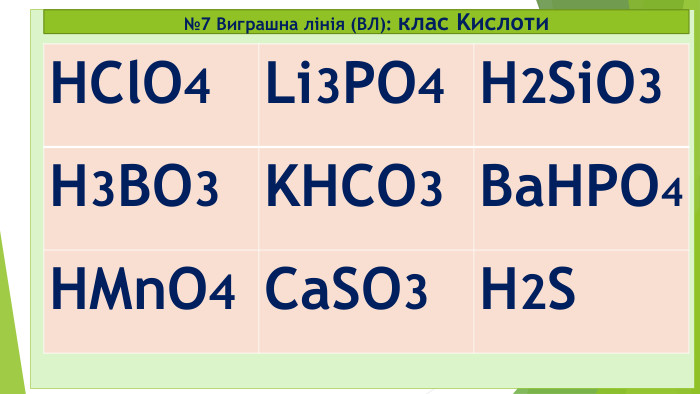
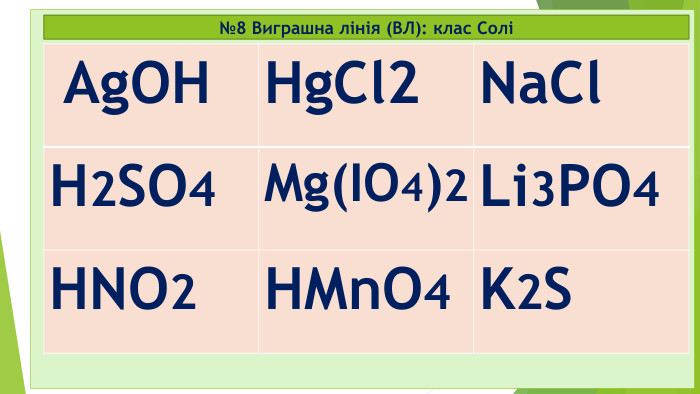
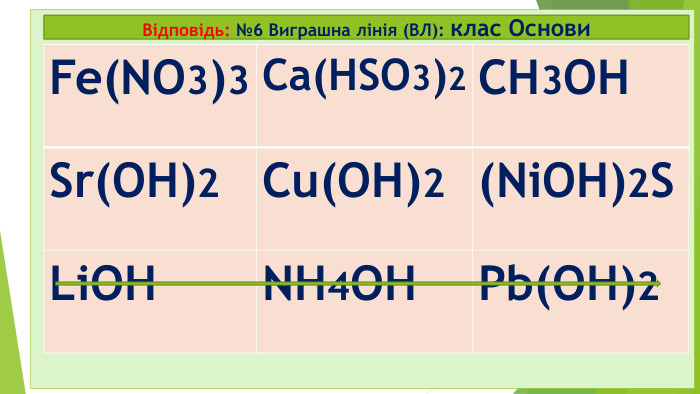
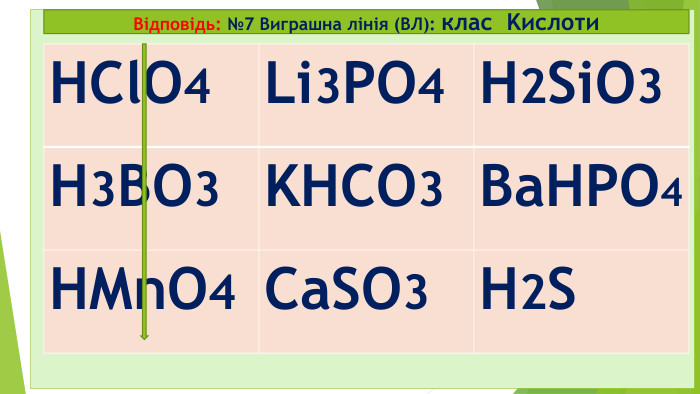
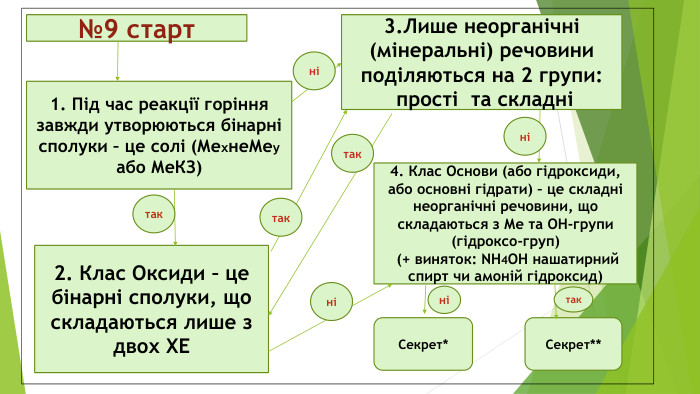
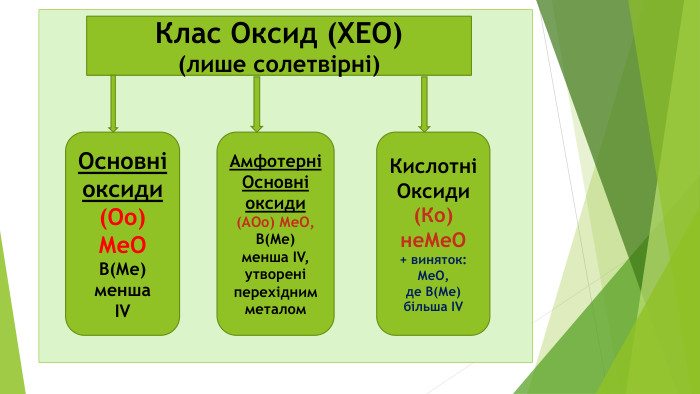
№9 старт 2. Клас Оксиди – це бінарні сполуки, що складаються лише з двох ХЕ 1. Під час реакції горіння завжди утворюються бінарні сполуки – це солі (МехнеМеу або МеКЗ) 3.Лише неорганічні (мінеральні) речовини поділяються на 2 групи: прості та складні 4. Клас Основи (або гідроксиди, або основні гідрати) – це складні неорганічні речовини, що складаються з Ме та ОН-групи (гідроксо-груп) (+ виняток: NH4OH нашатирний спирт чи амоній гідроксид) Секрет* Секрет** так так так ні ні ні ні так
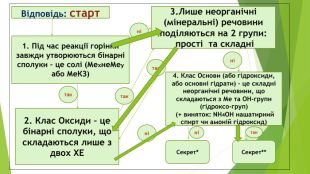
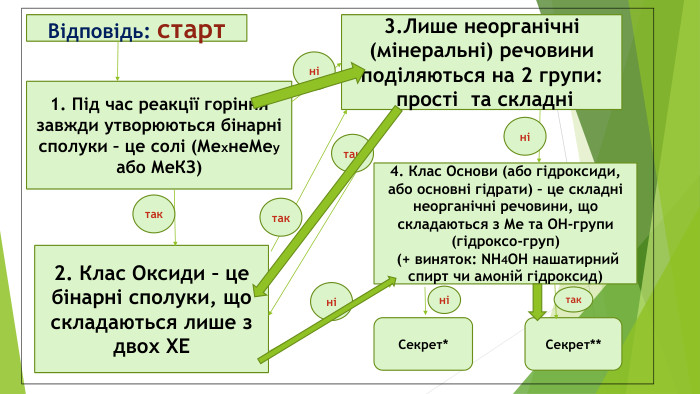
Відповідь: старт 2. Клас Оксиди – це бінарні сполуки, що складаються лише з двох ХЕ 1. Під час реакції горіння завжди утворюються бінарні сполуки – це солі (МехнеМеу або МеКЗ) 3.Лише неорганічні (мінеральні) речовини поділяються на 2 групи: прості та складні 4. Клас Основи (або гідроксиди, або основні гідрати) – це складні неорганічні речовини, що складаються з Ме та ОН-групи (гідроксо-груп) (+ виняток: NH4OH нашатирний спирт чи амоній гідроксид) Секрет* Секрет** так так так ні ні ні ні так
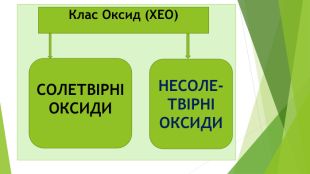
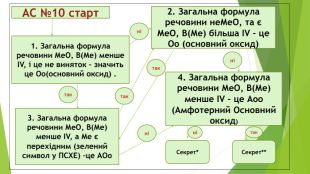
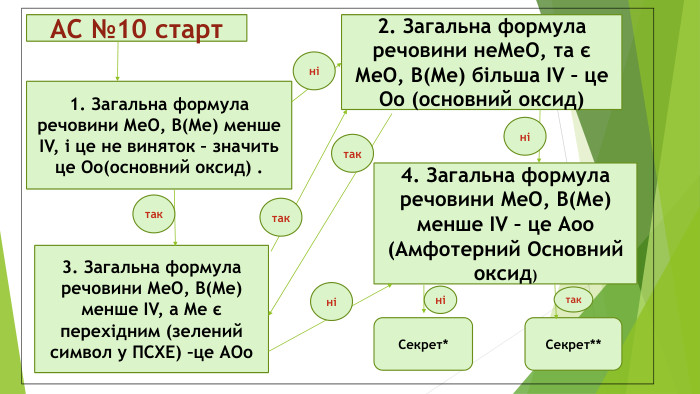
АС №10 старт 3. Загальна формула речовини МеО, В(Ме) менше ІV, а Ме є перехідним (зелений символ у ПСХЕ) –це АОо 1. Загальна формула речовини МеО, В(Ме) менше ІV, і це не виняток – значить це Оо(основний оксид) . 2. Загальна формула речовини неМеО, та є МеО, В(Ме) більша ІV – це Оо (основний оксид) 4. Загальна формула речовини МеО, В(Ме) менше ІV – це Аоо (Амфотерний Основний оксид) Секрет* Секрет** так так так ні ні ні ні так
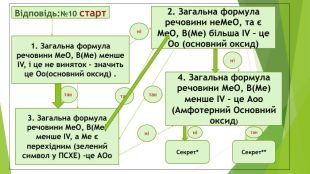
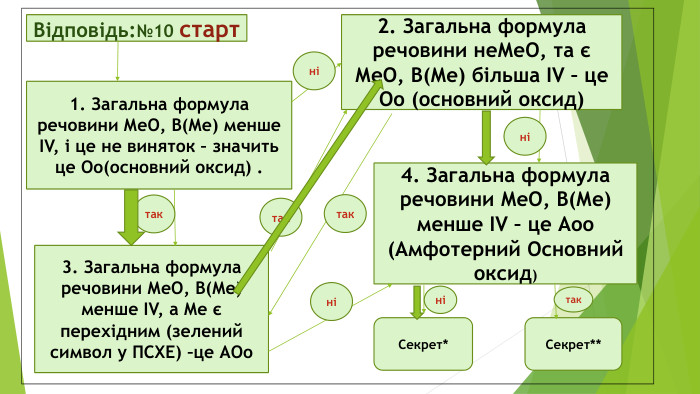
Відповідь:№10 старт 3. Загальна формула речовини МеО, В(Ме) менше ІV, а Ме є перехідним (зелений символ у ПСХЕ) –це АОо 1. Загальна формула речовини МеО, В(Ме) менше ІV, і це не виняток – значить це Оо(основний оксид) . 2. Загальна формула речовини неМеО, та є МеО, В(Ме) більша ІV – це Оо (основний оксид) 4. Загальна формула речовини МеО, В(Ме) менше ІV – це Аоо (Амфотерний Основний оксид) Секрет* Секрет** так так так ні ні ні ні так


про публікацію авторської розробки
Додати розробку