Урок на тему "Вода, склад її молекули, фізичні властивості та поширеність в природі" ( із застосуванням технології "критичного мислення")
Данний урок із застосуванням технології "критичного мислення", який дозволяє розвивати інтерес учнів до предмету, активізувати їх пізнавальну і творчу діяльність, вміння аналізувати ситуацію, обговорювати проблему, ставити чіткі запитання і давати на них змістовні відповіді.
Мета уроку: збагатити знання учнів про воду, як найпоширенішу речовину на Землі, повторити фізичні властивості води, дати поняття про її структуру та водневий зв'язок, показати поширеність води у природі, скласти таблицю «аномальних» властивостей води.
Урок на тему:
«Вода.Склад молекули, фізичні властивості, поширеність в природі»
(із застосуванням технології «критичного мислення»)
.
Горова Юлія
Олександрівна
Вчитель біології та хімії
Микільської на Дніпрі ЗОШ І-ІІІ ст.
Солонянського району
2018
Слайд 2 Тема: Вода. Склад молекули, фізичні властивості, поширеність в природі
(із застосуванням технології «критичного мислення»)
Слайд 3 Мета:
- освітня: збагатити знання учнів про воду, як найпоширенішу речовину на Землі, повторити фізичні властивості води, дати поняття про її структуру та водневий зв'язок, показати поширеність води у природі, скласти таблицю «аномальних» властивостей води.
- розвиваюча: розвивати інтерес учнів до предмету, активізувати їх пізнавальну і творчу діяльність, вміння аналізувати ситуацію, обговорювати проблему, ставити чіткі запитання і давати на них змістовні відповіді, аргументовано оцінювати діяльність на уроці.
Тип уроку: комбінований
Стратегії навчання: Асоціювання, Мозковий штурм, Запитання-відповіді, Знайди проблему.
Форми роботи: фронтальна, групова.
Прийоми навчання: розповідь, самоконтроль, закріплення набутих знань, проблемно-пошуковий.
Базові поняття: формула води структурна та молекулярна, фізичні і аномальні властивості води, водневий зв'язок.
Структура уроку:
1 етап. Розминка (3 хв.)
2 етап. Обґрунтування навчання (5 хв.)
3 етап. Актуалізація Виклик (7 хв.)
4 етап. Усвідомлення змісту (20 хв.)
5 етап. Рефлексія (8 хв.)
6 етап. Домашнє завдання (2 хв.)
Обладнання та матеріали: чорна коробка, вода, підручник, набір для складання кулестержневих молекул води, піпетки, копійки, 3 стакани, термос, скотч, відео фрагмент добування води, аудіозапис «шум води».
Хід уроку
І.Розминка
Слайд 1 Вчитель: У мене в ящику знаходиться речовина,про яку написані легенди і пісні,її вважають святою і живою,без неї неможливе життя. Її вивчають теоретики і експериментатори, хіміки, фізики, біологи. Кожен із нас зустрічається з нею повсякчасно. Вона в нас. Таємниці її ще не розкриті… (діти припускають що в чорному ящику).
ІІ. Обґрунтування навчання.
Вчитель: Ви здогадались яка тема нашого уроку?
Слайд 4 Вода…Якою вона буває?
(Стратегія «Асоціативний кущ»)
Оберемо ключове слово. Запишемо його посередині дошки, праворуч прикметники, з якими асоціюється слово вода, ліворуч – з якими іменниками
іній жива
 лід морська
лід морська
дощ свята
роса прісна
айсберг джерельна
сніг питна
річка цілюща
море таємнича
Чи багато ви знаєте про воду? Давайте перевіримо це на практиці
(застосування стратегії «Мозковий штурм»)
Слайд 5,6
- Яку частину поверхні планети Земля займає вода?
- Чому наша планета з космосу виглядає як блакитна куля?
- Що з’явилося першим? Вода чи Земля?
- Чи є вода всередині Землі?
- Вчені говорять, що весь океан – це одна гігантська молекула води. Чи так це?
- Чому вода рідина?
Підіб’ємо підсумок. Питань про властивості води можна задати багато, бо таємниці самої поширеної речовини в природі досі не розкриті. Можливо на сьогоднішньому уроці ми дамо відповіді на деякі з цих запитань.
Чи потрібно вам додаткова інформація про воду. І для чого? Діти відповідають
ІІІ.Актуалізація Виклик
Слайд 7
Що такий агрегатний стан? (Учні дають визначення)
Демонстрація: склянка з водою, кубики льоду, термос із окропом.
Діти, назвіть агрегатні стани води. (Рідина, лід, пара)
Чи має вода запах?
Якого вона кольору?
Користуючись підручником і довідником впишіть характеристики, які відображають фізичні властивості води ( працюють в парах):
- Температура кипіння ____________________________;
- Температура плавлення __________________________;
- Теплопровідність _______________________________;
- Колір _________________________________________;
- Запах _________________________________________;
- Смак __________________________________________;
- Електропровідність _____________________________;
- Агрегатні стани води ____________________________;
- Густина льоду при t нижче 0оС ____________________;
ІV. Усвідомлення змісту
А тепер послухайте казку:
Слайд 8 Таємниці джерельної води
У природному царстві хімічних елементів жили цар і цариця. І була у них донька Оксиген. Вона була ще та красуня і закохався в неї принц Гідроген. Але в чарівній книзі було записано, що коли вони доторкнуться один до одного – станеться велике лихо. До принцеси сватався зухвалий принц – Цинк, але Гідроген викликав його на бій і переміг. Оксиген кинулась в обійми Гідрогена. Спалахнув вогонь, пророцтво здійснилося. Але вони не загинули. На тому місці утворилась вода – веселий струмочок з кришталевою водою. І в дзюрчанні чистої води чується сміх принца і принцеси. Вони навіки разом.
(Демонстрація досліду «Взаємодія водню і кисню», віртуальна лабораторія)
Слайд 9 Запишемо хімічне рівняння утворення води: 2Н2 + O2 = 2Н2O
Над вивченням будови молекули води в кінці ХVІІІ ст. працював французький вчений Лавуаз’є. Він узяв два об’єми водню і один об’єм кисню, підпалив суміш і краплинка води заявила про своє народження «салютом».
Слайд 10 Формулу води знають усі, а яка просторова будова цієї молекули? Намалюємо її.
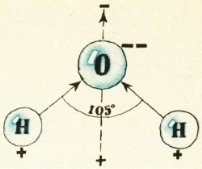
(Демонстрація кулестержневої моделі молекули води)
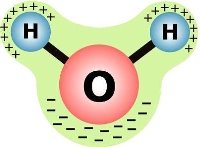
Слайд 11 Проблемне питання. Пам’ятаєте було питання «Чому вода – рідина?». (Відповіді учнів)
Учитель. Пояснюється це тим, що за звичайних умов молекули води існують не поодинці, а парами, трійками, квартетами, секстетами за рахунок водневих зв’язків. Інакше кажучи, вона являє собою газ, що створюється внаслідок кип’ятіння, коли зв’язки між молекулами води розриваються. Молекули води з’єднуються одна з одною за допомогою водневого зв’язку. Саме він зв’язує молекули води в димери, тримери, тетраметри і саму стійку структуру – гексамери.
Учням пропоную роботу в парах: зібрати кулестержневі моделі молекули води і з’єднати їх в димери скотчем так, як показано на дошці. Потім пропоную об’єднатися в групи по чотири, і зібрати тетраметри.
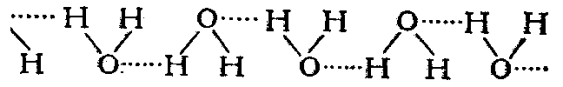
Зробіть висновки:
Що таке водневий зв’язок?
Які атоми він з’єднує?
Проблемне питання «Чому вода рідина?» - розв’язано!
Слайд 12 (шум води)
Фізкультхвилинка
Раз, два – всі пірнають.
Три, чотири – виринають.
П’ять, шість – на воді
Кріпнуть крильця молоді.
Сім, вісім – що є сили
Всі до берега поплили.
Дев’ять, десять – тихо сіли,
Щоб сусіда не заділи.
- Що активніше циркулює в наших організмах після фізкультхвилинок? (Кров)
- Яка хімічна речовина є основою крові? (Вода)
Слайд 13 «Аномальні» властивості води(Учні записують у зошити)
- Вода може «злипатися» сама із собою або з іншими речовинами
Демонстрація: налити склянку води з «верхом» – вода не розтікається.
Це має велике значення в житті рослин і тварин. Хто скаже, яке саме? (Думки учнів)
Учитель. Завдяки цій властивості коріння здатне всмоктувати вологу з ґрунту й подавати на висоту майже до 200 м (у найвищих деревах – евкаліпті, секвої та секвоядендроні), клопи-водоміри легко ковзають по дзеркалу водойм.
Майже всі речовини під час плавлення збільшуються в об’ємі, тому тонуть у власних розплавах. Що ж ми бачимо?
Демонстрація: кубик льоду кидаємо в склянку з водою.
Слайд 14 2. Лід же має більший об’єм, ніж вода, з якої він утворений, тому він плаває в ній. Відстань між молекулами води в кристалі більша, ніж у рідині.
Питання. Яке це має значення в природі? (Водойми не промерзають аж до дна, що забезпечує існування живих організмів у них, інакше життя на землі могло б не виникнути взагалі.)
Замерзанню води в клітинах перешкоджають такі процеси: скидання деревами листя восени, уміст речовин-антифризів, що знижують температуру замерзання.
Слайд 15 3. Густина води – найбільша за температури +4 °С. Під час охолодження густина води, як і інших речовин, збільшується, але тільки до +4 °С, а від +4 до 0 °С – зменшується.
Потім густина її знижується, і на поверхні водойми з’являється лід, що перешкоджає ще більшому охолодженню. Опускання холодної води на дно забезпечує постачання киснем глибоких шарів води, тому що внаслідок зниження температури розчинність газів у рідинах підвищується.
У зв’язку з цим спробуйте відповісти на запитання, чому в акваріум не можна заливати кип’ячену воду?(Учні висловлюють думки)
Учитель. Тому що в кип’яченій воді практично відсутній розчинений кисень, необхідний рибкам для дихання.
Слайд 16 4. Вода має високу теплоємність і низьку теплопровідність. Остудивши 1 м3 Н20 на І °С, можна нагріти 1000 м3 повітря на 3 °С. В 1 л води можна запасти в 330 разів більше тепла, ніж в 1 л повітря.
Ця властивість води дозволила сформувати на нашій планеті клімат, сприятливий для життя, тому що восени вода повільно остигає, зігріваючи повітря, а влітку й навесні повільно нагрівається, охолоджуючи його.
Слайд 17 5. У води надзвичайновисокаприхована теплота плавлення.
Ми вже відзначали, що вода в природі зустрічається у вигляді льодовиків.
Питання. Чим можна пояснити, що льодовики не тануть повністю?
(Думки учнів)
Учитель. Виявляється, для цього знадобилася б величезна кількість енергії, що неможливо.Наприклад, щоб розплавити 1 кг льоду, необхідно 79 ккал теплоти.Таким чином, це рятує нас від катастрофічних весняних повеней і дає ґрунтам можливість увібрати достатню кількість вологи на літо.
Слайд 18 6. За температури 0 °С вода перетворюється на лід
Чи справедливе це твердження? (Так, якщо йдеться про чисту воду, морська ж вода замерзає за температури –1,9 °С через домішки солей)
Висновок. Діти, я думаю, ви погодитеся з тим, що, якби вода не малі більшості аномальних властивостей, життя на планеті не було б таким різноманітним або не існувало б зовсім. У цьому еволюційне значення води.
V. Рефлексія (для опитування використовується програма Plickers)
Слайд 19 Хімічний диктант
1. Вода – це проста речовина. (Ні)
2. Молекула води складається з двох атомів Оксигену й одного атома Гідрогену. (Ні)
3. Вода – найпоширеніша речовина на планеті й займає площу в 3/4 поверхні землі. (Так)
4. Молекули води в рідкому стані розташовані групами. (Так)
5. Будь-яка вода замерзає за температури 0 °С. (Ні)
6. Густина води найбільша за температури 0 °С. (Ні, за температури
+4 °С)
7. Вода повільно остигає й повільно нагрівається. ( Так)
Слайд 20 (для опитування використовується програма Kahoot)
Екологічне лото

Слайд 21
VІ. Домашнє завдання
1. Опрацювати матеріал підручника § 25
2. Виконати завд.7, 11 ст.142-143.
3. Творче завдання: знайти загадки та цікавинки про воду або завд. 8 ст. 142.

про публікацію авторської розробки
Додати розробку
