Урок "Визначення валентності за формулами бінарних сполук"
07.11.2023 року
Урок №17
Тема «Визначення валентності за формулами бінарних сполук»
Мета: а) навчальна: формування знань учнів про валентність хімічних елементів та навчити складати формули хімічних сполук за їх валентністю і визначати валентність за формулами бінарних сполук;
б) виховна: виховати в учнів вміння уважно слухати вчителя, активно працювати на уроці;
в) розвивальна: розвинути в учнів увагу і зосередженість.
Тип уроку: поглиблення і систематизація знань.
Форми роботи: фронтальна бесіда, самостійна робота, робота з дидактичними картками.
Обладнання: підручник, робочий зошит, періодична система хімічних елементів Д.І.Менделєєва, картки.
Очікувані результати: учень визначає валентністю елементів за формулами бінарних сполук.
Хід уроку
І. Організаційний момент.
ІІ. Актуалізація опорних знань:
Фронтальна бесіда.
1. Що таке хімічна формула?
2. Який якісний і кількісний склад молекули К2О?
3. Що таке валентність?
4. Як поділяють валентність?
5. Правила складання формул бінарних сполук за валентністю.
Вправа «Перевір себе» (самостійна робота).
1. Напишіть формули сполук із Хлором, знаючи, що він одновалентний, елементів: Калій, Барій, Алюміній, Магній, Купрум(І), Хром (ІІІ), Гідроген.
2. Знаючи валентності елементів, складіть формули таких речовин:
|
ІІ |
IV I |
II |
II |
II I |
I |
I II |
|
Al S |
Si Cl |
Zn S |
Pb O |
Fe Cl |
K Cl |
Cu S |
|
I І |
V I |
III |
VI |
I I |
|
Na Cl |
P Cl |
N H |
W O |
Ag I |
ІІІ. Вивчення нового матеріалу.
Ми вже вивчили велентність, і знаємо, як можна вивести формулу сполуки по валентності. Вас вже можна назвати молодими хіміками. А для кращого засвоєння знань помандруємо в країну під назвою «Навпаки» і спробуємо, користуючись готовою формулою, визначати валентності елементів.
У формулах бінарних сполук сумарна валентність усіх атомів одного елемента повинна дорівнювати сумарній валентності атомів другого елемента.
Алгоритм визначення валентності.
1. Записати формулу сполуки.
2.Проставити відому валентність елемента.
3. Помножити валентність на кількість атомів даного елемента і розділити на кількість атомів другого елемента.
4. Дане число буде шуканою валентністю.
5. Записати валентність.
Наприклад, треба визначити валентність Алюмінію в алюміній оксиді, формула якого Аl2O3. Для цього записуємо формулу речовини і над хімічним символом Оксигену позначаємо римською цифрою його валентність (вона нам відома, завжди два):
![]()
Враховуючи число атомів Оксигену в сполуці, визначаємо сумарну валентність трьох атомів Оксигену, вона дорівнює шести (2 • 3 = 6). Ці шість одиниць валентності припадають на два атоми Алюмінію, значить, на один атом Алюмінію — три одиниці (6:2 = 3). Отже, Алюміній в оксиді Алюмінію тривалентний:
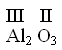
У формулах бінарних сполук сумарна валентність усіх атомів одного елемента завжди дорівнює сумарній валентності всіх атомів іншого елемента.
Наведемо ще один приклад. Визначити валентність Фосфору у фосфор(V) оксиді, формула якого Р2O5. Для цього записуємо формулу речовини і над хімічним символом Оксигену позначаємо римською цифрою його валентність (вона нам відома, завжди два):
![]()
Враховуючи число атомів Оксигену в сполуці, визначаємо сумарну валентність трьох атомів Оксигену, вона дорівнює десяти (2 • 5 = 10). Ці 10 одиниць валентності припадають на два атоми Фосфору. Значить, на один атом Фосфору — 5 одиниць (10:2 = 5). Отже, Фосфор в оксиді Фосфору п’ятивалентний:
![]()
Зв’язок між розміщенням елемента у періодичній системі та його валентністю.
Валентність елементів можна визначати за допомогою періодичної системи елементів. У періодичній системі елементи розташовані за групами. Номер групи, в якій міститься елемент, показує максимальне число хімічних зв'язків, що може утворити його атом. Тобто максимальна валентність дорівнює номеру групи. Проте, слід пам’ятати, що кожне правило має свої виключення. Те саме стосується й валентності. Наприклад, за періодичною системою валентність Оксигену VІ, а в дійсності ІІ.
Оксиди.
В назві речовин, утворених елементами із змінною валентністю, після назви цього елементу в дужках пишуть римську цифру, показуючу валентність даного елемента у цій сполуці.
СuO – купрум(ІІ) оксид;
Сu2O – купрум(І) оксид
FeCl2 – ферум(ІІ) хлорид
FeCl3 – ферум(ІІІ) хлорид
FеО – ферум(II) оксид
Fe2О3 – ферум(III) оксид
ІV. Узагальнення і систематизація знань.
Робота з картками:
- Визначити валентність елементів у сполуках з Гідрогеном:
HBr, H2S, PH3, HI, NH3.
- Визначити валентність елементів у сполуках з Оксигеном:
Na2O, CaO, SO2, P2O5, Al2O3, Cl2O7.
-
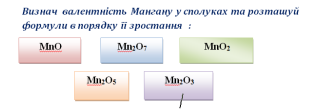
-

- Гра «Хрестики - нулики»:
Знайди виграшну лінію, на якій розташовані лише сполуки Оксигену з атомами хімічних елементів,що мають валентність:
валентність елемента - ІІ:
|
Cr 2O3 |
PbO2 |
СO |
|
FeО |
МgО |
СаО |
|
Li2O |
К2O |
Cl2O7 |
валентність елемента - ІІІ:
|
Fe2O3 |
PbO2 |
СO2 |
|
FeО |
АІ2O3 |
CrO3 |
|
Cl2O5 |
К2O |
Cr 2O3 |
валентність елемента - V:
|
Cr 2O3 |
Li2O |
Mn2O5 |
|
Fe2O3 |
As2O5 |
SO3 |
|
V2O5 |
PbO2 |
CІ 2O7 |
V. Підведення підсумків уроку.
VІ. Домашнє завдання. Опрацювати с.96, №109, №112.
 А Л Г О Р И Т М
А Л Г О Р И Т М
визначення валентності елемента
за формулами бінарних сполук
Що робити |
Приклад |
|
1. Записуємо формулу речовини |
P2O5 |
|
2. Над тим елементом, валентність якого відома, записуємо валентність римською цифрою |
ІІ P2O5 |
|
3.Знаходимо сумарну валентність всіх атомів того елемента, валентність якого відома ( валентність цього атома множимо на кількість його атомів) |
2х5=10 |
|
4. Десять одиниць валентності припадає на 2 атома Фосфору, значить на один атом - 5 |
10:2=5 |
|
5. Фосфор в цій сполуці п'ятивалентний |
V ІІ P2O5 |
|
ВИСНОВОК: У формулах сполук, що складаються з двох елементів, сума валентностей всіх атомів одного елемента дорівнює сумі валентностей всіх атомів іншого елемента! |
|

А Л Г О Р И Т М
визначення валентності елемента
за формулами бінарних сполук
Що робити |
Приклад |
|
1. Записуємо формулу речовини |
P2O5 |
|
2. Над тим елементом, валентність якого відома, записуємо валентність римською цифрою |
ІІ P2O5 |
|
3.Знаходимо сумарну валентність всіх атомів того елемента, валентність якого відома ( валентність цього атома множимо на кількість його атомів) |
2х5=10 |
|
4. Десять одиниць валентності припадає на 2 атома Фосфору, значить на один атом - 5 |
10:2=5 |
|
5. Фосфор в цій сполуці п'ятивалентний |
V ІІ P2O5 |
|
ВИСНОВОК: У формулах сполук, що складаються з двох елементів, сума валентностей всіх атомів одного елемента дорівнює сумі валентностей всіх атомів іншого елемента! |
|
______________________________________
1. Напишіть формули сполук із Хлором, знаючи, що він одновалентний, елементів: Калій, Барій, Алюміній, Магній, Купрум(І), Хром (ІІІ), Гідроген.
2. Знаючи валентності елементів, складіть формули таких речовин:
|
ІІ |
IV I |
II |
II |
II I |
I |
I II |
|
Al S |
Si Cl |
Zn S |
Pb O |
Fe Cl |
K Cl |
Cu S |
|
I І |
V I |
III |
VI |
I I |
|
Na Cl |
P Cl |
N H |
W O |
Ag I |
_______________________________________________
1. Напишіть формули сполук із Хлором, знаючи, що він одновалентний, елементів: Калій, Барій, Алюміній, Магній, Купрум(І), Хром (ІІІ), Гідроген.
2. Знаючи валентності елементів, складіть формули таких речовин:
|
ІІ |
IV I |
II |
II |
II I |
I |
I II |
|
Al S |
Si Cl |
Zn S |
Pb O |
Fe Cl |
K Cl |
Cu S |
|
I І |
V I |
III |
VI |
I I |
|
Na Cl |
P Cl |
N H |
W O |
Ag I |
_______________________________________________
1. Напишіть формули сполук із Хлором, знаючи, що він одновалентний, елементів: Калій, Барій, Алюміній, Магній, Купрум(І), Хром (ІІІ), Гідроген.
2. Знаючи валентності елементів, складіть формули таких речовин:
|
ІІ |
IV I |
II |
II |
II I |
I |
I II |
|
Al S |
Si Cl |
Zn S |
Pb O |
Fe Cl |
K Cl |
Cu S |
|
I І |
V I |
III |
VI |
I I |
|
Na Cl |
P Cl |
N H |
W O |
Ag I |


про публікацію авторської розробки
Додати розробку
