Урок "Якісні реакції на деякі йони"
Хімія 11 клас Дата __________
Тема: «Якісні реакції на деякі Йони»
Підготувала:
вчитель хімії
Соснівської філії КЗ
«Красно сільське НВО»
Орлик Тетяна Ігорівна
2019 р
11 клас Хімія Дата ________.
Тема: Якісні реакції на деякі йони.
Мета: продовжувати формувати в учнів знання з теми « якісні реакції»;
навчити проводити якісні реакції, визначати в розчинах катіони; Феруму(ІІ), Феруму(ІІІ) (осадженням їх лугами), Барію, амонію, а також силікат- і ортофосфат-аніони
Розвивати вміння досліджувати якісний склад речовин;
Виховувати самостійність під час виконання завдань.
Методи та прийоми: робота з таблицею, опорний текст, спілкування «питання-відповідь»,
Обладнання та матеріали:таблиця розчинності солей, основ та амфотерних гідроксидів, мультимедійна презентація, стрічки , фломастери.
Тип уроку: комбінований.
ХІД УРОКУ
I.Організаційний момент .
Вправа. Вітаю всіх, хто прийшов на урок, вітаю тих, що прийшли з хорошим настроєм, вітаю тих, хто підготував домашнє завдання і тих, хто не підготував. Вітаю тих, хто веселий і життєрадісний, тих, хто хмурий і зажурений. Вітаю всіх!
Вправа «Улюблений колір». У вас на партах находяться кольорові фломастери та паперові стрічки розфарбуйте стрічки фломастером свого улюбленого кольору та піднесіть вгору.
Яких кольорів більше?
II. Перевірка домашнього завдання.
На попередньому уроці ми вивчали поняття про кислотні та лужні ґрунти.
Вправа заповніть пропуски.
Грунти класифікують за величиною показника ___. (рН)
Величина показника рН грунтового розчину впливає на засвоюваність______
(макро-) та ____________ (мікроелементів) рослинами.
Рослини споживають аніони та катіони у певних пропорціях в обмін на
еквівалентну кількість йонів ____,____,______,_____ (Н+, ОН-,НСО3-, СО32-).
Надмірну кислотність грунту усувають _____(вапнуванням), а надмірну луж-
ність -________ (гіпсуванням).
2. Підпишіть компоненти
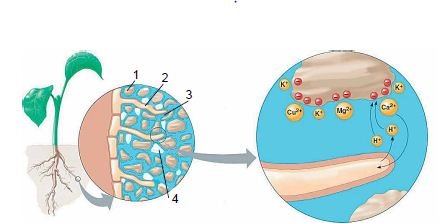
1._________________(Частинка грунту)
2.__________________(Кореневий волосок)
3.___________________(Вода)
4.__________________ (Пухирці повітря)
ІІІ. Актуалізація опорних знань.
На слайді зображені хімічні рівняння. Закінчіть їх.
NaCl + AgNO3 = AgCl↓ + NaNO3 – білий сирнистий осад;
KBr + AgNO3 = AgBr↓ + KNO3 - блідо-жовтий осад;
КІ + AgNO3 = AgІ↓ + КNO3 - жовтий осад;
Na2SO4 + BaCl2 = BaSO4↓ + 2NaCl - дрібнокристалічний білий осад;
K3PO4 + 3AgNO3 = Ag3PO4↓ + 3KNO3 – жовтий осад;
Na2CO3 + H2SO4 = Na2SO4 + CO2↑ + H2O виділення газу;
Щоми можемо сказати про ці реакції? Чому ми позначаємо колір осаду чи те що виділився газ?(Це якісні реакції на деякі йони. Виділення газу і характерний колір позначають для того щоб виділити певний йон.)
IV. Мотивація навчальної діяльності.
Хоча нині багато методів хімічного аналізу вдосконалено та автоматизовано, знання про якісні реакції на певні йони лишаються актуальними (поясніть чому або спростуйте думку авторок підручника).
А чи достатньо нам тих якісних реакцій що ми знаємо? Адже існує безліч і інших йонів що потребують визначення.
Отже сьогодні ми продовжимо розвивати наші знання з теми «Якісні реакції на деякі йони». А саме будемо визначати в розчинах катіони; Феруму(ІІ), Феруму(ІІІ) (осадженням їх лугами), Барію, амонію, а також силікат- і ортофосфат-аніони.
Запишіть тему уроку « Якісні реакції на деякі Йони.»
V. Вивчення нового матеріалу.
Відкрийте підручник на сторінці 141 та прочитайте рубрику цікаво і пізнавально.
«Засновником якісного аналізу є англійський науковець Роберт Бойль (1627–1691). Він увів термін «хімічний аналіз» і застосовував різноманітні реактиви під час проведення якісного аналізу речовин. Для визначен ня сульфатної та хлоридної кислот учений використовував розчини вапняних солей та аргентум(І) нітрату відповідно, кислот і лугів – настойки лакмусу, фіалок, волошок тощо.»
Проаналізуйте дану інформацію. Про визначення яких аніонів та катіонів у ній ідеться? Складіть відповідні хімічні рівняння у скороченій йонній формі.
Зверніть увагу що в більшості якісних реакцій ми спостерігаємо за кольором та характером осаду. А отже утворення осадів - це один з основних аналітичних ефектів, саме тому більшість якісних реакцій є реакціями осадження.
Подивіться на таблицю. Що на ній зображено?
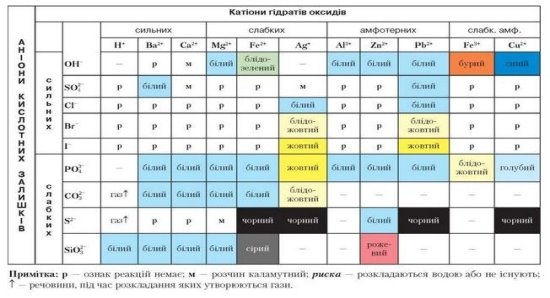
На які катіони ми сьогодні розглядаємо якісні реакції? Тож давайте знайдем їх та запишемо йонне скорочене рівняння на Fe2+ та Fe3+.

До цих і наведених далі скорочених йонних рівнянь доберіть по кілька молекулярних і повних йонних рівнянь, скориставшися за потреби таблицею «Розчинність основ, амфотерних гідроксидів, кислот і солей у воді»
Приклад:
FeCl2 + 2NaOH = Fe(OH)2↓ + 2NaCl.
FeCl3 + 3NaOH = Fe(OH)3↓ + 3NaCl.
Чому осад ферум(ІІ) гідроксиду на повітрі швидко набуває бурого кольору? Це зумовлено тим, бо під впливом кисню він перетворюється на ферум(ІІІ) гідроксид:
Fe(OH)2 + O2 + H2O = Fe(OH)3↓.
Катіони Барію можна осадити в різні способи (наведіть кілька з них, скориставшись, за потреби, таблицею «Розчинність основ, амфотерних гідроксидів, кислот і солей у воді»). Проте якісною зазвичай уважають реакцію осадження цих йонів сульфат-аніонами. Унаслідок її перебігу утворюється білий дрібнокристалічний осад барій сульфату, не розчинний у більшості кислот
![]()
Проведення фізкультхвилинки:
Всі знають таку гру як «Плескачі» Поділіться по двоє так як сидите за партою.
Раз права, два ліва, три обидві, раз, два.
Раз права, два ліва, три обидві, раз, два.
Обидві, обидві, раз, два, три.
Обидві, обидві, раз, два, три.
(Повторюємо декілька раз тільки змінюємо темп на більш швидкий)
Для проведення якісної реакцій на катіони амонію внесемо у пробірку водний розчин солі амонію об’ємом 1 мл, добавимо розчин лугу й злегка нагріємо вміст пробірки. Незабаром відчуємо різкий характерний запах амоніаку. Вологий індикаторний папірець, піднесений до отвору пробірки, змінить свій колір на синій. Тому, що відбудеться реакція обміну, унаслідок чого утвориться амоніак, який за нагрівання виділиться з розчину.
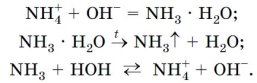
Тепер давайте звернемось до нашої таблиці. подивіться як можна виявити силікат- та ортофосфат-аніони.
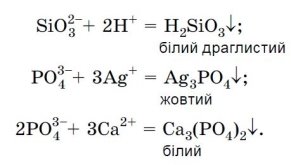
VI. Перевірка первинного розуміння.
Складіть опорний конспект вивченого на уроці. Якщо у вас виникнуть затруднення використовуйте §32.
(Учитель просить зачитати декількох учнів свої конспекти і корегує їх.)
VIІ. Закріплення нових знань.
Лабораторні роботи №3-8
(Інструктивна картка підручника «Хімія» Г.Лашевська, А.Лашевська сторінка 143)
Спілкування «питання- відповідь».
Ми по черзі складаємо питання наступний відповідає і складає питання далі.
Перше питання задаю я. «Що таке якісна реакція?»
VIII. Узагальнення та систематизація знань
Учні діляться на 4 групи і вирішують задачу на картках.
«Учень виконуючи дослід налив у дві пробірки ферум (ІІІ) хлорид та амоній хлорид, а позначити пробірки забув. Запропонуйте Сергійкові якими реагентами можна розрізнити в якій пробірці знаходиться ферум (ІІІ) хлорид а в якій амоній хлорид.»
«Учень виконуючи дослід налив у дві пробірки калій силікат та амоній сульфат, а позначити пробірки забув. Запропонуйте учневі якими реагентами можна розрізнити в якій пробірці знаходиться калій силікат а в якій амоній сульфат.»
«Учень виконуючи дослід налив у дві пробірки натрій ортофосфат та барій нітрат, а позначити пробірки забув. Запропонуйте учневі якими реагентами можна розрізнити в якій пробірці знаходиться натрій ортофосфат а в якій барій нітрат.»
«Учень виконуючи дослід налив у дві пробірки барій хлорид та алюміній сульфат, а позначити пробірки забув. Запропонуйте учневі якими реагентами можна розрізнити в якій пробірці знаходиться барій хлорид а в якій алюміній сульфат.»
IX. Домашнє завдання.
Опрацювати §32 підручника «Хімія» Г.Лашевська, А.Лашевська.
Напишіть повне йонно-молекулярні та скорочені рівняння до задач які виконувалися на уроці.
Попробуйте скласти подібну задачу.
Х. Підбиття підсумків уроку.
Отже сьогодні на уроці ми продовжили розвивати наші знання з теми «Якісні реакції на деякі йони». А саме навчилися визначати в розчинах катіони; Феруму(ІІ), Феруму(ІІІ) (осадженням їх лугами), Барію, амонію, а також силікат- і ортофосфат-аніони.
ХІ. Рефлексія.
Ми на початку уроку позначали на картках свій улюблений колір. А тепер давайте згадаємо чи згадували ми деякі з них на уроці. А це значить на скільки різноманітна і різнобарвна хімія.
Дякую за урок!


про публікацію авторської розробки
Додати розробку
