УРОК з теми « Кисень» ( узагальнення знань ( гра))
Тема: «Узагальнення знань з теми «Кисень»»
Мета:
навчальна: узагальнити та закріпити знання учнів про склад властивості і застосування кисню; сприяти розвитку логічного мислення та творчого підходу при вирішенні питань.
розвивальна: розвивати самостійне мислення учнів та вміння працювати в команді; розвивати розумові здібності та якості особистості (уяву, мислення, увагу, пам'ять).
виховна: виховувати повагу до чужих думок, відповідальність за результат командної роботи.
Тип урока: узагальнення, систематизація і корекція знань
Форма проведення: урок-гра «Сходження на пік знань»
ХІД УРОКУ
До початку уроку клас ділиться на 4 команди. Необхідно вибрати командира та придумати назву своєї команди
- Організаційний момент ( 1 хв)
Сьогодні ми з вами здійснимо подорож у країну, де править Кисень. Крок за кроком, долаючи перешкоди у вигляді різноманітних завдань, ми зможемо потрапити туди.
- Мотивация (2 хв)
Вчитель:
На початку уроку я хочу прочитати вам уривок з твору Л.Кєррола «Аліса в країні чудес»: « За кілька кроків від неї сидів на гілці Чеширській кіт.
— Скажите, пожалуйста, куда мне отсюда идти?
— А куда ты хочешь попасть? — ответил Кот.
— Мне все равно… — сказала Алиса.
— Тогда все равно, куда и идти, — заметил Кот».
Питання до учнів
1. Що хотів цим сказати кіт Алісі?
2. Навіщо я вам прочитала ці слова напочатку уроку? (відповіді учнів)
Продовжить фразу
- Сьогодні на уроці я …..
- Узагальнення, систематизація та корекція знань ( проведення гри)
Правила гри:
1. До початку уроку розділитися на 4 команди;
2. Вибрати командира команди;
3. Отримати картку учасника. (Додаток 1)
4. Ознайомитись з ігровим полем ( Додаток 2)
№1 - №28 ( от 0,5 до 2 балів)
№13 - №27 (зроби крок вперед)
№9 розовый (зроби 2 кроки назад)
№19 желтый (пропусти хід)
|
№ |
Бали |
Завдання |
Відповідь |
||
|
1 |
2б |
В результаті спалювання простих речовин в кисні отримані оксиди, формули яких SO2, Al2O3, ZnO
|
S; Al; Zn. S + O2 = S(Ⅵ)O(Ⅱ)2 4Al + 3O2 = 2Al(III)2O(Ⅱ)3 2Zn + O2 = 2Zn(Ⅱ)O(Ⅱ)
|
||
|
2 |
1б |
Які реакції називаються реакціями розкладання? Приведи приклади. |
Хімічні реакції, при яких з однієї складної речовини утворюються дві або більше нових речовин (простих або складних), називаються реакціями розкладання. 2KMnO4 = K2MnO4 + MnO2 + O2↑ Умова: тем- ра 2H2O2 = 2H2O + O2↑ Умова: MnO2 |
||
|
3 |
1б |
Завдання «Стара шпаргалка». Закінчити рівняння реакцій, провести балансування. Zn + O2 = … Al + Cl2 = … |
2Zn + O2 = 2Zn(Ⅱ)O(Ⅱ) 2Al + 3Cl2 = 2Al(III) Cl(Ⅰ)3
|
||
|
4 |
1б |
Якщо потримати шматочок цукру в полум'я газового пальника, цукор стає коричневим і починає плавитися. Однак цукор не запалюється. Але, якщо струсити трошки сигаретного попелу на цей шматочок цукру, він спалахне і повільно згорить.
|
Так. У цьому каталітичному процесі сигаретний попіл, звичайно ж, діє як каталізатор. Цей каталізатор прискорює хімічний процес горіння цукру настільки, що, навіть якщо видалити полум'я газового пальника, горіння цукру буде тривати. Сам по собі сигаретний попіл ніяким чином не змінюється в цьому процесі. |
||
|
5 |
1б |
Як перевірити наявність кисню в пробірці? |
За допомогою тліючої скіпки; тліюча скіпка спалахує, так як O2 підтримує горіння. |
||
|
6 |
1б |
Агрегатний стан і фізичні властивості кисню. |
Кисень - це безбарвний газ без смаку і запаху, погано розчинний у воді, трохи важчий за повітря. При t = - 1830C переходить в рідкий стан (рідкий кисень рухома рідина блакитного кольору), а при t = - 2190C - в сині кристали. |
||
|
7 |
0,5б |
З наведеного переліку речовин виписати оксиди: Mn(OH)2, MgO, H2SO3, SO3, CaO, CaCO3, Na2O, Na2SiO3. |
MgO, SO3, CaO, Na2O.
|
||
|
8 |
0,5б |
Вибрати реакції горіння: А) 2Ba + O2 = 2BaO Б) Zn + Cl2 = ZnCl2 В) 4Al + 3O2 = 2Al2O3 Г) 2Mg + O2 = 2MgO Д) 3K + P = K3P |
А) 2Ba + O2 = 2BaO В) 4Al + 3O2 = 2Al2O3 Г) 2Mg + O2 = 2MgO
|
||
|
9 |
0б |
Два кроки назад |
|||
|
10 |
2б |
В природе очень широко встречаюсь И газом жизни называюсь. Легко лучинкой меня ты открываешь, Когда соль марганца При нагревании разлагаешь.
|
2KMnO4 =t K2MnO4 + MnO2 + O2↑ Сума: 5
|
||
|
11 |
1б |
В одній колбі міститься кисень, а в іншій повітря. Як розпізнати, в якій колбі кисень? |
Внести тліючу скіпку; тліюча скіпка в кисні спалахує і горить набагато швидше, ніж в повітрі. |
||
|
12 |
2б |
Вкажіть області застосування кисню. |
- в промисловості (виплавка чавуну і сталі; отримання нітратної і сульфатної кислот) - кисень необхідний для наповнення балонів спеціальних приладів, якими користуються льотчики під час висотних польотів, космонавти, пожежники при рятувальних роботах, водолази під час роботи під водою. - в медицині (кисневі подушки, кисневі намети, кисневі коктейлі) |
||
|
13 |
0б |
Крок вперед |
|||
|
14 |
1б |
Чи діє кисень як каталізатор, коли внесена в нього тліюча лучинка спалахує і горить набагато швидше, ніж в повітрі? |
Ні. Чистий кисень не є каталізатором. Всякий процес горіння обов'язково протікає в повітрі повільніше, ніж в чистому кисні, але лише тому, що повітря має невисокий вміст кисню (20%) |
||
|
15 |
0,5б |
Бліц опитування А. Найпоширеніший елемент - неметалл на Землі? Б. Назва якого елемента неметалла в перекладі з латинської означає «той, який народжує кислоти»? В. Сам не горить, а горіння підтримує? Г. Речовина, що містять три атому Оксигену. |
А. Оксиген Б. Оксиген В. Кисень Г. Озон |
||
|
16 |
2б |
Отримайте кисень з пероксиду водню. Знайдіть суму коефіцієнтів у правій частині рівняння. |
2H2O2= 2H2O + O2 Умова: MnO2 Сума = 3
|
||
|
17 |
1б |
Впишіть відсутні слова в наступне визначення: ... - це речовина, яка ... хімічну реакцію, але в кінці реакції залишається в той же формі, як і напочатку. Процес, що протікає за участю ..., називається ... |
Каталізатор - це речовина, яка прискорює хімічну реакцію, але в кінці реакції залишається в той же формі, як напочатку. Процес, що протікає за участю каталізатора, називається каталітичним |
||
|
18 |
2б |
Повітря не чиста речовина, а суміш, що складається головним чином з двох газів. Один з них бере участь у горінні і, отже, споживається при цьому процесі. Інший газ не бере участь в горінні і, отже, не витрачається. Назвіть ці два газу. Запам'ятали ви пропорцію цих двох газів в повітрі? А. приблизно 2/5 першого і 3/5 другого Б. приблизно 4/5 першого і 1/5 другого В. приблизно 1/5 першого і 4/5 другого |
O2 та N2 В. Приблизно 1/5 кисню (O2) та 4/5 азоту (N2)
|
||
|
19 |
0б |
Пропускаєш хід |
|||
|
20 |
2б |
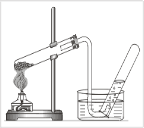
Розгляньте рис.1 і рис.2 і назви два способи збору кисню. Порівняй їх і вкажи, при яких фізичних властивостях кисню вони засновані?
|
Рис.1 (метод витіснення води) Рис. 2 (метод витіснення повітря) O2 погано розчиняється у воді. O2 важчий за повітря |
||
|
21 |
2б |
Напишіть рівняння реакції горіння ацетилену C2H2. Вкажіть суму коефіцієнтів в цьому рівнянні. |
2 C2H2 + 5O2 = 4CO2 + 2H2O Сума = 13
|
||
|
22 |
1б |
Як відбувається кругообіг кисню в природі? |
Трохи кисню з повітря використовується не тільки в господарській діяльності, а й у процесі дихання людини, тварин, рослин, при спалюванні палива, гнитті і тлінні органічних залишків. Як же поповнюються його запаси в повітрі? Атмосферний кисень утворюється в результаті фотосинтезу, який відбувається в зелених рослинах на світлі. Рослини нашої планети щорічно виділяють в атмосферу 5 * 1011т О2. Однак цієї кількості достатньо тільки для компенсації його природних втрат. Ось чому так важливо зберігати і висаджувати зелені насадження. |
||
|
23 |
2б |
Як можна розкласти воду на кисень і водень? За допомогою фізичного або хімічного процесу? |
Вода є сполукою. Тому її можна розкласти тільки за допомогою хімічного процесу, наприклад електролізу: 2H2O =эл.ток 2H2↑ + O2↑ |
||
|
24 |
2б |
Напишіть рівняння реакції горіння бутану С4Н10. Вкажіть суму коефіцієнтів у правій частині рівняння. |
2C4H10 + 13O2 = 8CO2 + 10H2O Сума = 18
|
||
|
25 |
0,5б |
До процесів повільного окислення відносяться: А. дихання живих організмів Б. гниття і тління В. іржавіння заліза Г. Горіння |
А. дихання живих організмів Б. гниття і тління В. іржавіння заліза |
||
|
26 |
2б |
Записати рівняння хімічної реакції отримання кисню з калій хлорату. Знайдіть суму коефіцієнтів у правій частині рівняння. |
2KClO3 = 2KCl + 3O2↑ Умова: MnO2 Сума = 5
|
||
|
27 |
0б |
Зроби крок вперед |
|||
|
28 |
2б |
Напишіть рівняння реакції горіння сірководню Н2S. Вкажіть суму коефіцієнтів у лівій частині рівняння |
2H2S + 3O2 = 2SO2 + 2H2O Сума = 5
|
||
- Підсумки
- Домашнє завдання. (підготуватися до контрольної роботи з теми «Кисень»)
Література
Химия.7 кл.: учебник для 7 класса общеобразоват. учебн. заведений с обучением на русском языке /А.В.Григорович.–Харьков: Изд-во «Ранок», 2015. – 192 с. : ил.
Додадок 1
|
Картка учасника |
|
|
ПІБ : |
Кількість отриманих балів |
|
№1 |
|
|
№2 |
|
|
№3 |
|
|
№4 |
|
|
№5 |
|
|
№6 |
|
|
№7 |
|
|
№8 |
|
|
№9 |
|
|
№10 |
|
|
№11 |
|
|
№12 |
|
|
№13 |
|
|
№14 |
|
|
№15 |
|
|
№16 |
|
|
№17 |
|
|
№18 |
|
|
№19 |
|
|
№20 |
|
|
№21 |
|
|
№22 |
|
|
№23 |
|
|
№24 |
|
|
№25 |
|
|
№26 |
|
|
№27 |
|
|
№28 |
|
|
Всього балів |
|
Додаток 2



про публікацію авторської розробки
Додати розробку