Збірник дидактичних ігор
![]()


Автор:
Денейчук Людмила Василівна ,
вчитель хімії загальноосвітньої школи І-ІІІ ст. села Нуйно.
В посібнику зібрано цікаві вправи та задачі в ігровій формі та допоможе вчителям творчо та цікаво підготуватися до уроку та позакласного заходу з хімії
Збірник призначений для вчителів хімії загальноосвітніх навчальних закладів.
Схвалено методичною радою школи , протокол №5 від 4 березня 2019 року
ЗМІСТ
Вступ ……………………………………………………………………………3
Настільні ігри……………………………………………………………….…9
Ребуси………………………………………………………………………...…9
Кросворди……………………………………………………………………..13
Головоломки………………………………………………………………..…27
Хрестики - нулики……………………………………………………………35
Ігри – вправи………………………………………………………………...37
Загадки ………………………………………………………………………..37
Гра «біла ворона»…………………………………………………………….41
Гра «ТАК - НІ»………………………………………………………………..43
Ігри-ролі………………………………………………………………………47
Ситуаційні задачі……………………………………………………………..47
Казки…………………………………………………………………………...50
Використана література…………………………………………………….51


Гра – це величезне світле вікно, через яке в духовний світ дитини вливається цілющий потік уявлень, понять про природу.
В.О. Сухомлинський
ВСТУП
Сьогодні перед сучасною педагогічною наукою постала проблема, як підвищити інтерес учнів до процесу навчання. Одна з причин втрати інтересу - це непридатність низки традиційних прийомів навчання до сучасного контингенту учнів, адже в сучасної молоді значно розвинене почуття самосвідомості та власної гідності, вона багато про що має уявлення, тому заняття, що базуються на авторитарному тиску, наказах, вказівках викликають лише роздратування й нудьгу.
“Давно визнано, що гра займає значну частину життя дитини. Ще у вісімнадцятому столітті Ж. Ж. Руссо писав про те, що для того, щоб пізнати та зрозуміти дитину, необхідно спостерігати за його іграми». Про першорядне значення гри, для природного розвитку дитини свідчить той факт, що ООН проголосила гру універсальним та невід’ємним правом дитини.
“Гра для дітей – засіб навчитися тому, чому їх ніхто не може навчити. Це засіб дослідження та орієнтації в реальному світі, просторі та часі, речах, тваринах, людях. Включаючись в процес гри, діти навчаються жити в нашому символічному світі – світі змістів та цілей, в той же час досліджуючи, експериментуючи, навчаючись”.
Крім того, гра створює особливі умови, за яких розвивається творчість учнів. Сутність цих умов полягає у спілкуванні на рівних, де зникає боязкість, виникає відчуття – “я теж можу”, тобто у грі відбувається внутрішнє розкріпачення. В ній органічно закладена пізнавальна задача та відчувається самостійний пошук знань. “Оволодіння знаннями у грі – нова, унікальна умова співпраці однолітків, умова набування інтересу та поваги один до одного».
За визначенням, гра – це вид діяльності в умовах ситуацій, спрямованих на відновлення та засвоєння суспільного досвіду, в якому складається та удосконалюється самоуправління поведінкою.
В людській практиці ігрова діяльність виконує такі функції:
- Розважальну (це основна функція гри – розважити, приносити задоволення, надихнути, пробудити інтерес);
- Комунікативну: засвоєння діалектики спілкування;
- Самореалізації: адже гра, як полігон людської практики;
- Ігротерапевтичну: подолання різних труднощів, що виникають у інших видах життєдіяльності;
- Діагностичну: виявлення відхилень від нормативної поведінки, самопізнання в процесі гри;
- Функцію корекції: внесення позитивних змін в структуру особистих показників;
- Міжнаціональної комунікації: засвоєння єдиних для всіх людей соціально-культурних цінностей;
- Соціалізації: включення в систему суспільних відношень, засвоєння норм людського спілкування.
Для більшості ігор властиві чотири головні риси :
- ПРОЦЕДУРНЕ ЗАДОВОЛЕННЯ- вільна розливальна діяльність, що застосовується лише за бажанням дитини, заради задоволення від самого процесу діяльності, а не лише від результату;
- «ПОЛЕ ТВОРЧОСТІ» - творчий, в значній мірі імпровізований, дуже активний характер цієї діяльності
- «ЕМОЦІЙНА НАПРУГА» - емоційне піднесення діяльності, суперництво, змагальність, конкуренція, та ін.
- Наявність прямих або непрямих правил, що відображають зміст гри, логічну та тимчасову послідовність її розвитку/
В сучасній школі, що робить ставку на активізацію та інтенсифікацію учбового процесу, ігрова діяльність використовується в наступних випадках:
- в якості самостійних технологій для засвоєння понять, теми та навіть розділу учбового предмету;
- як елементи більш різноманітної технології;
- якості уроку або його частини (вступ, пояснення, закріплення, вправи, контролю);
- як технології позакласної роботи.
Організація гри починається з її задуму. Тут необхідно пояснити умови та закони існування ігрового світу. При цьому особливу увагу необхідно приділити наступним моментам: задумана ситуація повинна бути цілісна та повна, та припускати численні ситуації, в тому числі заздалегідь не задані. Чим повніше та більше задумане, тим краще. Однак тут слід зробити поправку на досвід гравців.
Наступний етап організації гри, розробка правил. При цьому слід враховувати наступні моменти: щоб запобігти суперечок в процесі гри правила повинні бути зафіксовані в письмовому вигляді. Всі учасники повинні бути ознайомлені з правилами до початку гри. В правилах повинна міститися наступна інформація:
- Загальний опис гри та ситуації на момент її початку;
- Перелік учасників та основних команд із вказівкою їх іміджу;
- Правила перерахунку реального та ігрового часу;
- Окремі відомості гри.
Динаміка гри в цілому забезпечується наступними факторами:
- Фактор підготовки учасників. Для гри дуже важливо, щоб гравець усвідомив свою мету.
- Фактор пророблення цілі. Це визначальний фактор для успішного проведення гри.
- Фактор підтримки цілі. “Ціль повинна світити учаснику всю гру так як вона є пружиною, що штовхає учня до дії.
Дидактичні ігри з хімії можна класифікувати за різними ознаками. Їх можна поділити на індиівідуальні, парні, групові. Залежно від засобів і загальної спрямованості ігор на: ігри-вправи, настільні ігри, ігри-ролі та ігри -моделювання
Застосування ігор на уроках хімії показує затребуваність учнями даної технології. Результати анкетування виявили наступну картину: уроки-ігри, та уроки з елементами гри подобаються 70% опитаних учнів.
Отже:
- Практика показує, що успішне вивчення хімії в школі практично неможливе без розвитку пізнавального інтересу учнів.
- Уроки хімії з використанням ігрових прийомів, які роблять захоплюючим навчальний процес, сприяють появі активного пізнавального інтересу школярів. На таких заняттях складається особлива атмосфера, де є елементи творчості та вільного вибору. Розвивається вміння працювати в групі: Адже її перемога залежить від особистих зусиль кожного. Достатньо часто це вимагає від учня подолання власної соромливості та нерішучості, невіри в свої сили. Таким чином, реалізується саморозвиток школярів, який виражається не лише в розвитку інтелекту, але і в збагаченні емоційної сфери та становленні вольових якостей особистості, формуванні адекватної самооцінки.
- Також ігри розвивають здібності школярів до критичного сприйняття навколишньої дійсності та переживанню.
- Хімічні ігри повнофункціональні. Вони дуже гармонійно поєднують фактичний та теоретичний матеріал, звичайне сприйняття інформації та творчу роботу, емоційний та логічний засіб сприйняття – словом, примушують активно функціонувати різні рівні пізнавальної діяльності учнів.
- Гра спонукає до активної роботи на уроці кожного учня. Гра – форма роботи, що протистоїть пасивному слуханню. В процесі гри інтелектуально пасивні діти звичайно виконують такий обсяг учбової діяльності, який їм недосяжний в звичайній навчальній ситуації
- Робота вчителя за даною методикою дозволяє вирішити проблему сумісності в одному класі учнів з різними темпераментами. Не секрет, що при швидкому темпі ведення уроку флегматики та меланхоліки розгублюються, не поспішають слідкувати за думкою вчителя та виконувати всі завдання. Сповільнений темп уроку, навпаки, примушує нудьгувати холериків. Вони починають відволікатися, порушувати дисципліну, їм просто нецікаво на уроці.
- Контроль уваги та темпу уроку, різна ступінь узагальнення матеріалу, неодноразове його вдосконалення, дозволяє засвоїти практично весь учбовий матеріал на уроці, при мінімумі самостійної роботи у позаурочний час

,,,,


бензол
 синтез
синтез кислота
кислота
|
РТ=М |
атом
|
,,
Т=Д |
Менделєєв
|
К=М Я=А |
молекула
|
|
хлорид
|
|
кислота



Щоб розв’язати цей кросворд необхідно серед явищ природи та предметів, пов’язаних із водою, знайти «загублене» слово до якого немає картинки. Слова ламаються під прямим кутом і не перетинаються.
|
А |
Н |
Л |
Е |
К |
У |
Л |
С |
А |
Г |
|
Р |
И |
О |
У |
Л |
А |
А |
П |
Р |
А |
|
І |
Д |
М |
М |
Р |
Н |
И |
О |
Р |
Щ |
|
І |
Ж |
И |
Г |
О |
З |
Ч |
М |
Е |
О |
|
Н |
С |
Н |
Р |
Ф |
О |
Р |
А |
Б |
Д |
|
Д |
А |
К |
Е |
Б |
И |
К |
Ш |
Ь |
Л |
|
И |
С |
Л |
Я |
С |
Ч |
К |
А |
Б |
У |
|
И |
Т |
П |
А |
Й |
І |
І |
Г |
О |
Л |
|
Л |
Л |
І |
Р |
А |
Р |
Д |
Р |
И |
А |
|
Я |
Т |
Д |
К |
Т |
А |
Р |
К |
С |
Т |
















Малі пустуни H, C, P, S, K, Ca, Mg, Fe, Zn, Pb, Cl, O, N, Cu, Ag, B, F, Ba, I переплутали всі літери у своїх назвах. Допоможіть їм відновити свої імена із запропонованих літер. Якщо ви все зробите правильно, то з літер, які залишаться, складеться назва хімічного елемента, названого на честь видатного російського хіміка.
|
К |
І |
Д |
Р |
А |
Л |
Ь |
Й |
И |
Н |
О |
Р |
|
А |
Г |
Н |
О |
К |
І |
Ц |
І |
Ц |
К |
У |
У |
|
Р |
Б |
О |
Г |
Й |
Й |
Г |
Н |
М |
П |
Л |
Й |
|
Ф |
О |
Н |
Е |
І |
М |
А |
Р |
У |
Л |
Ф |
О |
|
Ф |
С |
С |
І |
Ц |
Й |
І |
Е |
М |
Ю |
Й |
Д |
|
О |
Р |
И |
Л |
К |
А |
Л |
Ф |
Б |
У |
І |
Р |
|
О |
К |
М |
Г |
І |
К |
У |
Г |
О |
М |
Б |
А |
|
И |
С |
У |
Т |
Д |
М |
П |
Е |
Р |
Н |
О |
Б |
|
Г |
Е |
Н |
Н |
Р |
У |
Р |
Н |
Т |
І |
Р |
Й |
|
Х |
Л |
Г |
Е |
А |
Р |
Г |
І |
Р |
У |
М |
І |
|
Р |
О |
Р |
А |
М |
Е |
Н |
Д |
Е |
Л |
Е |
В |
Слова ламаються під прямим кутом і не перетинаються.

Почавши рух з верхньої лівої клітинки та рухаючись вліво, вправо, вверх і вниз пройдіть усі клітинки так, щоб із літер утворилося правило безпечного нагрівання пробірок.
|
П |
Б |
І |
У |
З |
Д |
И |
Ю |
, |
|
Р |
О |
Р |
К |
Р |
І |
Н |
О |
Щ |
|
Е |
Р |
Я |
С |
Є |
А |
Р |
Г |
О |
|
Б |
Т |
, |
Ь |
Т |
В |
І |
А |
Н |
|
А |
И |
М |
И |
О |
О |
Р |
В |
І |
|
Т |
Р |
А |
Т |
Т |
В |
О |
М |
Д |
|
В |
І |
Р |
А |
Т |
Д |
І |
Е |
С |
|
. |
Ш |
И |
В |
О |
І |
В |
Б |
Е |

Впишіть в клітинки кросворду назви лабораторного посуду та обладнання і по вертикалі побачите назву спеціально обладнаного приміщення для проведення дослідів і аналізу речовин.
|
|
1 |
|
|
|
|
|
||||||||
|
|
2 |
|
|
|
|
|
|
|
||||||
|
|
3 |
|
|
|
|
|
|
|
||||||
|
|
4 |
|
|
|
|
|||||||||
|
|
5 |
|
|
|
|
|
|
|||||||
|
|
6 |
|
|
|
|
|
|
|
|
|
|
|||
|
|
7 |
|
|
|
|
|
||||||||
|
|
8 |
|
|
|
|
|
|
|
||||||
|
|
9 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
10 |
|
|
|
|
|
|
|
|
|
|||||
|
11 |
|
|
|
|
|
|
|
|
||||||

1. Скляна плоскодонна, конічна або круглодонна посудина для проведення хімічних експериментів.
2. Пристосування для відбирання порцій твердих сипучих речовин.
3. Основний лабораторний посуд учнів.
4. Матеріал для виготовлення лабораторного посуду.
5. Пальне для спиртівки.
6. Посуд для дозування розчину краплями.
7. Деталь лабораторного штатива.
8. Разом із ступкою використовується для подрібнення часточок твердої речовини.
9. Хімічна операція, яка неможлива без лійки.
10. Нагрівний прилад.
11. Матеріал, з якого виготовляють чашки для випарювання розчинів.

Впишіть у клітинки кросворду назви хімічних елементів. Ключове слово – прізвище відомого шведського хіміка, що запропонував сучасні назви хімічних елементів.
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Na |
|
|
|
|
|
|
|
|
|
|
|
|
K |
|
|
|
|
|
Fe |
|
|
|
|
|
Cu |
|
|
Br |
|
|
Zn |
|
|
I |
|
S |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|


Розгадайте запропонований кросворд. Якщо ви не зможете пригадати потрібні слова, зверніться по допомогу до підручника ( тема «Розчини»).
|
|
1 |
|
|
|
|
|
|
|
|
|
|
||||
|
|
2 |
|
|
|
|
|
|
||||||||
|
|
3 |
|
|
|
|
|
|
|
|||||||
|
4 |
|
|
|
|
|
|
|
|
|
||||||
|
|
5 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
6 |
|
|
|
|
|
|
|
|||||||
|
|
7 |
|
|
|
|
|
|
|
|
||||||
|
|
|
8 |
|
|
|
|
|
|
|||||||
|
|
9 |
|
|
|
|
||||||||||
|
|
10 |
|
|
|
|
||||||||||
|
|
11 |
|
|
|
|
|
|
|
|
||||||
|
12 |
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
13 |
|
|
|
|
|
|
|
|
||||||
|
14 |
|
|
|
|
|
|
|
|
|
|
|||||
|
|
15 |
|
|
|
|
|
|
|
|
|
|
||||
Якщо ви вірно розгадаєте кросворд, у виділених клітинках прочитаєте загальну назву кристалічних речовин, що містять у своєму складі певну кількість молекул води.
1. Сполуки, водні розчини і розплави яких проводять електричний струм.
2. Однорідна суміш речовин.
3. Електроліти, які дисоціюють з утворенням катіонів одного типу – йонів Гідрогену.
4. Струшена суміш рідини і нерозчинної в ній добре подрібненої твердої речовини.
5. Розчин у якому міститься значно більше розчинної речовини ніж розчинника.
6. Електроліт, який незначною мірою дисоціює на йони.
7. Струшена суміш нерозчинних одна в одній рідин.
8. Частинка з двома різнойменно зарядженими полюсами.
9. Електроліти, які дисоціюють з утворенням аніонів одного типу – гідроксид-йонів.
10. Неоднорідна суміш газу і рідини.
11. Міжмолекулярний хімічний зв'язок за участю атомів Гідрогену.
12. Сполуки, водні розчини і розплави яких не проводять електричний струм.
13. Розчин, у якому за даних умов речовина більше не розчиняється.
14. Реакція приєднання води до сполуки.
15.Властивість речовини утворювати з іншою речовиною розчин.

Розгадайте кросворд і у виділених клітинках по вертикалі прочитайте назву здатності сполук алюмінію виявляти як основні, так і кислотні властивості.
|
|
1 |
|
|
|
|
||||||
|
|
2 |
|
|
|
|
||||||
|
3 |
|
|
|
|
|
|
|
||||
|
|
4 |
|
|
|
|
|
|||||
|
|
5 |
|
|
|
|
|
|||||
|
|
6 |
|
|
|
|
|
|
|
|
|
|
|
|
7 |
|
|
|
|
||||||
|
|
8 |
|
|
|
|
|
|
||||
|
9 |
|
|
|
||||||||
|
|
10 |
|
|
|
|
|
|
||||
|
11 |
|
|
|
|
|
||||||
|
12 |
|
|
|
|
|
|
|||||
1. Інвар, дюраль, бронза, чавун, сталь… .
2. Складова частина латуні.
3. Тугоплавкий метал електричних лампочок.
4. Солдатик Андерсена.
5. Самий м’який метал.
6. Покриття предметів нікелем.
7. «Харчується» залізом.
8. Сплав для вимірювальних приладів високої точності.
9. Центр залізорудного басейну Кривий… .
10. Столове … .
11. Рідкий метал.
12. Лужноземельний метал.

|
|
|
|
|
|
|
|
|
|
|
6 |
|
|
|
|
|
|
|
|
|
|
4 |
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
|
|
3 |
|
|
5 |
|
|
|
|
7 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1. Речовина, за допомогою якої можна змити фарбу або лак
2. Речовини для зміни кольору речей.
3. Наслідок вдихання випарів
4. Вугілля, яке вживають при отруєнні
5. Речовина для закріплення зачіски.
6. Стан підвищеної чутливості організму на речовини побутової хімії.
7. Речовини, які людина вживає під час хвороб.


Знайдіть хімічні елементи за положенням у Періодичній системі та впишіть їхні назви у клітинки кросворду. З перших літер ви отримаєте назву елемента четвертого періоду.
|
1 |
|
|
|
|||
|
2 |
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
4 |
|
|
|
|
|
|
1) ІІ період, ІІІ група;
2) V період, І група, головна підгрупа;
3) ІІ період, VІ група;
4) ІІІ період, ІІ група.
Мандруючи Періодичною системою, ви зустрінете немало назв хімічних елементів, що містять літеру «А». Впишіть ці назви у запропоновані сітки.
|
|
А |
|
|
|
|
|
|
А |
|
|
|
|
|
|
А |
|
|
|
|
|
|
А |
|
|
|
|
|
|
А |
|
|
|
|
|
|
А |
|
|
|
|
|
|
А |
|
|
|
|
|
|
А |
|
|
|
|
|
А |
|
|
|
|
|
|
А |
|
|
|
|
А |
|
|
|
|
|
|
А |
|
|
|
|
А |
|
|
|
|
|
|
А |
|
|
|
|
А |
|
|
|
|
|
|
А |
|
|
|
Впишіть по горизонталі назви хімічних елементів,
що починаються з літери «Н».
|
|
|
|
||||
|
|
|
|
|
|
||
|
|
|
|
|
|
||
|
|
|
|
|
|
||
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|

Впишіть по горизонталі назви хімічних елементів,
що закінчуються літерою «Н».
|
|
|
|
||||
|
|
|
|
||||
|
|
|
|
|
|||
|
|
|
|
|
|||
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|




Уважно роздивіться таблицю і визначте, скільки разів у ній зустрічаються записи, які означають:
1) вільні атоми;
2) формули простих речовин;
3) формули складних речовин.
|
Cl2 |
O2 |
SO2 |
PH3 |
H2 |
F2 |
O |
|
N2 |
CuO |
CH4 |
P |
CaCl2 |
CO2 |
KOH |
|
BaS |
PCl3 |
H2O |
MgS |
HCl |
CaO |
CO |
|
SiO2 |
F |
HF |
Cl |
P2O5 |
H |
N |

Уважно роздивіться таблицю і визначте, скільки разів у ній зустрічаються записи, які означають:
1) одну молекулу простої речовини, яка складається з 2 атомів;
2) два атоми хімічного елемента;
3) дві молекули складної речовини;
4) одну молекулу складної речовини;
5) чотири молекули складної речовини.
|
2H |
2O2 |
CO2 |
2PH3 |
2Cl |
O2 |
O3 |
|
H2 |
2CO2 |
N2 |
4O2 |
O |
2O |
3CO2 |
|
2SO2 |
Cl2 |
CO |
2Cl |
4N |
4CCl4 |
N2 |
|
2N |
HNO3 |
4H2 |
H2O |
2H |
4Br2 |
4O |
|
S |
4NO |
2Cl2 |
HPO3 |
4NO2 |
CH4 |
3CO |
|
HCl |
N2O |
CS2 |
2HCl |
H |
2H2O |
2CH4 |

Виконавши завдання без помилок, із літер складете прізвище відомого російського хіміка.
|
Формули речовин |
Оксиди |
Основи |
Кислоти |
Солі |
|
К2О |
Л |
К |
Б |
А |
|
ВаСІ2 |
П |
Е |
М |
О |
|
СО2 |
М |
С |
Ф |
Н |
|
NaOH |
Д |
О |
Л |
Т |
|
H2S |
И |
Р |
Н |
Е |
|
CaCO3 |
Ш |
С |
К |
О |
|
HNO3 |
А |
Л |
С |
Я |
|
KOH |
У |
О |
В |
Р |
|
P2O5 |
В |
Є |
И |
Т |

Ця чудова вправа допоможе вам краще орієнтуватися в класах неорганічних сполук, розвине вашу «хімічну» увагу, активізує зорову пам'ять.
Уважно роздивіться запропоновані формули і спробуйте відповісти на запитання.
|
|
А |
Б |
В |
Г |
Д |
Е |
Ж |
|
1 |
SO2 |
CuO |
Na2S |
H2O |
KCl |
CaCl2 |
NaOH |
|
2 |
HCl |
H2S |
HNO3 |
HF |
H2O |
HBr |
H2CO3 |
|
3 |
NaCl |
NaNO3 |
AlCl3 |
Na2SO4 |
KF |
MgCO3 |
KNO3 |
|
4 |
CuO |
Na2O |
K2O |
FeO |
CaO |
HgO |
BaO |
|
5 |
Na2S |
H2CO3 |
C |
Na2CO3 |
O2 |
Al2O3 |
HCl |
|
6 |
HF |
Hl |
HNO3 |
HBr |
H2S |
HCl |
H2SO4 |
|
7 |
S |
P |
H2 |
Cl2 |
N2 |
C |
O2 |
|
8 |
CO2 |
NO |
P2O5 |
H2O |
CaO |
MgO |
SO3 |
|
9 |
Zn |
H2SO4 |
S |
CaCl2 |
C |
H2O |
KCl |
|
10 |
NO |
Cl2 |
NaCl |
H2 |
S |
N2 |
Al(OH)3 |
|
11 |
NaOH |
KOH |
LiOH |
Al(OH)3 |
H2O |
Ba(OH)2 |
Ca(OH)2 |
|
12 |
N2 |
H2O |
HF |
P |
NaF |
H3PO4 |
SO2 |
- У якому ряду знаходяться лише формули простих речовин?
- Які ряди складаються тільки з формул оксидів?
- У якому ряду знаходяться лише формули основних оксидів?
- У якому ряду записано формули лише кислот? Солей?
- Формула якої речовини повторюється найчастіше?
- Скільки формул сполук Натрію наведено в таблиці?
- Формула якої простої речовини зустрічається тільки один раз?
- Формули яких складних речовин зустрічаються по одному разу?
- Де знаходяться формули солей – хлоридів, карбонатів та ін.?

Працюємо із цим завданням як з таблицею розчинності. Літери, що відповідають вірним відповідям, утворять ключове слово – прізвище видатного вченого, лауреата Нобелівської премії, автора теорії електролітичної дисоціації.
|
|
АІ |
ОН |
Аg |
СІ |
Fe |
Н |
SO4 |
|
Катіони, які присутні в розчині алюміній сульфату |
А |
К |
О |
З |
В |
Г |
Р |
|
Аніони, які присутні в розчині сульфатної кислоти |
В |
М |
Ч |
А |
І |
М |
Р |
|
Аніон, який зв’язує йони Купрум (ІІ) |
Т |
Р |
П |
З |
Н |
С |
К |
|
Йони, присутні в розчинах лугів |
М |
Е |
Ц |
М |
О |
Д |
У |
|
Йони, присутні в розчинах кислот |
Г |
Р |
Ш |
Е |
У |
Н |
С |
|
Йони, якими визначають хлорид-йон |
Ф |
Н |
І |
В |
Я |
Л |
Т |
|
Йони, якими утворюється молекула води |
М |
У |
Р |
Б |
К |
С |
В |



В «секретному повідомленні» заховані формули оксидів. Спробуйте знайти і назвати їх.
K2OSNO2P2O3CuSO4NH3P2O5ZnOB2O3

|
NaCl |
Й. З. |
|
H2O |
К. З. |
|
Cu |
? |
|
Менделєєв |
Р |
|
Авогадро |
І |
|
Лавуазьє |
? |
|
Фосфор |
Н |
|
Натрій |
М |
|
Алюміній |
? |

Якщо до імені римського імператора, відомого своєю жорстокістю, додати літеру «й», то отримаємо назву нервової клітини. Якщо ж тепер додати літеру «т» - назву елементарної частинки, яка входить до складу атомного ядра.



Підставивши замість літер відповідні числові значення, розв’яжіть приклад:
p q________________________________________
√ √ (а : b - c) : d + m – n
a – рік відкриття Періодичного закону;
b – число елементів, властивості яких передбачив Дмитро Іванович Менделєєв;
c – число елементів, відомих на момент відкриття Періодичного закону;
d – протонне число елемента з таким розподілом електронів в атомі: 2, 8, 18, 32, 8, 2;
m – число металів, відомих в давнину;
n – число природних ізотопів Оксигену;
p – число елементів, відкритих П’єром і Марією Кюрі;
q – порядковий номер одного з елементів, відкритих у 1817 році.
Підказка! У відповіді ви отримаєте дуже кругле число.

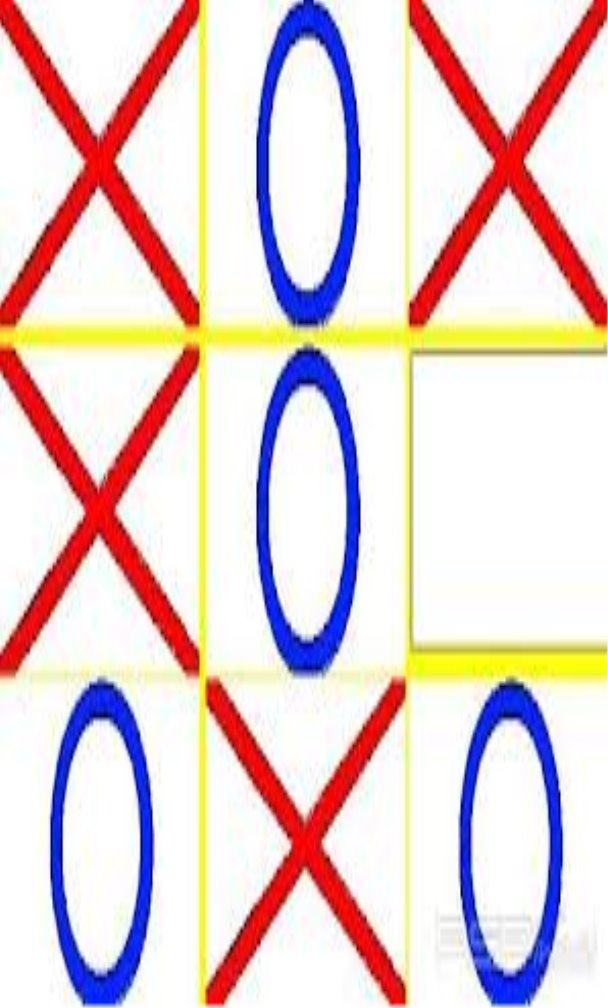
Визначити виграшні варіанти , вказати оксиди, які мають амфотерні властивості:
|
|
|
|
|
|
|
|
|
|
|
|
Вказати речовини, як належать до простих:
|
|
|
|
|
|
|
|
|
|
|
|
Вказати елементи , які належать до одного періоду :
|
|
|
|
|
|
|
|
|
|
|
|



1. Є складна речовина,
Що містить Оксиген вона.
З двох елементів складається
І як вона називається? (Оксид)
2.Гідроген дає – гідриди Оксиген дає …… (Оксиди)
3. Кислий смак в природі маю,
Й фрукти також підкисляю.
Слабкою можу бути й сильною,
І небезпечною й корисною.
4. Мене водою розбавляють:
Концентрацію знижають,
Обов’язково пам’ятай:
Мене у воду доливай!
Не роби це навпаки,
Щоб уникнути біди! (Кислота)
5. Кислота ця унікальна,
Містить Нітроген вона,
І безбарвна, і летка,
З їдким запахом вона.
Від кислот же тим відмінна,
Що сполуки всі її – Розчиняють в воді. (Нітратна)
6. Належим до сполук неорганічних,
Буваєм небезпечні і корисні.
З водою реагуєм, та не всі,
А лише ті, що розчиняються в воді.
З кислотами союз у нас міцний:
Нейтралізуєм їх, утворюючи сіль.
Як зветься наша дружная сім’я?
Хто влучно відгада її ім’я? (Основи, луги)
7. Елемент він чудодійний,
За властивістю подвійний:
З кислотою він основний,
А з основами – кислотний. (Амфотерний)
8. Належу до сполук неорганічних,
І маю в формулах своїх хімічних
Я завжди атоми металів.
З-поміж властивостей ще є такі деталі:
З металами я реагую, крім активних,
Бо люблю дуже я пасивних,
Тих, що у витискувальному ряду
Ліворуч себе я знайду.
І з лугами також я реагую,
Народжуючись потім знов на світ,
І з родичами дружно співісную,
Утворюючи з ними новий вид.
І нагрівання на сполуки розкладає
Мене, якщо я буду кисневмісна,
І хімвластивість всіх кислот згоряє,
Коли взаємодію з ними Я… Так хто ж назве моє ім’я? (Сіль)
9. Без неї не проживеш,
Її властивостям немає меж.
Життя без неї – справжній біль.
Ви знаєте її. Це – … (сіль – натрій хлорид NaCl)
10. Спочатку – вода,
Потім – кислота
Інакше станеться велика біда.
Про яке явище йдеться мова? (Рзчинення кислоти у воді)

11. Хоч не можу я горіти,
Мене треба погасити –
Буду вам добро робити».(процес – гашення вапна)
12. На картині Жуковського «Перед терасою» віднайдіть і назвіть фізичні та хімічні явиша.



Спробуйте свої сили в цій грі. Що з наведеного переліку зайве
CuSO4, CuCl2, CuS.
H2SO4, H2CO3, HNO3.
Етан, етанол, етилен.
А зараз складніші завдання .
Кристалічна сода, кухонна сіль, мідний купорос, залізний купорос, гіпс.
Олія, нітратна кислота, етиловий спирт, оцтова кислота, ацетон.
Mg, Cu, Zn, Fe, Al.





Обов’язково поясніть свій вибір. Цікаво, що варіантів відповіді може бути декілька.


ТИПИ ХІМІЧНОГО ЗВЯЗКУ
- Хімічний зв'язок – взаємодія між структурними частинками речовини .
- Відомо лише ковалентний полярний та ковалентний неполярний зв'язок .
- Йонний зв'язок – це взаємодія між молекулами речовини .
- Катіони та аніони – це йони.
- Катіон – негативно заряджений йон.
- Аніон – негативно заряджений йон
- Хімічний зв'язок утворюється за рахунок валентних електронів.
- Завершення зовнішнього енергетичного рівня може бути досягнуто приєднанням чи віддачею електронів.
- Електронегативність у періодах зі збільшенням заряду ядра атомів зменшується .
- Електронегативність у групах зі збільшенням заряду ядра атомів зменшується .
- Найбільш електронегативним є Флуор .
- Найменш електронегативним є Оксиген .
- Йонний зв'язок характерний для йонних сполук .
- У молекулі води ковалентний полярний зв'язок .
- У молекулі кисню ковалентний полярний зв'язок .
- У молекулі питної соди ковалентний полярний зв'язок .
ФЕРУМ. ЗАЛІЗО
- Ферум – неметалічний елемент_________________
- Порядковий номер Феруму – 26 ________________
- Навколо ядра атома Феруму рухається 56 електронів _________
- Ферум знаходиться в ІV групі______________
- Ферум знаходиться в 4 періоді_____________
- Відносна атомна маса Феруму – 56 _________
- Проста речовина, утворена елементом ферумом, називається залізом ____
- Сполуки Оксисену з Ферумом – це оксиди феруму _________
- Fе2О3 – це ферум(ІІ) оксид _________
- Залізо має здатність намагнічуватись _______________
- Залізо – малопластичний метал ___________________
- Залізо має жовто – червоне забарвлення _____________
- Залізо легше за воду ___________
- Температура плавлення заліза 1539 0С _____

ЯВИЩА. ВЛАСТИВОСТІ РЕЧОВИН
- Зміна агрегатного стану – фізичне явище
- Спостерігати можна тільки хімічні явища
- Колір і прозорість – це хімічна властивість
- Експеримент можна проводити без нагляду
- Закони природи постійно змінюються
- Кожній речовині притаманні індивідуальні властивості
- Під час хімічних реакцій утворюються нові речовини
- Під час фізичних явищ утворюються нові речовини
- Метали практично не розчиняються у воді
- Мідний купорос блакитного кольору



1.Якби я був директором металургійного комплексу…
Уявіть. що кожен з вас – директор якогось металургійного підприємства. Що б ви зробили як директор, щоб добитися більшої ефективності в роботі галузі? Свої пропозиції аргументуйте.
2. Уяви собі, що ти – Робінзон, який опинився на безлюдному острові. Лише жага до життя штовхає вперед. Пофантазуй щодо подальших дій з урахуванням сучасних знань з хімії та біології. Описані тобою явища поясни і підтвердь рівняннями реакцій.
3. Уяви собі, що ти – офіцер війська Олександра Македонського. Тяжкий поход в Індію…Хвороби на шлунково-кишкові захворювання, нестача їжі, води. Твоє взуття стало непридатним. Не сподівайся на щасливий випадок у вигляді каравану з різним скарбом та ліками. Пофантазуй щодо цього, використовуючи знання з хімії та біології. Підтвердь умовиводи формулами, рівняннями реакцій.
4. Ви – співробітники журналу «Велике прання». До вас завітав режисер фільму «Чистота вредит здоровью?!» і запросив на прем`єру. Підготуйте питання до прес – конференції з режисером. Чи можна приготувати мило або інші СМЗ в домашніх умовах? Які речовини треба взяти? Складіть рівняння відповідних реакцій.
5. Уяви собі, що ти – Робінзон, який опинився на безлюдному острові. Лише жага до життя штовхає вперед. Пофантазуй щодо подальших дій з
урахуванням сучасних знань з хімії та біології. Описані тобою явища поясни і підтвердь рівняннями реакцій.
5. Лісництво міста Камінь - Каширський висуває директору комунального господарства вимогу переобладнати міський смітник, що своїм місцем розташування отруює навколишнє середовище. Директор комунальних підприємств у свою чергу висуває претензії до підприємства, що викидає промислові відходи. Обіграти ситуацію. Яких заходів ви б ужили, якби були: а) лісником; б) директором комунальних підприємств; в) директором промислового пыдприэмства?
6. Інспектор з рибного нагляду висуває вимоги до працівників залізниці у зв`язку з появою нафтових плям на поверхні озер, що привело до масової загибелі мальків? Обіграти ситуацію. Яких заходів ви б ужили, якби були: а) інспектором рибнадзору; б) рибалкою; в) начальником локомотивного депо?
7.Згідно з дослідженнями членів екологічного гуртка ЗОШ села Нуйно, загальна кількість автомобілів, що проїжджають за добу по вулиці Лесі Українки, що поблизу школи, складає 519. При цьому на 1 км. шляху вони витрачають приблизно 210 л бензину, збагачено Плюмбумом (до 0,36 г/л). Яка кількість Плюмбуму потрапляє за добу в атмосферу міста разом з відпрацьованими газами автомобілів? Як впливають сполуки Плюмбуму на організм людини?
8. Уявіть, що ви - працівник рекламного агентства. Вам доручили написати слогани до картинок, з зображенням товарів, виробництво яких пов’язано з застосуванням гліцерину.
Придумайте цікаві слогани, або прорекламуйте те, що зображено на картинках. Пам’ятайте, ми вивчаємо гліцерин та його властивості! Врахуйте це при підготовці реклами.

Жила-була Вода, і одного разу надумала вона зробити Природу красивою. Вода вирішила відправитися по світу і поспостерігати за Природою. Вона перетворилася на маленький Струмочок і потекла по Землі. З часом Струмочок ставав все ширше і ширше, все більше і сильніше. Незабаром Струмочок перетворився на Річку і потік не швидко, як струмок, а повільно і важливо, як тече справжня річка.
Раптом яскраво засвітило Сонце, Річка висохла і стала Паром. Пар піднявся високо-високо і запитав у Сонця:
- Сонце, навіщо ти мене висушило?
Сонце і відповідає:
- Не бійся, я допоможу тобі зробити всім добро!
Пар запитує:
- Сонце, скажи, як мені зробити Природу красивою?
Сонце посміхнулося і відповіло:
- Ти сам здогадайся, а я тільки підкажу. Рослинам і деревам потрібний дощ!
Пар вигукнув:
- Точно! Спасибі тобі, Сонце!
І обернулася Пара дощиком. Полив він все навколо і милується: всі дерева, і кущі знову зацвіли, птахи заспівали свої веселі пісеньки, навіть в пустелях з'явилися оази. Всі люди і тварини радісно закричали:
- Спасибі тобі, Дощик!
А Дощик зібрався знову в дзвінкий Струмочок і потік, весело побіг по землі. Йому було дуже радісно і приємно, що він зробив щось хороше для матінки-Природи. Струмочок був дуже задоволений. Далі він побіг очищати Моря і Океани від солі.
Струмочок дістався до Моря і крикнув йому:
- Здрастуй, Море!
Море відповіло:
- Привіт, дзвінкий Струмочок! Чого ти хочеш?
Струмочок сказав:
-Можна взяти в тебе трохи солі в їжу людям?
Море задумалося:
- Гаразд, Струмочок, ось тобі моя сіль. Використовуй її, як хочеш.
Струмочок обрадувано відповів:
- Так, добре! Спасибі тобі, Море!
Вони попрощалися, і Струмочок віддав сіль в їжу людям, щоб вони були здоровими, а потім прийняв свій первісний вигляд.
Вода звернулася до Природи і сказала:
- Природа, я зробила тебе красивою, я зробила людей здоровими, я допомогла Морю позбутися зайвої солі. Я виконала своє призначення.
Природа відповідає:
- Спасибі тобі, Вода, я тобі дуже вдячна!
На тому й розійшлися. Вода, виконавши своє призначення, повернулася до себе додому і почала спокійно жити і робити добро всьому світу.

КАЗКА ПРО АТОМИ
Десь у світі живуть собі атоми. Живуть та й живуть. І ніби все в них є, немає тільки відчуття гармонії, стабільності. Ви, може, ще й не знаєте, але все в цьому світі прагне досконалості.
Для атомів такою досконалістю є заповнена зовнішня електронна оболонка, тобто кожен атом на зовнішньому рівні прагне мати вісім діток-електронів, як будь-який поважаючий себе інертний газ.
Такий октет є стабільним, він дозволяє атому почувати себе захищеним.
І от.
В одному будиночку живе атом Натрію. Ви, може, думаєте, що він задоволений своїм життям? Але ж уявіть, що десь там, на зовнішній оболонці у нього живе одна дитина – один електрон на зовнішньому рівні (перша група елементів). Цей електрон заважає атому Натрію відчувати себе впевнено і атом прагне його позбутися – віддати на усиновлення, може, комусь знадобиться більше, ніж йому. А електрон і радий старатися, все одно, з батьком-Натрієм його зв’язують не такі вже й сильні зв’язки.
І іде електрон шукати собі нову родину. Уявіть, що знаходить! Бо десь, в іншій хатці живе, скажімо, атом Хлору. У нього сім дітей і до повного задоволення Хлору не вистачає тільки однієї дитини. Він радо приймає приблуду на свій зовнішній енергетичний рівень, отримуючи омріяний октет електронів: Хлору добре і електронам затишно.
Тут варто закінчити, напевно, словами: «і жили вони всі довго і щасливо», адже всі задоволені, але щось змінилося…
Давайте подумаємо, що отримав кожен атом при таких блуканнях електрона.
Атом Натрію – електронейтральна частинка, тобто має заряд 0. Якщо він втрачає один електрон (електрон несе заряд мінус, значить атом втрачає мінус 0-(-1)=+1). Отже, процес такий:Na![]() – 1e=Na
– 1e=Na![]() +, в хімії такий процес називається окисненням – віддачею електрона.
+, в хімії такий процес називається окисненням – віддачею електрона.
Хлор навпаки, отримує на свою зовнішню оболонку один мінусовий заряд, значить, сам набуває заряду: 0+(-1)=-1 Cl![]() +1e=Cl-, цей процес називається відновленням – процесом прийому електронів.
+1e=Cl-, цей процес називається відновленням – процесом прийому електронів.
СПИСОК ВИКОРИСТАНОЇ ЛІТЕРАТУРИ
1. Исаев С.Д. Об использовании дидактических игр.// Химия в школе.//Химия в школе №6, 2002, С.50.
2. Степин Б.Д., Аликберова Л.Ю. Занимательные задания и эффективные опыты по химии.-М.: “Дрофа”.2002 год.
3. Туринська Н.М., Величко Л.П. Б 91 Хімія, 10 кл.: Підручник для серед. загальноосвітніх шк. - Київ; Ірпінь: ВТФ “Перун”, 2000. - 176 с.
4. Царьова Ніна Ц Неорганічна хімія. Дидактичні матеріали для 8-10 класів. - Тернопіль: Підручники і посібники, 2000. - 104 с. Гольдфарб Я.Л. та ін.
5. Шабаршин В.М. Проектирование и организация химико-педагогических игр на основе принципа интеграции субкультур / Фестиваль педагогических идей «Открытый урок». Cб. тезисов. 2003-2004 учебн. год. М.: ООО «Изд-во «Первое сентября», ООО «Чистые пруды», 2004. - С. 345.




-1 -


про публікацію авторської розробки
Додати розробку