Зошит для навчальних досліджень з хімії 7 клас
 НОВА УКРАЇНСЬКА ШКОЛА
НОВА УКРАЇНСЬКА ШКОЛА
Зошит для навчальних досліджень
уч ___________7 класу
Автор Денисюк Юлія Іванівна
Правила поведінки в кабінеті хімії
1. Заходити до кабінету хімії можна лише з дозволу вчителя.
2. Рухатися в кабінеті потрібно спокійно, щоб випадково не перевернути хімічний посуд, устаткування або реактиви, що знаходяться на столі.
3. Підтримуйте порядок на своєму робочому місці.
4. Під час роботи на столі не повинно бути нічого зайвого. На ньому можуть бути підручник, зошит, письмове приладдя, довідник. Працюйте швидко, але без зайвого поспіху, під час роботи зберігайте тишу.
6. Виконуйте лише ті хімічні досліди, які погоджені з учителем/ учителькою.
7. Починайте роботу після перевірки обладнання, посуду та реактивів, необхідних для виконання дослідів. Без указівки вчителя/вчительки не змішуйте невідомі речовини.
8. Дотримуйтеся правил поводження з реактивами, хімічним посудом, лабораторним обладнанням.
9. Після роботи приберіть своє робоче місце та обов’язково ретельно вимийте руки.
Правила поведінки під час виконання хімічного експерименту
1. Під час нагрівання розчинів у пробірці користуйтеся спеціальним тримачем.
2. Жодних речовин не пробуйте на смак!!!
3. Уважно читайте етикетку на банці з речовиною, яка береться для досліду.
4. Реактивів для дослідів беріть у кількостях, які вказані в інструкції.
5. Залишок узятого реактиву не можна зливати (зсипати) назад у посудину, де він зберігався. Його слід зливати (зсипати) в окрему банку чи посудину для зливу.
6. Під час наливання рідин посудину з реактивом беріть так, щоб
етикетка була направлена в бік долоні, правильно знімайте краплю з краю шийки посудини, інакше рідина стікатиме по склу, псуватиме етикетку та може пошкодити шкіру рук.
7. Посудину, з якої узяли реактив, відразу ж слід закрити корком і поставити на місце.
8. Не заглядайте в пробірку, у якій нагрівається рідина, і не нахиляйтеся над посудиною, у яку наливають рідину, тому що найдрібніші краплі можуть попасти в око.
9. Нюхайте всі речовини обережно, не нахиляйтеся над пробіркою і не вдихайте на повні груди, а направляйте до себе пару або газ помахом руки.
10. Працюйте з розчинами кислот і лугів обережно. Особливо бережіть очі.
11. У разі потрапляння розчину лугу або кислоти на руки негайно змийте уражене місце великою кількістю протічної води та обробіть його нейтралізуючим розчином (2% розчином оцтової кислоти або 2% розчином соди відповідно).

Навчальне дослідження 1. Виконання найпростіших операцій із лабораторним обладнанням: наливання рідини в пробірку та перемішування. Нагрівання речовин у пробірках і порцелянових чашах.
Мета: ознайомитись з лабораторним посудом, вивчити правила техніки безпеки під час користування лабораторним обладнанням, виконати найпростіші операції.
Обладнання та реактиви: лабораторний штатив, спиртівка, штатив із пробірками, сірники, вода, хімічна склянка, порцелянова чашка, лійка, колби, газовідвідна трубка, металева ложечка, шпатель, скляна паличка, кухонна сіль.
ХІД РОБОТИ
- Повторення правил техніки безпеки під час роботи з хімічним лабораторним обладнанням.
- Вивчення лабораторного обладнання, його призначення. Заповнити таблицю.
Заповнити таблицю:
|
Лабораторний посуд |
Назва |
Призначення |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
- Вивчення будови лабораторного штативу. Підпишіть складові частини лабораторного штативу.
![]()
![]()
![]()
![]()
![]()

- Вивчення будови спиртівки. Підписати деталі спиртівки.
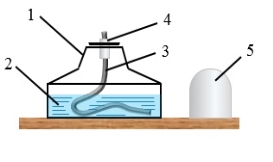 1.___________________________
1.___________________________
2. ___________________________
3. ___________________________
4.____________________________
5.____________________________
5. Вивчення будови полум’я . Заповніть спиртівку спиртом не менше, ніж на дві третини свого об’єму. У спирт занурте гніт. Саме через нього спирт буде підійматися вгору, де утворюватиме легкозаймисті пари. Дотримуючись правил роботи з пальником, за допомогою сірника запаліть ґніт. Розгляньте полум’я та пригадайте його будову.
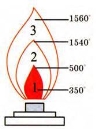
1.___________________________
2. ___________________________
3. ___________________________
|
6. Вивчення перемішування речовин. У видану вам посудину (склянку, колбу чи пробірку) з водою внесіть шпателем трішки кухонної солі та добре перемішайте суміш оптимальним для цього способом. Що спостерігаєте ? ________________________________________________________________________________________________________________________________________ |
|
|
7. Ознайомлення з процесом нагрівання. а) Перелийте в пробірку 3-5 мл розчину з першого завдання, закріпіть пробірку в тримачі ближче до отвору. Прогрійте пробірку в полум’ї пальника та, дотримуючись усіх правил безпеки, нагрійте розчин. Перед початком закипання розчину припиніть нагрівання та загасіть спиртівку.
б) Закріпіть порцелянову чашу в кільце штатива. Перелийте в неї 3-5 мл розчину з першого завдання. Нагрійте розчин, дотримуючись усіх правил безпеки.
Висновок:
|

Оцінка :
Навчальне дослідження 2. Моделювання: створення газометра власноруч. Вимірювання маси твердих і рідких речовин, об’ємів твердих, рідких і газуватих речовин, збирання газів у газометр (лабораторний або сконструйований власноруч).
Мета: ознайомитись з будовою газометра, повторити правила техніки безпеки під час користування лабораторним обладнанням, навчитись визначати масу, об’єм, густину речовини, збирати гази у газометр, виконати найпростіші операції.
Обладнання та реактиви: терези або електронні ваги, зразки вати, воску, пластиліну, металеві предмети (цвях, ключ, мідний дріт ); мірний циліндр, вода.
ХІД РОБОТИ
- Повторення правил техніки безпеки під час роботи з хімічним лабораторним обладнанням.
- Вивчення будови газометра.
![]()
![]()
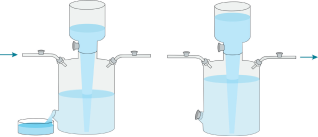
![]() Газометр для зберігання й використання газів у лабораторії:
Газометр для зберігання й використання газів у лабораторії:
![]()
![]() а — наповнення газометру газом методом витіснення води;
а — наповнення газометру газом методом витіснення води;
б — використання зібраного газу
- Моделювання газометра власноруч.

- Зважування твердих тіл. Дотримуючись правил зважування, зважте по 1 г зразків вати, воску, пластиліну.
Для визначення об’єму зразків використайте мірний циліндр. Налийте у мірний циліндр 10мл води і по черзі опустіть зразки твердих тіл. Визначте ціну поділки мірного циліндра після того, як опустили у воду зразок твердого тіла. Результати запишіть у таблицю.
|
Маса вати (г) |
Об’єм вати (см3) |
Маса воску (г) |
Об’єм воску (см3) |
Маса пластиліну (г) |
Об’єм пластиліну (см3) |
|
|
|
|
|
|
|
Порівняйте об’єми даних зразків. Зробіть висновки. _____________________________________________________________________________________________________________________________________________________________________________________________
- Визначення густини.
Густина - фізична величина, яка дорівнює відношенню маси речовини до її об'єму.
ρ = m / V , де m — маса, V — об'єм.
Основною одиницею густини речовини є г/ см 3.
Дослідіть густину металевих фізичних тіл (цвяха, ключа, мідного дроту тощо).
- За допомогою електронної ваги визначте масу досліджуваного цвяха, ключа і мідного дроту.
- Визначте об’єми досліджуваних тіл.
- Визначте густину досліджуваних тіл.
Результати дослідження та розрахунків представте у вигляді
таблиці.
|
Маса цвяха (г) |
Об’єм цвяха (см 3) |
Густина цвяха (г/ см 3) |
Маса ключа (г) |
Об’єм ключа (см 3) |
Густина ключа (г/ см 3) |
Маса дроту (г) |
Об’єм дроту (см 3) |
Густина дроту (г/ см 3) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
 Використовуючи довідники, за отриманими значеннями густин, зробіть висновок, із яких металів можуть бути виготовлені досліджувані фізичні тіла. __________________________________________________________________________________________________________________________________
Використовуючи довідники, за отриманими значеннями густин, зробіть висновок, із яких металів можуть бути виготовлені досліджувані фізичні тіла. __________________________________________________________________________________________________________________________________
Оцінка :
Навчальне дослідження 3. Моделювання «Будова атомів хімічних елементів» (створення 2D- і 3D-моделей).
Мета: поглибити знання про будову атома, навчитись створювати 2D- і 3D-моделі.
Обладнання та реактиви: пластилін,
ХІД РОБОТИ
- Повторення правил техніки безпеки під час роботи у кабінеті хімії.
- Вивчення будови атома.
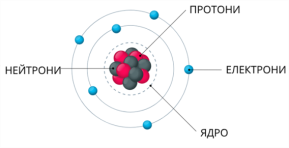
Продовжити речення:
- Атом - це _____________________________________________________________________ .
- Протони – це ________________________________________________.
- Електрони – це ______________________________________________.
- Нейтрони – це _______________________________________________.
- Ядро складається з ___________________________________________ .
- Поняття про 2D і 3D моделі .
- Розгляньте приклади 2D моделей:
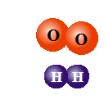
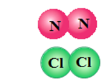
- Розгляньте приклади 3D моделей:

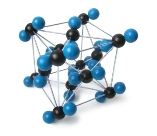
!!! 2D створює зображення двовимірне, а 3D — тривимірне
- Створення 2D і 3D моделей.
Завдання : Створити моделі за малюнком.
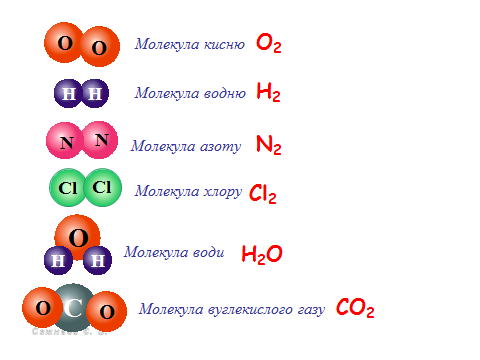
Візьміть різного кольору пластилін. Зробіть з нього кульки. Уявіть, що червоні — атоми Оксигену, сині — атоми Гідрогену, чорні — атоми Карбону, зелені – атоми Хлору, рожеві – атоми Нітрогену.
Атоми мають властивість сполучатися між собою. З'єднайте їх так, щоб
отримати моделі молекул кисню, водню, азотк, хлору, води, вуглекислого газу.
Визначіть, які моделі є 2D, а які 3D. Заповніть таблицю
|
2D моделі |
3D моделі |
|
|
|
|
|
|
Висновок:
Закінчіть речення:
- Найменшою неподільною частинкою речовини є ____________ .
- Атом складається з ______________________________________ .
- Атом — електронейтральний, тобто _______________________________________________________.
-
 Масштабні моделі дають уявлення про просторове розміщення ________ у молекулі речовини.
Масштабні моделі дають уявлення про просторове розміщення ________ у молекулі речовини.
Оцінка:
Навчальне дослідження 4. Порівняння фізичних властивостей металів і неметалів.
Мета: поглибити знання про фізичні властивості речовин, порівняти фізичні властивості металів і неметалів, встановити спільні і відмінні ознаки.
Обладнання та реактиви: зразки речовин: мідь, залізо, сірка, алюміній, графіт, активоване вугілля, хімічний стакан, вода.
ХІД РОБОТИ
- Повторення правил техніки безпеки під час роботи у кабінеті хімії.
2.Поняття про фізичні властивості речовин.
Фізичні властивості речовин - це ті характеристики, які можна спостерігати та виміряти без зміни хімічного складу речовини.
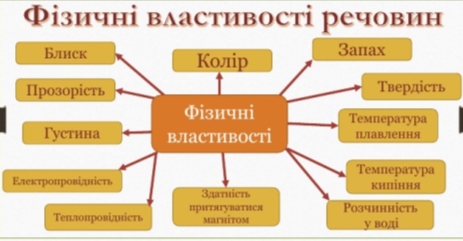
Гіпотеза: Фізичні властивості металів і неметалів відрізняються.
- Вивчення фізичних властивостей металів.
Розгляньте видані вам зразки металів. Проведіть відповідне дослідження. Заповніть таблицю
|
Фізичні властивості |
Алюміній |
Залізо |
Мідь |
|
Агрегатний стан |
|
|
|
|
Колір |
|
|
|
|
Блиск |
|
|
|
|
Розчинність у воді |
|
|
|
4.Вивчення фізичних властивостей неметалів.
Розгляньте видані вам зразки неметалів. Проведіть відповідне дослідження. Заповніть таблицю
|
Фізичні властивості |
Сірка |
Графіт |
Активоване вугілля |
|
Агрегатний стан |
|
|
|
|
Колір |
|
|
|
|
Блиск |
|
|
|
|
Розчинність у воді |
|
|
|
- Порівняння фізичних властивостей металів і неметалів

 Укажіть подібні та відмінні властивості досліджених речовин. Заповніть діаграму Венна, яка ілюструє властивості металів і неметалів.
Укажіть подібні та відмінні властивості досліджених речовин. Заповніть діаграму Венна, яка ілюструє властивості металів і неметалів.
Властивості металів Властивості неметалів
![]()
Спільне
Підтверджено чи спростовано вашу гіпотезу? __________________________________________________________________________________________________________________________________
Висновок:
Дайте відповіді на запитання:
- Чим відрізняються метали від неметалів? ______________________________________________________________
- Які властивості характерні для металів? ______________________________________________________________
- Які властивості характерні для неметалів?
______________________________________________________________

Оцінка:
Навчальне дослідження 5. Визначення фізичних властивостей речовин (пластичність, крихкість / твердість, електропровідність, колір, температура кипіння / плавлення).
Мета: ознайомитись з фізичними властивостями речовин,
Обладнання та реактиви: чашки Петрі, пробірки, дистильована вода, пінцет, шпатель, скляна паличка, графітовий стержень, алюмінієва, мідна та залізна пластинки, кухонна сіль.
ХІД РОБОТИ
- Повторення правил техніки безпеки під час роботи з хімічним лабораторним обладнанням.
- Ознайомлення з фізичними властивостями речовин.
Проведіть відповідні дослідження і заповніть таблицю.
|
Фізичні властивості |
Графітовий стержень |
Алюмінієва пластинка |
Мідна пластинка |
Залізна пластинка |
Кухонна сіль |
|
Колір |
|
|
|
|
|
|
Блиск |
|
|
|
|
|
|
Запах |
|
|
|
|
|
|
Розчинність у воді |
|
|
|
|
|
|
Твердість |
|
|
|
|
|
|
Пластичність |
|
|
|
|
|
3. Дослідження теплопровідності та електропровідності
1) Виберіть із запропонованих матеріалів зразки для дослідження.
_______________________________________________________________
2) Сформулюйте гіпотезу, складіть план експерименту та спрогнозуйте його результати.
Гіпотеза:______________________________________________________________________________________________________________________
План експерименту:
_____________________________________________________________________________________________________________________________________________________________________________________________
Прогнозовані результати: ______________________________________________________________________________________________________________________________
- Ознайомтеся з порядком виконання експерименту та дослідіть зразки.

Дослідження теплопровідності: тримаючи один кінець дослід-
жуваного зразка, інший занурте в гарячу воду.
Зробіть висновки. ______________________________________________________________________________________________________________________________ !!! Дотримуючись правил безпеки, не торкайтеся гарячої води.
Покладіть досліджуваний зразок на тильний бік долоні. 
Дослідіть кожен зразок тильною поверхнею руки. Якщо ви не відчуваєте
холоду, речовина є поганим провідником тепла.
Зробіть висновки.
______________________________________________________________________________________________________________________________
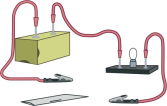 Дослідження електропровідності: Складіть електрик не коло, як показано на малюнку.
Дослідження електропровідності: Складіть електрик не коло, як показано на малюнку.
Підключіть затискачі типу «крокодил» до обох кінців
досліджуваного зразка. Замкніть коло. Якщо
лампочка світиться, то речовина проводить
електричний струм. Дотримуючись правил безпеки,
не торкайтеся схеми мокрими руками.
Уважно розгляньте дані таблиці 13.1. (підручник Л.Мідак, 2024, с.115)
- Які речовини (метали чи неметали) мають високі температури плавлення та кипіння?
_____________________________________________________________
- Для речовин атомної чи молекулярної будови характерні вищі температури плавлення та кипіння? _____________________________________________________________
Довідка!
У речовинах атомної будови всі атоми міцно сполучені між собою. Характерні фізичні властивості таких речовин — високі температури плавлення і кипіння. Вони не розчиняються у воді, мають високу твердість.
Речовини молекулярної будови мають невисоку твердість, низькі температури плавлення і кипіння, а деякі — запах. Молекулярні речовини не проводять електричний струм.
- За результатами спостережень заповніть таблицю.
|
|
Алюміній |
Мідь |
Графіт |
|
агрегатний стан |
|
|
|
|
колір |
|
|
|
|
блиск |
|
|
|
|
запах |
|
|
|
|
розчинність у воді |
|
|
|
|
твердість |
|
|
|
|
пластичність |
|
|
|
|
електропровідність |
|
|
|
|
теплопровідність |
|
|
|
|
агрегатний стан |
|
|
|
- Укажіть подібні та відмінні властивості досліджуваних речовин.
_______________________________________________________________________________________________________________________________________________________________________________________
- Поміркуйте, чи можливо дати характеристику рідинам за
всіма переліченими фізичними властивостями. Відповідь обґрунтуйте. ____________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
|
5. Дослідження розчинності. |
|
Розчинність — здатність речовин розчинятися в інших речовинах. 1) Наведіть приклади розчинних у воді речовин. _______________________________________________________________ 2) Якими способами можна підвищити розчинність речовин? _______________________________________________________________3) Сформулюйте гіпотезу _______________________________________________________________ |
- Проведіть спостереження за розчинністю цукру, крейди та кухонної солі у воді. Результати занесіть у таблицю.
|
Етапи експерименту |
Спостереження |
Висновок |
|
|
|
|
|
|
|
|
|
|
|
|
6.Дослідження агрегатного стану.
1) Танення льоду.
Для роботи нам потрібні кубики льоду, секундомір або таймер, пластиковий ZIP-пакет.
Сформулюйте мету дослідження: ______________________________________________________________
Сформулюйте гіпотезу: ______________________________________________________________
Ознайомтеся з методикою виконання експерименту та спрогнозуйте його результати.
а) Швидко помістіть один кубик льоду в поліетиленовий ZIP-пакет і закрийте його.
б) Потримайте ZIP-пакет у руках (за верхній його край, не торкаючись льоду). Виміряйте час, протягом якого кубик льоду повністю розтане.
в) Запишіть свої спостереження. ____________________________________________________________________________________________________________________________
Висновок:
- Речовини характеризуються такими фізичними властивостями: ____________________________________________________________________________________________________________________________
- Фізичні властивості для одного агрегатного стану речовини можуть бути (однакові, різні) _______________.
- Щоб дослідити теплопровідність потрібно один кінець досліджуваного зразка тримати рукою, а інший занурити в _________ воду.
- Щоб дослідити електропровідність потрібно ______________ електричне коло.

Оцінка :
Навчальне дослідження 6.
Розділення сумішей фільтруванням і хроматографією (на папері), відстоюванням (із використанням ділильної лійки).
Мета: поглибити знання про хроматографію, способи розділення сумішей, провести відповідні дослідження.
Обладнання та реактиви: фломастери (3 шт.), фільтрувальний папір (3 арк.), чашки Петрі (3 шт.), шматочки порожнього картриджа фломастера (3 шт.), спирт, піпетка.
ХІД РОБОТИ
- Повторення правил техніки безпеки під час роботи у кабінеті хімії.
- Поняття про хроматографію.
Хроматографія — це фізико-хімічний метод розділення та аналізу сумішей.
Хроматографічними методами можна розділити суміші рідин і газуватих речовин.
Чорнило — це чиста речовина чи суміш речовин? __________________ Які речовини зумовлюють колір чорнила фломастера? ______________
Сформулюйте гіпотезу: _______________________________________________________________.
- Дослідження хроматографії .
- Візьміть три невеликі аркуші фільтрувального паперу круглої форми, три чашки Петрі (фільтрувальний папір повинен вміщатися в чашку Петрі) і декілька шматочків порожнього картиджа фломастера.
2) У центрі кожного аркуша фільтрувального паперу намалюйте фломастерами коло, діаметром приблизно 5–7 мм. Покладіть аркуші фільтрувального паперу зі зразками чорнила різних кольорів у різні чашки Петрі.
3) На чорнилі розмістіть шматочки порожнього картриджа фломастера та змочіть його спиртом із використанням піпетки.
4) Спостерігайте за рухом лінії фронту та за змінами, що відбуваються під час хроматографії. Проаналізуйте, що у вашому досліді буде рухомою фазою, а що — нерухомою?
______________________________________________________________________________________________________________________________Зупиніть експеримент (заберіть шматки картриджів і вийміть хроматограми з чашок Петрі) тоді, коли лінія фарби буде на відстані приблизно 1-1,5 см від краю паперу. Висушіть отримані хроматограми на
повітрі.
5. Уважно розгляньте хроматограми. Які кольори ви побачи-
ли на папері?
_______________________________________________________________
- Дослідження відстоювання речовин.
- Змішайте в склянці олію з водою. Розгляньте одержану суміш. Опишіть її властивості. Поміркуйте, як можна розділити дану суміш. Сформулюйте гіпотезу: ____________________________________________________________
-
Розгляньте ділильну лійку та закріпіть її в штативі (як показано на мал.
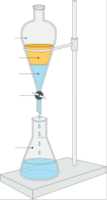 ).
).
- Розмістіть конічну колбу під лійкою.
- Перелийте досліджувану суміш у лійку та залишіть її в спокої на деякий час. Знову розгляньте суміш. Що ви помітили? _______________________________________________
- Обережно відкрийте кран і злийте нижній шар суміші в конічну колбу, після чого перекрийте кран. Який компонент суміші залишився в лійці? ____________________Чому? __________________________________
- Чи вдалося розділити суміш олії з водою? _______________________
- Проаналізуйте причини невдач, якщо вони були. ____________________________________________________________
Висновок:
- Хроматографія — метод розділення, аналізу і дослідження сумішей речовин, що ґрунтується на різному розподілі речовин в динамічних умовах між ____________ і __________ фазами.
- Для розділення суміші рідин використовують _________________________________.
- Відстоювання -це _________________________________________________________.

Оцінка:
Навчальне дослідження 7. Математичне моделювання: створення алгоритму обчислення мас, об’ємів і масових часток компонентів у сумішах
Мета: навчитись розділяти речовини способом фільтрування і випарювання, провести розрахунки визначення масових часток компонентів суміші.
Обладнання та реактиви: суміш піску із сіллю, терези, хімічні склянки, мірний циліндр, випарна порцелянова чашка, скляна паличка з гумовим наконечником, ложечка, фільтрувальний папір, лійка, штатив, пальник, вода.
ХІД РОБОТИ
- Повторення правил техніки безпеки під час роботи з хімічним лабораторним обладнанням.
- Приготування суміші піску і солі.
- Насипте у хімічну склянку 2 г піску і 2г кухонної солі.
- За допомогою скляної палички перемішайте дані речовини.
- Розчинення суміші у воді.
Відміряйте мірним циліндром 10 мл води і перелийте у хімічну склянку із сумішшю.
- Дослідження способу фільтрування.
-
Підготувати фільтрувальний папір, як показано на малюнку.

- Лійку закріпіть у кільці штатива, а її кінець опустіть у чисту склянку. Перемішайте скляною паличкою суміш у склянці. Каламутний розчин невеликими порціями вилийте на фільтр.
Що спостерігаєте? ___________________________________________________________
- Дослідження способу випарювання.
-
 Налийте розчин зі склянки у випарну порцелянову чашку
Налийте розчин зі склянки у випарну порцелянову чашку
не більше ніж на 1/3 її об’єму.
- Поставте випарну чашку на кільце лабораторного штатива
та обережно нагрівайте її вміст над водяною банею до
початку утворення кристалів, періодично помішуючи.
- Припиніть нагрівання, коли води залишиться мало. Продовжуйте помішування, поки вода повністю не випарується.
4). Порівняйте отримані компоненти суміші з вихідною сумішшю.
___________________________________________________________
- Визначення масової частки компонентів суміші.
- Зважте компоненти суміші.
m(піску) = _______г
m(кухонної солі)= _______г
Дано: Розв’язання:
![]() m(піску) = …..г
m(піску) = …..г
![]()
![]() m(кухонної солі)= ….г
m(кухонної солі)= ….г
W(піску) -?
W(кухонної солі)-?
Відповідь: ____________________________________________________
Висновок:
- Для обчислення масової частки розчиненої речовини в розчині потрібно використати формулу: ________________________.
- Розчинник — це ________________________________________________.
- Маса розчину — це _____________________________________________.
- Фільтрування – це _______________________________________________________________ .
- Випарювання – це _______________________________________________.

Оцінка:
Навчальне дослідження 8. Розпізнавання фізичних і хімічних явищ (на основі власних спостережень, за відеофрагментами, світлинами, ілюстраціями природних явищ і технологічних процесів).
Мета: навчитися розрізняти за характерними ознаками хімічні та фізичні явища, закріпити на практиці поняття хімічної реакції та фізичного явища; вдосконалювати вміння працювати з хімічними речовинами та лабораторним обладнанням.
Обладнання та реактиви: штатив, тигельні щипці, пробіркотримач, спиртівка, хімічні склянки, мідний дріт , парафін, свічка, вода, оцет, сода.
ХІД РОБОТИ
- Повторення правил техніки безпеки під час роботи з хімічним лабораторним обладнанням.
- Дослідження плавлення парафіну
- Поклади шматочок парафіну у пробірку.
- Закріпи пробірку у штативі та обережно нагрій у полум’ї спиртівки.
Що спостерігаєте? _____________________________________________
Яке явище спостерігали? ________________________________________
- Дослідження горіння свічки.
1) Запали свічку, дотримуючись правил техніки безпеки.
2) Деякий час спостерігай процес горіння.
Що спостерігаєте? _____________________________________________
Яке явище спостерігали? ________________________________________
- Дослідження взаємодії соди з оцтом.
- Візьми дві хімічні склянки.
- У першу склянку налий воду, в другу — оцет.
- Додай до кожної склянки трохи питної соди.
Що спостерігаєте? _____________________________________________
Які явища спостерігали? _______________________________________
- Дослідження прожарювання мідного дроту.
1) Запали спиртівку, дотримуючись правил техніки безпеки.
2) За допомогою тигельних щипців внеси у полум’я спиртівки мідний дріт і потримай близько 1 хвилини.
Що спостерігаєте? _____________________________________________
Яке явище спостерігали? ________________________________________
- Заповніть таблицю, розподіливши у ній явища, які досліджували.
|
Фізичні явища |
Хімічні явища |
|
|
|
|
|
|
|
|
|
Висновок:
1. Під час фізичних явищ _____________________________________________
___________________________________________________________________.
2.Під час хімічних явищ _______________________________________________
____________________________________________________________________
3. Хімічні явища можна відрізнити від фізичних за ________________________
____________________________________________________________________

Оцінка:
Навчальне дослідження 9. Моделювання виверження вулкана з використанням соди, оцту та барвника.
Мета: поглиблювати навички проведення лабораторних дослідів, закріпити вміння працювати з лабораторним посудом, дослідити деякі ознаки хімічних реакцій.
Обладнання та реактиви: лимонна кислота, сода, барвник, корок від пляшки, пластилін, вода, рідке мило, тарілка.
ХІД РОБОТИ
- Повторення правил техніки безпеки під час роботи з хімічним лабораторним обладнанням.
- Моделювання виверження вулкану.
- Змішайте лимонну кислоту, соду та барвник.
- На тарілку покладіть корок від пластикової пляшки та обліпіть його пластиліном.
- Надайте пластиліну форму вулкана.
- Усередину пластилінової моделі вулкана насипте зроблену вами суміш.
- У склянці змішайте 2 мл води з рідким милом.
- Налийте мильну воду всередину вулкану.
- Спостерігайте за явищем, що відбувається.
-
 Намалюйте світлину, яку спостерігали
Намалюйте світлину, яку спостерігали
Висновок:
- Оцет - це кислота. Сода - це луг.
- Вони вступають в інтенсивну реакцію, в результаті якої _____________ вуглекислий газ.
- Так як гази займають більше місця, ніж тверді тіла і рідини, суміш починає пузиритися і витікати з пляшки, тобто відбувається _______________________, той же процес, що при виверженні вулканів.
- Провівши даний дослід ми побачили, як ____________________________ вулкану.

Оцінка:
1


про публікацію авторської розробки
Додати розробку







-

Євсєєва Анжела Сергіївна
05.11.2025 в 09:40
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Крупа Наталія Іванівна
30.08.2025 в 13:05
Дякую!
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Гурєєва Ольга В'ячеславівна
25.03.2025 в 15:14
Дякую! Це колосальна праця! Обов'язково із задоволенням і вдячністю використаю у своїй роботі.
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Стремедловська Раїса Іванівна
19.03.2025 в 20:28
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Фертак Наталя Володимирівна
11.03.2025 в 22:00
Дякую
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Сердюк Наталія Василівна
10.03.2025 в 09:09
Загальна:
4.7
Структурованість
5.0
Оригінальність викладу
4.0
Відповідність темі
5.0
-

Совпель Ольга Вікторівна
03.02.2025 в 07:21
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
Показати ще 4 відгука