Зошит для практичних та контрольних робіт, Хімія 10 клас.
Зошит для практичних та контрольних робіт, Хімія 10 клас. Контрольні і практичні роботи розроблені відповідно до нової програми.

Довжик А. А.
Хімія
Зошит для практичних та контрольних робіт
10 клас
______________________________
______________________________
______________________________
______________________________ ______________________________
Луцьк 2021 Зміст
Контрольна робота № 1…………………………………………………3
Варіант 1…………………………………………………………………3
Варіант 2…………………………………………………………………4
Контрольна робота № 2…………………………………………………6
Варіант 1…………………………………………………………………6
Варіант 2…………………………………………………………………7
Контрольна робота № 3………………………………………………..10
Варіант 1………………………………………………………………. 10
Варіант 2………………………………………………………………..11
Контрольна робота за 1 семестр………………………………………13
Варіант 1………………………………………………………………..13
Варіант 2………………………………………………………………..14
Контрольна робота № 4………………………………………………..17
Варіант 1………………………………………………………………..17
Варіант 2………………………………………………………………..18
Контрольна робота № 5………………………………………………..20
Варіант 1………………………………………………………………..20
Варіант 2………………………………………………………………..21
Контрольна робота № 6………………………………………………..23
Варіант 1………………………………………………………………..23
Варіант 2………………………………………………………………..24
Контрольна робота за 2 семестр………………………………………26
Варіант 1………………………………………………………………..26
Варіант 2………………………………………………………………..27
Практична робота № 1……………………………………………….. 29
Варіант 1………………………………………………………………..29
Варіант 2………………………………………………………………..30
Практична робота № 2…………………………………………………32
Варіант 1………………………………………………………………..32
Варіант 2………………………………………………………………..33
Додаток 1……………………………………………………………….36
Додаток 2……………………………………………………………….37
Контрольна робота № 1
Теорія будови органічних сполук О. М. Бутлерова
Варіант 1
1. Вкажіть тип кристалічної гратки, найбільш характерної для органічних сполук:
а) атомну; в) молекулярну;
б) йонну; г) металічну.
2. Гомологи мають:
а) подібну будову,але різні властивості;
б) різну будову, але однакові властивості;
в) подібну будову і подібні властивості;
г) різну будову і різні властивості.
3. Вкажіть органічну сполуку, що має функціональну групу -ОН:
а) метанол; в) метан;
б) калій гідроксид; г) етин.
4. Вкажіть масову частку Карбону в етані :
а) 20% ; б) 80% ; в) 86% ; г) 92%. 5. Обчисліть відносну густину за воднем пропану:
а) 36 ; б) 44 ; в) 22 ; г) 18 ;
6. Обчисліть і позначте кількість атомів Карбону в молекулі алкану, що містить
20 атомів Гідрогену :
а) 8; б) 9; в) 7 ; г) 10.
7. Встановіть відповідність між назвами речовин і типом гібридизації орбіталей:
1) етин а) sр3
2) метан б) sр2 3) етен в) sр
г) sр3d
8. Встановіть відповідність між формулою речовини та класом органічних сполук
Формула Клас органічних сполук
1) CH3 - СН(NH2) - COOH а)спирти
2) CH3- CH2 - CH2-OH б) альдегіди
3) CH3-CH =C H- CH3 в) амінокислоти 4) CH3 - COH г) алкени д) алкани
9. Знайдіть молекулярну формулу і напишіть структурну формулу насиченого вуглеводню, відносна молекулярна маса якого дорівнює 86.
10.Який об’єм вуглекислого газу (н.у.) утвориться при спалюванні 5,2 г ацетилену.
11. Виведіть молекулярну формулу вуглеводню масова частка Карбону в якому становить 85,7% , а відносна густина за воднем парів речовини 28.
Варіант 2
1. Вкажіть тип хімічного зв’язку, найбільш характерного для органічних сполук:
а) ковалентний; в) йонний;
б) водневий; г) металічний.
2. Ізомери мають:
а) різні формули, але подібну будову;
б) однакові формули, але різну будову;
в) різні формули і різну будову;
г) однакові формули і подібну будову.
3.Вкажіть органічну сполуку, що має функціональну групу -СООН:
а) метанол; в) етан;
б) натрій гідроксид; г) метанова кислота.
4. Вкажіть масову частку Гідрогену в метані:
а) 20%; б) 25%; в) 75%; г) 80%;
5. Обчисліть відносну густину за воднем пентану:
а) 72; б) 36; в) 60; г) 30;
6. Обчисліть і позначте кількість атомів
Карбону в молекулі алкану, що містить 18 атомів Гідрогену :
а) 10; б) 7; в) 9; г) 8.
7. Встановіть відповідність між назвами речовин та будовою їх молекул:
1) метан а) тетраедрична
2) етин б)лінійна 3) етен в)плоска
г) квадратна
8. Встановіть відповідність між формулою речовини та класом органічних сполук
Формула Клас органічних сполук
1) CH3 - СН2 - СН2 - COOH а)спирти
2) СН3 – COO - CH3 б) альдегіди
3) CH3 – CH = CH2 в) естери
4) CH3 – CH2 - CH2 - OH г) алкени
д) карбонові кислоти
9. Знайдіть молекулярну формулу і напишіть структурну формулу насиченого вуглеводню, відносна молекулярна маса якого дорівнює 100.
10. Який об’єм етану спалили(н.у.), якщо виділився карбон (ІV) оксид масою 22г.
11. Виведіть молекулярну формулу вуглеводню масова частка
Гідрогену в якому становить 20% ,а відносна густина за воднем парів речовини 15.
Дата: ______________ Варіант:_____
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________
____________________________________________________________
Контрольна робота № 2
Вуглеводні
Варіант 1
1. Загальна формула алканів
а) CnH2n-2 б) CnH2n+2 в) CnH2n 2. Дегідратація це:
а) приєднання водню; в) приєднання води;
б) відщеплення води; г) відщеплення водню.
3. Характерна реакція для алканів:
а) приєднання; б) заміщення; в) нейтралізації.
4. У молекулі етилену між атомами карбону є:
а) одинарний зв'язок; в) подвійний зв'язок;
б) потрійний зв'язок;
5. Ароматичні вуглеводні називають:
а) алкани, б) арени, в) алкіни, г) алкени; 6. Тип гібридизації алканів:
а) sp3 ; б) sp2 ; в) sp .
7. Які вуглеводні називаються насиченими? Складіть молекулярні формули алканів, що містять 5,7,9,10 атомів карбону.
8. Складіть рівняння реакції:
а) окиснення метану;
б) хлорування етилену;;
в) окиснення ацетилену KМnO4;
г) нітрування бензолу.
9. Напишіть структурні формули:
а) 2,2,4-триметилоктану;
б) 4-етил-2,5-диметилгепт-2-ену; 10. Здійсніть перетворення:
CH3COONa СН4 СH3CI
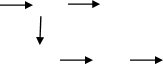 С2H2 C2H4 (C2H4 )n
С2H2 C2H4 (C2H4 )n
11. Визначте молекулярну формулу алкану з молекулярною масою 100. Навести розрахунок.
12. Який об'єм пропану спалили , якщо утворився вуглекислий газ кількістю речовини 4,5 моль?
Варіант 2
1. Загальна формула алкенів:
а) CnH2n; б) CnH2n+2; в) CnH2n-2.
2. Гідрування це:
а) приєднання водню; в) приєднання води;
б) відщеплення води; г) відщеплення водню.
3. Алкіни не вступають в реакцію:
а) приєднаня; б) окиснення; в) заміщення.
4. У молекулі ацетилену між атомами карбону є:
а) одинарний зв'язок; в) подвійний зв'язок;
б) потрійний зв'язок;
5. До природніх джерел вуглеводнів відносять:
а) бензен; б) нафта; в) етен; г) етин.
6. Тип гібридизації алканів:
а) sp3 ; б) sp2 ; в) sp .
7. Які вуглеводні називаються насиченими? Складіть молекулярні формули алкенів, що містять 3,6,8,10 атомів карбону.
8. Складіть рівняння реакції:
а) нітрування метану;
б) горіння етилену;
в) тримеризація ацетилену;
г) бромування бензолу.
9. Напишіть структурні формули:
а) 3,5-диетил-2-метилгептану;
б) 2,4,4,6-тетраметилокт-2-ину;
10. Здійсніть перетворення
C CH4 CH3NO2
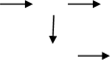 C2H2 C2H4
C2H2 C2H4 ![]() C2H5OH
C2H5OH
11. Визначте молекулярну формулу алкану з молекулярною масою 114. Навести розрахунок.
12. . Розрахувати об'єм (н.у.) карбон (IV) оксиду , що утворився при спалюванні 4,2 г пропену.
Дата: ______________ Варіант:_____
____________________________________________________________
____________________________________________________________
____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________ Контрольна робота № 3
Спирти. Альдегіди. Карбонові кислоти
Варіант №1
1. Функціональна група спиртів:
а) -OH; б) -COOH; в) -COH;
2. Етанол — це:
а) багатоатомний спирт; в) насичений одноатомний спирт;
б) ароматичний спирт; г) ненасичений одноатомний спирт.
3. Вкажіть ознаку якісної реакції на гліцерол:
а) утворення яскраво-синього розчину;
б) утворення срібного нальоту;
в) утворення жовтого осаду;
г) утворення блакитного драглистого осаду.
4. Спільна ознака між альдегідами і карбоновими кислотами:
а) наявність зв'язку С = С;
б) наявність зв'язку С = О;
в) здатність реагувати з лугами;
г) здатність змінювати колір лакмусу;
5. В реакцію естерифікації вступає:
а) пропан; б) пропаналь; в) пропен; г) пропанова кислота.
6. Лимонна кислота — це кислота:
а) одноосновна; б) двоосновна; в) трьохосновна.
7. Напишіть рівняння реакцій:
а) взаємодія фенолу з бромною водою;
б) взаємодія гліцерину з Cu(OH)2;
в) взаємодія оцтового альдегіду з Ag2O;
г) взаємодія оцтової кислоти з магнієм.
8. Напишіть структурні формули речовин за їх назвами:
а) 4-етил-3,5-диметилгексаналь;
б) 3-метилпентанова кислота.
9. За систематичною номенклатурою назвіть спирт, структурна формула якого наведена нижче:
![]() С2Н5
С2Н5
СН3 — СН2 — С — СН2 — СН — СН — СН3
![]()
![]()
С2Н5 ОН СН3
10. Здійснити перетворення:
![]() С2Н5ОН C2H4
С2Н5ОН C2H4 ![]() С2Н5CI
С2Н5CI ![]() С2Н5ОН
С2Н5ОН
С2Н5 — O — С2Н5
11. Обчисліть об'єм водню , що виділиться при дії металічного кальцію на метанол масою 96 г.
12. Обчисліть об’єм кисню, що витратились на повне окиснення метанолу масою 18,4 г
Варіант 2
1. Функціональна група альдегідів:
а) -OH; б) -COOH; в) -COH;
2. Етиленгліколь — це спирт:
а) одноатомний; б) двохатомний; в) трьохатомний.
3.Укажіть назву отруйного насиченого одноатомного спирту:
а) етанол; б) метанол; б) гліцерол; г)фенол.
4. Загальна формула одноосновних карбонових кислот:
а) СnН2n+1СОOH; в) СnН2n+1СOH;
б) СnН2n+1ОH; г) СnН2n+1СOОR. 5. Спільна ознака між альдегідами і спиртами:
а) наявність карбоксильної групи; в) наявність Оксигену;
б) наявність гідроксильної групи; г) здатність реагувати з Nа.
6. В реакцію “срібного дзеркала” вступає:
а) гліцерин; б) пропаналь; в) пропен; г) пропанова кислота.
7. Напишіть рівняння реакцій:
а) взаємодія метанолу з металічним натрієм;
б) взаємодія фенолу з нітратною кислотою;
в) взаємодія оцтового альдегіду з Cu(OH)2;
г) взаємодія оцтової кислоти з цинком;
8. Напишіть структурні формули речовин за їх назвами:
а) 3,4,4-триметилгексаналь;
б) 2-метилпентанова кислота.
9. За систематичною номенклатурою назвіть спирт, структурна формула якого наведена нижче:
СН3 — СH — СН2 — СН — СН — СН3
![]()
![]()
![]()
С2Н5 ОН СН3
10. Здійснити перетворення:
![]() C2H4
C2H4 ![]() С2Н5ОН
С2Н5ОН ![]() СН3СООС2Н5 СН3СООН
СН3СООС2Н5 СН3СООН
СН3СООNа
11. Обчисліть масу етанолу, що утвориться при дії водного розчину натрій гідроксиду на хлоретан масою 129 г.
12. Обчисліть об’єм кисню, що витратились на повне окиснення етанолу масою 16,1 г
Дата: ______________ Варіант:_____
____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
Контрольна робота за 1 семестр
Варіант 1
1. Загальна формула алкінів:
а) CnH2n; б) CnH2n+2; в) CnH2n-2. 2. Тип гібридизації алкенів:
а) sp3 ; б) sp2 ; в) sp ;
3. Функціональна група спиртів:
а) -OH; б) -COOH; в) -COH;
4. Укажіть якісний реагент на гліцерил:
а) арґентум (І) нітрат; в)купрум (ІІ) гідроксид;
б) йод; г)бромна вода.
5. Вкажіть загальну формулу насичених одноосновних карбонових кислот:
а) СnН2n+1OH; в) СnН2n+1СOH;
б) СnН2n+1СOОH; г) СnН2n+1СOОR.
6. Реакція “срібного дзеркала” характерна для:
а) оцтової кислоти; в) оцтового альдегіду.
б) метанолу;
7.Установіть відповідність:
1. Оцтовий альдегід a) CH2CI2
2. Етиленгліколь б) C3H7COOH
3. Дихлорометан в) CH2OH – CH2OH
4. Масляна кислота г) CH3COH
8. Визначіть молекулярну формулу алкену з молекулярною масою 112.
Наведіть розрахунок.
9. Напишіть формули:
а) 2,2,3-триметилпентану;
б) 2-етил-3,4-диметилгептанова кислота.
10. Напишіть рівняння наступних реакцій:
а) нітрування метану;
б) взаємодія фенолу з нітратною кислотою;
в) міжмолекулярна дегідратація етанолу;
г) взаємодія оцтового альдегіду з Ag2O.
11. Здійсніть перетворення:
![]()
![]()
![]() С СН4 СО СН3ОН СН3СОН СН3СООН 12. Обчисліть масу етанолу, що утвориться при дії водного розчину натрій гідроксиду на хлоретан масою 129 г.
С СН4 СО СН3ОН СН3СОН СН3СООН 12. Обчисліть масу етанолу, що утвориться при дії водного розчину натрій гідроксиду на хлоретан масою 129 г.
Варіант 2
1. Загальна формула алкенів:
а) CnH2n; б) CnH2n+2; в) CnH2n-2.
2. Тип гібридизації характериний для алкінів:
а) sp3 б) sp2 в) sp .
3. Визначіть речовину ‘Х’, що відповідає схемі перетворень
С2Н4→Х→С2Н4
а) ацетилен; б) вода; в) етанол; г) етилен.
4. Вкажіть ознаку якісної реакції на гліцерол:
а) утворення яскраво-синього розчину;
б) утворення срібного нальоту;
в) утворення жовтого осаду;
г) утворення блакитного драглистого осаду.
5. Спільна ознака між альдегідами і карбоновими кислотами:
а) наявність зв'язку С = С;
б) наявність зв'язку С = О;
в) здатність реагувати з лугами;
г) здатність змінювати колір лакмусу; 6. Загальна формула альдегідів:
а) СnН2n+1OH; в) СnН2n+1СOH;
б) СnН2n+1СOОH; г) СnН2n+1СOОR.
7.Установіть відповідність:
1. Валеріанова кислота a) HCOH
2. Гліцерол б) C4H9COOH
3. Нітрометан в) CH2OH – CHOH — СН2ОН
4. Метаналь г) CH3NO2
8. Визначіть молекулярну формулу алкіну з молекулярною масою 54 .
Наведіть розрахунок.
9. Напишіть формули:
а) 3-етил-3-метилпентану;
б) 3-метилпентанова кислота.
10. Напишіть рівняння наступних реакцій:
а) хлорування метану;
б) окиснення ацетилену KMnO4;
в) дегідратація етанолу ;
г) взаємодія оцтової кислоти з магнієм. 11. Здійсність перетворення:
C2H2 C2H4 ![]() C2H5OH
C2H5OH ![]() C2H5СOН
C2H5СOН
![]()
![]()
CH4 C2H5СOОН
12. Обчисліть об'єм водню , що виділиться при дії металічного кальцію на метанол масою 96 г.
Дата: ______________ Варіант:_____
____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
Контрольна робота № 4
Естери. Вуглеводи
Варіант 1
1. Загальна формула естерів:
а) R – COOH; б) R – O – R; в) R – COOR ; г) R – OH;
2. Виберіть правильне твердження щодо естерів:
а) усі тверді речовини; в) мають прємний запах;
б) проявляють кислотні вла-ті; г) нелеткі.
3. Глікоген — це:
а) моносахарид; б) дисахарид; в) полісахарид; г) олігосахарид.
4. Фруктозу інакше називають:
а) молочним цукром; в) фруктовим цукром;
б) інвертний цукром; г) тростинним цукром.
5. Вкажіть формулу крохмалю:
а) С6Н12О6; б) С12Н22О11; в) (С6Н10О5)n; г) С5Н10О5.
6. Вкажіть вуглеводи, які не розчиняються у воді:
а) дисахариди; б) полісахариди; в) моносахариди.
7. Встановіть відповідність між формулою естеру і назвою:
1. СН3СООСН3 а) етилпропіонат
2. НСООС3Н7 б) пропілформіат
3. С2Н5СООС2Н5 в) метилацетат
8. Молекулярна і структурна формула сахарози. Фізичні та хімічні властивості.
9. Напишіть рівняння реакцій:
а) гідрування триолеїну;
б) гідроліз сахарози;
в) спиртове бродіння глюкози.
10. Здійснити перетворення:
![]()
![]() сахароза глюкоза етиловий спирт диетиловий етер
сахароза глюкоза етиловий спирт диетиловий етер
вуглекислий газ
11. Розрахуйте масу гліцеролу яку можна добути з 1 кг трипальмітину. 12. Який об’єм вуглекислого газу утвориться в результаті повного окиснення (горіння) сахарози масою 260 г?
Варіант 2
1. В основі виробництва маргарину з олії лежить процес:
а) гідролізу жирів; в) гідрування жирів;
б) дегідрування жирів; г) гідратації жирів.
2. Виберіть правильне твердженн щодо естерів:
а) електроліти; б) розчинні у воді; в) нерозчинні у воді.
3. Мальтоза — це:
а) моносахарид; б) дисахарид; в) полісахарид; г) олігосахарид.
4. Вкажіть ознаку реакції взаємодії крохмалю з йодом:
а) поява запаху; в) утворення червоного осаду;
б) знебарвлення розчину; г) утворення синього забарвлення.
5. Вкажіть формулу сахарози:
а) С6Н12О6; б) С12Н22О11; в) (С6Н10О5)n; г) С5Н10О5.
6.Фруктозу інакше називають:
а) молочним цукром; в) фруктовим цукром;
б) інвертним цукром; г) тростинним цукром.
7. Встановіть відповідність між формулою естеру і назвою:
СН3СООС3Н7 а) етилацетат
НСООС2Н5 б) етилформіат
СН3СООС2Н5 в) пропілацетат
8. Молекулярна і структурна формула глюкози. Фізичні та хімічні властивості.
9. Напишіть рівняння реакцій:
а) гідроліз тристеарину;
б) гідроліз целюлози;
в) молочнокисле бродіння глюкози.
10. Здійснити перетворення:
![]()
![]() сахароза глюкоза етиловий спирт вуглекислий газ
сахароза глюкоза етиловий спирт вуглекислий газ
молочна кислота
11. Яка мас натрій гідроксиду потрібна на добування 500 г гліцеролу з чистого триолеїну?
12. Який об’єм вуглекислого газу утвориться при спиртовому бродінні глюкози масою 270 г?
Дата: ______________ Варіант:_____
____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________
____________________________________________________________
Контрольна робота № 5
Нітрогеновмісні органічні сполуки
Варіант 1
1. Молекулярна формула етиламіну:
а) СН3NH2; б) СН3СН2NH2; в) (СН3)2NH; г) (СН3)3N.
2. Виберіть число атомів у молекулі феніламіну:
а) 7; б) 9; в) 12; в) 14.
3. Білки це:
а) біополімери, що складаються із залишків α-амінокислот ;
б) біопомімери, що складаються їз залишків α-глюкози ;
в) біополімери, що складаються із залишків будь яких амінокислот. 4. Кількість амінокислот, залишки яких можуть входити до складу білків:
а) 15; б) 20; в) безліч.
5. Денатурація білка – це руйнування структури:
а) первинної; б) вторинної; в) первинної та вторинної.
6. Залишки амінокислот у білках сполучені зв’язками:
а) йонними; б) водневими; в) пептидними.
7. Які сполуки називають білками?
8. Обчисліть масові частки елементів в амінооцтовій кислоті.
9. Напишіть структурні формулу таких речовин:
а) 2,3-диметил-5-аміногексанова кислота;
б) 2,-етил-3,3-метилпентан-1-амін.
10. Написати схему утворення дипептиду аланіну і лейцину.
11. Яку масу аміноетанової кислоти можна добути при взаємодії мнохлоретанової кислоти масою 56,7 г і аміаку об'ємом 11,2 л? 12. Обчисліть масу аніліну , який утвориться з нітробензолу масою 503 г та водню масою 24 г?
Варіант 2
1. Формула триметиламіну:
а) С6Н5NH2 ; б) (СН3)2NH; в) (СН3)3N.
2. Аміни – це похідні:
а) алканів; б) алкенів; в) бензену; г) амоніаку. 3. Виберіть число атомів у молекулі етиламіну:
а) 6; б) 7; в) 8; г) 10.
4. Виберіть зв'язок який називають пептидним:
а) — СО — О — ; в) — СО — NH2 —;
б) — СО — NH —; г) — СООН — NH — .
5. Амінокислоти – це речовини, у молекулах яких одночасно містяться функціональні групи:
а) аміно- та гідроксильна; б) карбоксильна і гідроксильна;
в) аміно- та карбоксильна.
6. Виберіть неправильне твердження що до хімічних властивостей амінооцтової кислоти:
а) амінооцтова кислота — амфотерна речовина;
б) молекула амінооцтової кислоти не взаємодіють одна з одною;
в) амінооцтова кислота взаємодіє з лугами;
г) амінооцтова кислота взаємодіє з хлоридною кислотою.
7. Що таке денатурація білка і які фактори її спричиняють?
8. Обчисліть масові частки елементів в амінобутановій кислоті.
9. Напишіть структурні формулу таких речовин:
а) 3-етил-α-амінопентанова кислота;
б) 3-етил-5,5-диметилгептан-2-аміну.
10. Написати схему утворення дипептиду лейцину і валіну.
11. Аміноетанова кислота масою 67,5 г вступила в реакцію з натрій гідроксидом. Яка маса солі натрій аміноацетату утворилась? 12. Яка маса солі утворилася внаслідок взаємодії пропіламіну масою 17,7 г їз сульфатною кислотою масою 32 г.
Дата: ______________ Варіант:_____
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
Контрольна робота № 6
Синтетичні високомолекулярні органічні сполуки
Варіант 1
1. Каучуки- це полімери;
а) алканів; б) алкінів; в) алкенів; г) алкадієнів.
2. До синтетичних волокон належить:
а) бавовна; б) капрон; в) вовна; г) ацетатне волокно.
3. До природніх волоког належить:
а) лавсан ; б) капрон; в) шовк; г) ацетатне волокно.
4. Виберіть кислоту, яка належить до вітамінів:
а) гептанова; б) аскорбінова; в) масляна; г) пальмітинова.
5. Сировиною для виробництва гуми є:
а) синтетичний каучук; б) лавсан;
в) ацетатне волокно; г) поліетилен.
6. Нестача вітамінів А викликає:
а) пелагру; б) рахіт; в) курячу сліпоту; г) недокрів'я.
7. Хімічна назва аспірину:
а) аскорбінова кислота; б) фталева кислота;
в) ацетилсаліцилова кислота; г) бензойна кислота.
8. До полімерів належать:
а) поліетилен; б) бутадієн; в) каучук; г) нонан.
9. Вітамін Д міститься в продуктах:
а) яєчні жовтки; б) капуста; в) м'ясо; г) риб'ячий жир.
10. Встановити відповідність:
Вітамін Хімічна назва
1 А а) ціанокобаламін
2 В2 б) аскорбінова кислота 3 В12 в) рибофлавін г) ретинол
11. Встановити відповідність
Волокно Група волокон
1 лавсан а синтетичні
2 вовна б штучні 3 мідноамоніачне в природні
12. Встановити відповідність
Харчові добавки Призначення
1 ароматизатори а поліпшення зовнішнього вигляду
2 барвники б регуляція консистенції 3 емульгатори в регуляція смаку г збільшення теміну придатності
Варіант 2
1. До штучних волокон належить:
а) бавовна; в) капрон; б) вовна; г) ацетатне волокно.
2. Сировиною для виробництва синтетичного каучуку є:
а) бутадієн-1,3; б) капрон; в) ацетилен; г) пропен.
3. Авітаміноз вітаміну С викликає захворювання:
а) бері-бері; б) судоми; в) цингу; г) анемія.
4. У низькокалорійних продуктах замість цукру використовують:
а) глутамат натрію; б) аспартам; в) кукурмін; г) молочну кислоту.
5. Надлишковий вміст вітаміну в організмі називається:
а) авітаміноз; б) цинга; в) гіповітаміноз; г) гіпервітаміноз.
6. До полімерів належать:
а) білки; б) гліцерин; в) жири; г) крохмаль.
7. Особливими властивостями капрону є:
а) гігроскопічність; в) термостійкість; б) міцність; г) малостійкість.
8. До харчових добавок синтетичного походження належать:
а) сахарин; в) кукурмін; б) аспартам; г) цукор.
9. Виберіть продукти, я яких знаходиться вітамін В12:
а) морепродукти; в) яйце; б) сир; г) фрукти
10. Встановити відповідність:
Вітамін Хімічна назва
1 С а тіамін
2 В1 б аскорбінова кислота
3 В6 в рибофлавін г придоксин
11. Встановити відповідність
Волокно Група волокон
1 капрон а синтетичні
2 бавовна б штучні
3 ацетатний шовк в природні 12. Встановити відповідність
Харчові добавки Призначення
1 консерванти а поліпшення зовнішнього вигляду
2 загусники б регуляція консистенції 3 відбілювачі в регуляція смаку г збільшення теміну придатності
Дата: ______________ Варіант:_____
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________ Контрольна робота за 2 семестр
Варіант 1
1. Виберіть правильне твердення щодо мила:
а) рідкі мила є солями Калію;
б) рідкі мила є солями Натрію;
в) утворюється гліцерином і вищими карбоновими кислотами;
г) утворюється нижчими карбоновими кислотами.
2. Аміни — це похідні :
а) алканів; б) амоніаку; в) алкенів; г) бензену.
3. Виберіть продукти згоряння амінів:
а) СО2, Н2О, NH3; б) СО2, Н2О, N2; в) СО2, Н2О; г) СО2, Н2О, N.
4. Сахароза — це:
а) моносхарид; б) дисахарид; в) полісахарид.
5. Вкажіть ознаку реакції взаємодії крохмалю з йодом:
а) поява запаху; в) утворення червоного осаду;
б) знебарвлення розчину; г) утворення синього забарвлення.
6. До синтетичних волокон належить:
а) бавовна; б) капрон; в) вовна; г) ацетатне волокно.
7. Встановити відповідність:
Вітамін Хімічна назва
1 С а тіамін
2 В1 б аскорбінова кислота
3 В6 в рибофлавін
г придоксин
8. Які сполуки називають білками?
9. Напишіть структурні формулу 3-етил-6.6-диметилгептан-2-аміну.
10. Напишіть рівняння реакцій:
а) окиснення глюкози аміачним розчином Ag2O;
б) взаємодія феніламіну з хлоридною кислотою.
11. Обчисліть масу гліцерину , що утвориться при взаємодії необхідної кількості калій гідроксиду із 9,8 кг триолеїну.
12. Який об'єм натрій гідроксиду з масовою часткою 30% потрібен для нейтралізації 150 г аміноетанової кислоти?
Варіант 2
1. Триолеїн на відміну від тристеарину, реагує з:
а) водою; б) воднем; в) лугом; г) натрій хлоридом.
2. Виберіть зв'язок який називають пептидним:
а) — СО — О — ; б) — СО — NH —;
в) — СО — NH2 —; г) — СООН — NH —.
3. Білки це:
а) біопомімери, що складаються їз залишків α-глюкози ;
б) біополімери, що складаються із залишків α-амінокислот ;
в) біополімери, що складаються із залишків будь яких амінокислот 4. Мальтоза — це:
а) моносхарид; б) дисахарид; в) полісахарид; г) олігосахарид.
5. Вкажіть формулу крохмалю:
а)С6Н12О6; б)С12Н22О11; в)(С6Н10О5)n; г)С5Н10О5.
6. До штучних волокон належить:
а) бавовна; в) капрон; б) вовна; г) ацетатне волокно.
7. Встановити відповідність
Волокно Група волокон
1 лавсан а синтетичні
2 вовна б штучні 3 мідноамоніачне в природні
8. Чому мила погано миляться у воді? Відповідь підтвердіть рівняннями реакцій.
9. Напишіть структурні формулу 2,3-диметил-5-аміногексанова кислоти;
10. Напишіть рівняння реакцій:
а) взаємодія сахарози з Cu(OH)2;
б) взаємодія аніліну з бромом.
11. Внаслідок гіролізу сахарози масою 700 г добули глюкозу масою 360 г. Визначте масову частку домішок, що мітяться у сахарозі.
12. Яку масу аміноетанової кислоти можна добути при взаємодії мнохлоретанової кислоти масою 56,7 г і аміаку об'ємом 11,2 л?
Дата: ______________ Варіант:_____
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________
____________________________________________________________
Практична робота № 1
Властивості оцтової кислоти
Мета: Дослідити фізичні та хімічні властивості оцтової кислоти. Встановити подібність та відмінність у хімічних властивостях оцтової кислоти та мінеральних кислот.
Обладнання: штатив з пробірками, пробіркотримач, спиртівка, сірники
Реактиви: розчин оцтової кислоти, лакмус, метилоранж, розчин лугу, цинк, крейда, натрій карбонат.
З правилами техніки бепеки при роботі в хімічному кабінеті ознайомлений (-на) і зобов'язуюсь їх повністю виконувати.
_____________ ______________
дата підпис учня
Завдання № 1. Виберіть правильну відповідь.
Варіант 1
1. До органічних кислот відносять речовини:
а) НСОН; б) СН3ОН; в) С2Н5СООН.
2. Одноосновні насичені карбонові кислоти мають загальну формулу:
а) СnН2n+1OH; в) СnН2n+1СOH;
б) СnН2n+1СOОH; г) СnН2n+1СOОR. 3. З оцтовою кислотою реагують з виділенням водню:
а) Mg; б) Cu; в) Zn.
4. З оцтовою кислотою реагують за певних умов:
а) CaO; б) HCI; в) NaOH; г) Na2CO3.
5. При взаємодії оцтової кислоти з спиртами відбувається реакція:
а) нейтралізації; б) естерифікації; в) гідролізу.
Варіант 2
1. До органічних кислот відносять речовини:
а) НСОН; б) СН3СООН; в) С2Н5ОН.
2. Функціональна група карбонових кислотмає назву:
а) гідроксильна; в) карбонільна.
б) карбоксильна; 3. З оцтовою кислотою реагують з виділенням водню:
а) Hg; б) Ag; в) Fe.
4. З оцтовою кислотою реагують за певних умов:
а) Mg(OH)2; б) NaNO3; в) Na2O; г) CaCO3.
5. При взаємодії естеру з водою відбувається реакція:
а) естерифікації; б) гідролізу; в) нейтралізації.
Завдання 2. Виконайте досліди.
Дослід № 1
Фізичні властивості оцтової кислоти
Опишіть зовнішній вигляд оцтової кислоти, випробуйте її запах. До 1 мл води у пробірці додайте стільки ж оцтової кислоти.
Охарактерезуйте фізичні властивості оцтової кислоти.
____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________
Дослід №2
Дія оцтової кислоти на індикатори
У дві пробірки додайте 1-2 мл розчину оцтової кислоти, добавте в першу пробірку 1-2 краплі лакмусу, а в другу — 1-2 краплі метилоранжу?
Що спостерігаєте? Про наявність яких йонів свідчить зміна забарвлення індикатора?
____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ Напишіть рівняння електролітичної дисоціації?
____________________________________________________________ ____________________________________________________________
Дослід № 3
Взаємодія оцтової кислоти з основами
До розчину лугу, забарвленому фенолфталеїном ,краплями додайте розчин оцтової кислоти.
Що спостерігаєте? Яке середовище існувало в розчині лугу?
____________________________________________________________
____________________________________________________________ ____________________________________________________________ Запишіть рівняння реакцій в молекулярній та йонних формах. До яких реакцій відноситься даний процес?
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
Дослід № 4
Взаємодія оцтової кислоти з металами
У дві пробірки покладіть по гранулі цинку. Долийте в першу 1 мл оцтової кислоти, а в другу 1 мл розчину хлоридної кислоти.
Що спостерігаєте? В якій пробірці реакція відбувається швидше?
____________________________________________________________
____________________________________________________________ ____________________________________________________________
Запишіть рівняння реакцій в молекулярній та йонних формах. До яких типів відносяться дані реакції?
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________
Дослід 5
Взаємодія оцтової кислоти з солями
В одну пробірку з розчином оцтової кислоти добавте 0,5 мл розчину натрій карбонату, а в другу покладіть кусочок крейди. Що спостерігаєте?
____________________________________________________________ ____________________________________________________________
Запишіть рівняння реакцій в молекулярній та йонних формах. Чи всі солі взаємодіють з оцтовою кислотою?
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________ Висновки:
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________
Практична робота № 2
Розв'язування експериментальних задач на розпізнавання органічних речовин.
Мета: Закріпити знання про характерні реакції на органічні речовини. Обладнання: штатив з пробірками, пробіркотримач, спиртівка, сірники. Реактиви (вказати після виконання роботи):
З правилами техніки бепеки при роботі в хімічному кабінеті ознайомлений (-на) і зобов'язуюсь їх повністю виконувати.
_____________ ______________
дата підпис
Завдання № 1. Виберіть правильну відповідь.
Варіант 1
1. Характерною ознакою на крохмаль є його взаємодія з:
а) Cu(OH)2; б) розчином Н2SO4; в) йодом.
2. Утворення розчину яскраво блакитного кольору при взаємодії з Cu(OH)2 зумовлено наявністю в речовині:
а) декількох гідроксильних груп; б) однієї гідроксильної групи
в) альдегідної групи.
3. Наявніть альдегідної групи в речовині можна визначити:
а) при нагріванні речовини з аміачним розчином Ag2O ;
б) при нагріванні речовини з Cu(OH)2;
в) при нагріванні речовини з CuO. 4. Оцтовий альдегід можна добути при:
а) гідратації етилену; в) окисненні оцтової кислоти.
б) гідратації ацетилену;
Варіант 2
1. Реакція “срібного дзеркала” характерна для:
а) мурашинної кислоти; б) оцтової кислоти; в) розчину глюкози.
2. Якісними реакціями на білки є:
а) реакція Кучерова; в) біутерова реакція.
б) ксантопротеїнова реакція; 3. Білий осад утвориться при доливанні бромної води до:
а) бензену; б) розчину фенолу; в) розчину етанолу. 4. Глюкозу можна добути при гідролізі:
а) сахарози; б) крохмалю; в) білка.
Завдвння №2 Варіант 1.
У двох колбах містяться рідини: гліцерин і глюкоза. Встановіть хімічним способом вміст кожної колби.
Варіант 2.
У двох колбах містяться рідини: оцтова кислота і гліцерин.
Встановіть хімічним способом вміст кожної колби.
Складіть план виконання дослідів, опишіть спостереження та напишіть рівняння проведених реакцій.
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________
Завдвння №3 Варіант 1.
У двох прономерованих пробірках містяться розчини білка і мила. За допомогою характерних реакцій визначте кожну речовину.
Варіант 2.
У двох прономерованих пробірках містяться розчини сахарози і глюкози. За допомогою характерних реакцій визначте кожну речовину.Складіть план виконання дослідів, опишіть спостереження та напишіть рівняння проведених реакцій.
____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ Висновки:
____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________ ____________________________________________________________
____________________________________________________________
____________________________________________________________ ____________________________________________________________
____________________________________________________________
Додаток 1. Таблиця розчинності кислот, основ і солей у воді.
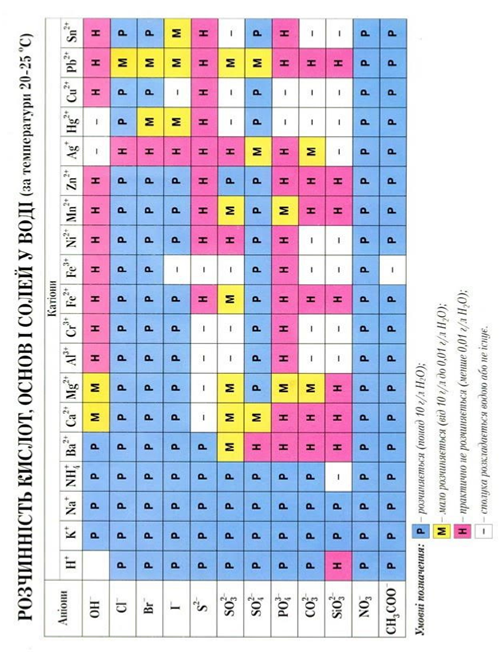
Додаток 2. Періодична система елементів Д. І. Менделєєва
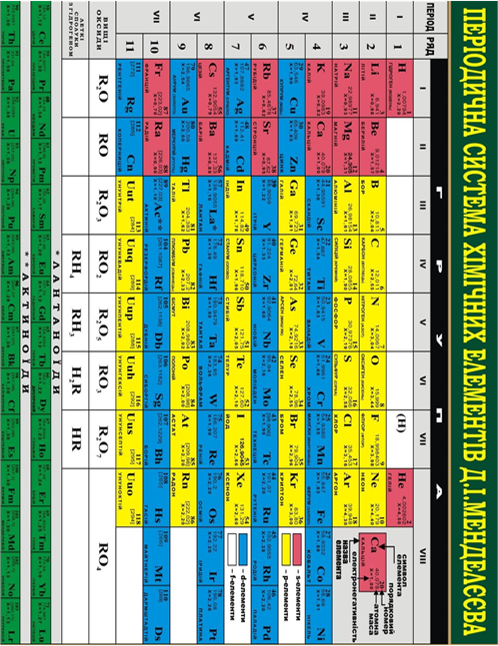



про публікацію авторської розробки
Додати розробку
