Амінокислоти. Білки. Біологічна роль білків та амінокислот.







![Хімічні властивості амінокислот. Реакції за участю аміногрупи – основні властивостіПодібно до амінів (основ), амінокислоти реагують з кислотами H2 N - СН2 – СООН + НCl → [H3 N - СН2 – СООН]Cl гліциній хлорид (сіль)Реакції між амінокислотами – утворення поліпептидів. H2 N-СН2–СООН + H2 N-СН2–СООН →H2 N-СН2–СО-NН-СН2–СООН + Н2 О Хімічні властивості амінокислот. Реакції за участю аміногрупи – основні властивостіПодібно до амінів (основ), амінокислоти реагують з кислотами H2 N - СН2 – СООН + НCl → [H3 N - СН2 – СООН]Cl гліциній хлорид (сіль)Реакції між амінокислотами – утворення поліпептидів. H2 N-СН2–СООН + H2 N-СН2–СООН →H2 N-СН2–СО-NН-СН2–СООН + Н2 О](/uploads/files/90527/238770/258169_images/12.jpg)
































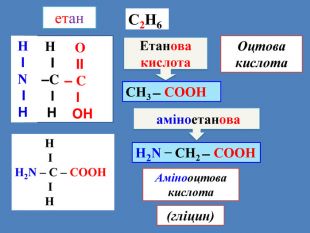
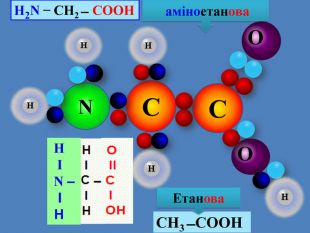
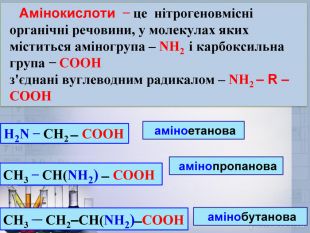
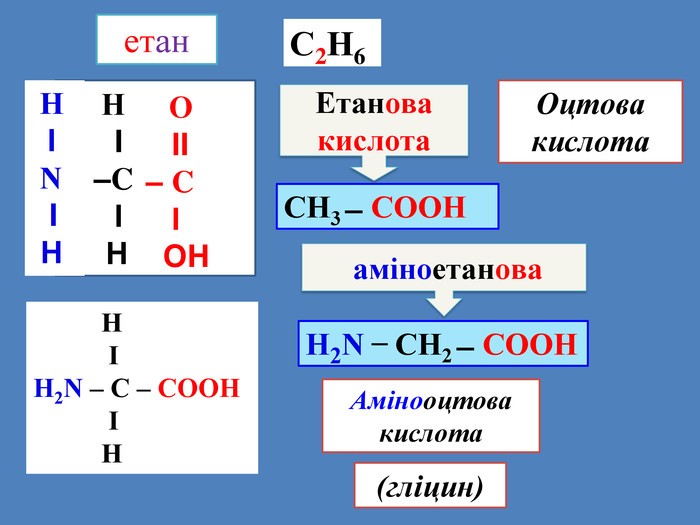
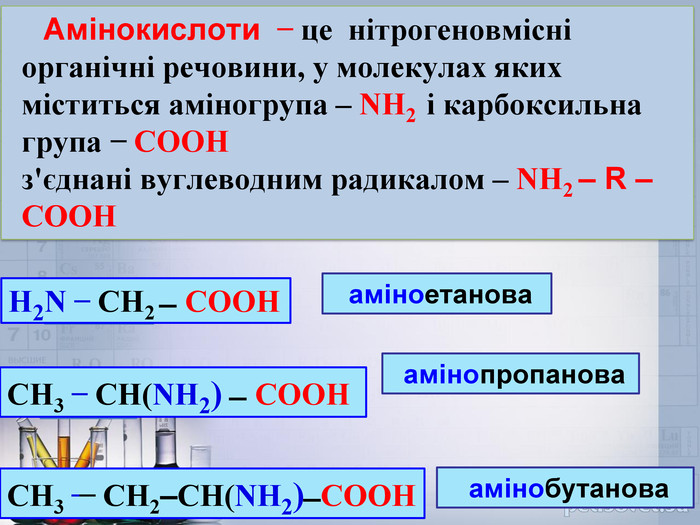
Амінокислоти ̶ це нітрогеновмісні органічні речовини, у молекулах яких міститься аміногрупа – NH2 і карбоксильна група ̶ СООНз'єднані вуглеводним радикалом – NH2 – R – СООНС2 Н6 H2 N ̶ СН2 ̶ СООН аміноетанова. С3 Н8 СH3 ̶ СН(NH2) ̶ СООН амінопропанова. С4 Н10 СH3 ̶ ̶ СН2–СН(NH2) ̶ СООН амінобутанова
Найпростіший представник класу амінокислот має формулу H2 N ̶ СН2 ̶ СООН — аміноетанова (або амінооцтова) кислота — перший член гомологічного ряду одноосновних насичених амінокислот. (альфа)– амінокислота— це сполука, в якій групи – NH2 і ̶ СООН з'єднані з одним і тим же атомом Карбону Амінокислоти — це цеглинки, з яких побудовані всі рослинні і тваринні білки. Вони є структурними одиницями білків.
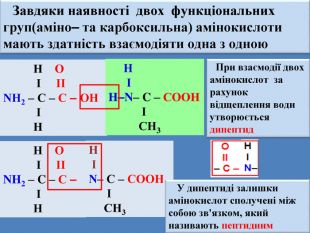
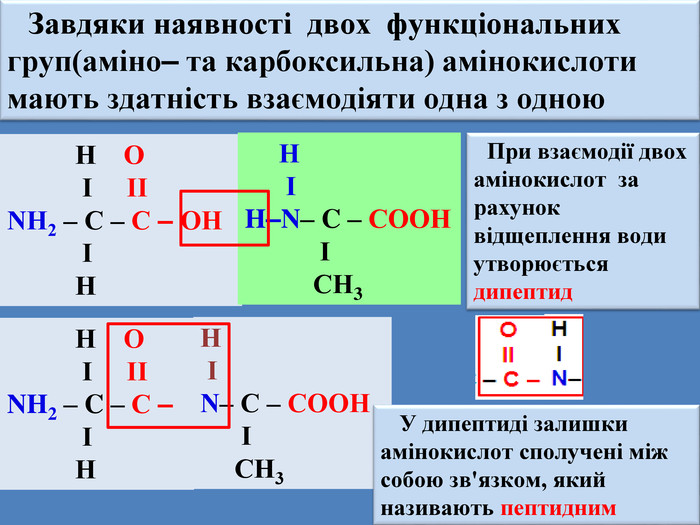
Завдяки наявності двох функціональних груп(аміно– та карбоксильна) амінокислоти мають здатність взаємодіяти одна з одною Н О Ι ΙΙNH2 – C – С – ОН Ι Н Н Ι H–N– C – СООН Ι СН3 При взаємодії двох амінокислот за рахунок відщеплення води утворюється дипептид Н О Ι ΙΙNH2 – C – С – Ι Н Н Ι N– C – СООН Ι СН3 У дипептиді залишки амінокислот сполучені між собою зв'язком, який називають пептидним
Систематична номенклатура: назва утворюється від назви відповідного алкану (нумерація ланцюжка від атома Карбону карбоксильної групи) додаванням префікса аміно-, суфікса –ова і слова кислота. Традиційна номенклатура: до назви відповідної карбонової кислоти додають префікс аміно-, а місце аміногрупи позначають літерами ά, β, γ, δ тощо. Для амінокислот, що входять до складу білків, використовують тривіальні назви, причому скорочені, в тому числі у латинському написанні. НОМЕНКЛАТУРАКожна із двадцяти стандартних, і багато нестандратних, амінокислот мають тривіальні назви. Частина цих назв пов'язана із джерелами, з яких вперше було виділено сполуку: наприклад, аспарагін виділений зі спаржі (лат. Asparagus), глутамін — з глютену пшениці, тирозин — із сиру (сир грецькою tyros). Для скороченого запису протеїногенні амінокислоти позначають трибуквенним кодом, використовуючи перші три літери тривіальної назви (за винятком аспарагіну (Асн), глутаміну (Глн), ізолейцину (Іле) і триптофану (Трп), для останнього використовують також скорочення «три»).
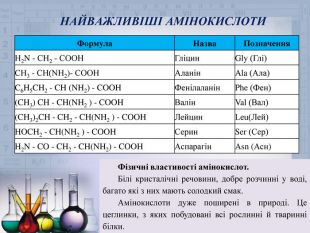
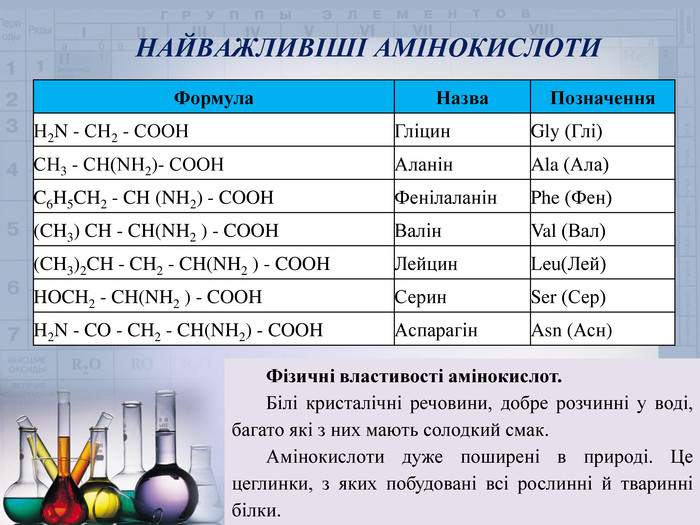
Формула. Назва. Позначення. Н2 N - СН2 - СООНГліцин. Gly (Глі)СН3 - СН(NH2)- СООНАланін. Ala (Ала)C6 H5 CH2 - CH (NH2) - COOHФенілаланін. Phe (Фен)(CH3) CH - CH(NH2 ) - COOHВалін. Val (Вал)(CH3)2 CH - CH2 - CH(NH2 ) - COOHЛейцин. Leu(Лей)HOCH2 - CH(NH2 ) - COOHСерин. Ser (Сер)H2 N - CO - CH2 - CH(NH2) - COOHАспарагін. Asn (Асн)Фізичні властивості амінокислот. Білі кристалічні речовини, добре розчинні у воді, багато які з них мають солодкий смак. Амінокислоти дуже поширені в природі. Це цеглинки, з яких побудовані всі рослинні й тваринні білки. НАЙВАЖЛИВІШІ АМІНОКИСЛОТИ
ХІМІЧНІ ВЛАСТИВОСТІ АМІНОКИСЛОТРеакції за участю карбоксильної групи - кислотні властивостіПодібно до карбонових кислот, амінокислоти реагують з оксидами металів, основами, солями слабких кислот, амоніаком, спиртами. H2 N - СН2 – СООН + Nа. OH → H2 N - СН2 – СООNa + Н2 О натрій аміноацетат (сіль) 2 H2 N - СН2 – СООН +Cu(OH)2 →(H2 N - СН2 – СОО)2 Cu +2 H2 O купрум(ІІ) аміноацетат Якісна реакція на α - амінокислоти : утворюється речовина синього кольору.
Хімічні властивості амінокислот. Реакції за участю аміногрупи – основні властивостіПодібно до амінів (основ), амінокислоти реагують з кислотами H2 N - СН2 – СООН + НCl → [H3 N - СН2 – СООН]Cl гліциній хлорид (сіль)Реакції між амінокислотами – утворення поліпептидів. H2 N-СН2–СООН + H2 N-СН2–СООН →H2 N-СН2–СО-NН-СН2–СООН + Н2 О
Фрагменти молекул амінокислот, що утворюють пептидний ланцюг, називаються кислотними залишками,а зв'язок СО – NH ̶ пептидним зв'язком. За допомогою пептидного зв'язку із залишків амінокислот утворюється поліпептиди — білки. Таких амінокислот, з яких утворюються білки, лише 20 їх називають незамінні, так як вони не утворюються в організмі,а мають потрапити лише з їжею.
ЗАГАЛЬНА ХАРАКТЕРИСТИКАБілки – це органічні високомолекулярні сполуки, побудовані із залишків амінокислот, об’єднаних пептидними зв’язками. В організмі людини налічується близько п'яти мільйонів різноманітних білків, які складають 15- 20% маси тіла. Молекули білка виконують в організмі багато різноманітних функцій: каталітичну, структурну, захисну, запасаючу, регуляторну, сигнальну, транспортну, рецепторну, моторну.
ФУНКЦІЇ БІЛКІВØ каталітична – ферментативна – пепсин, трипсин; Ø структурна – кератин рогових покривів, колаген сполучної тканини, еластин; Ø рухова – актин та міозин м’язових волокон; Ø транспортна – гемоглобін, міоглобін; Ø регуляторна – гормони інсулін (51 амінокислота), вазопресин (9), соматотропін (190); Ø захисна – антитіла, інтерферон; Ø енергетична – 17 к. Дж енергії виділяється з 1 г білку; Ø рецепторна – передача нервового імпульсу.
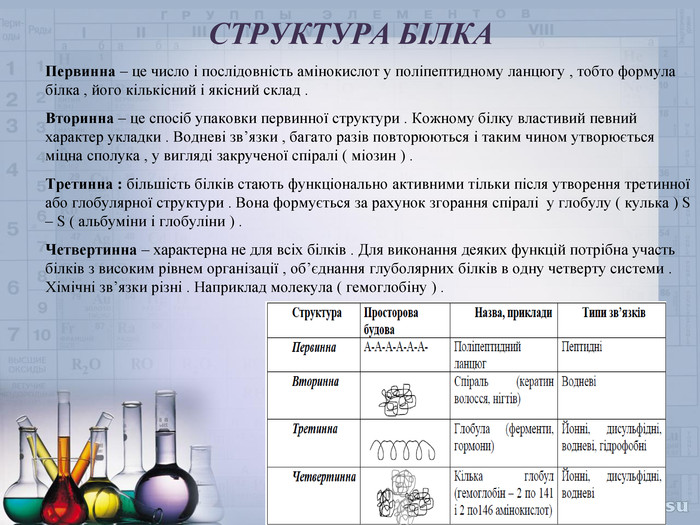
СТРУКТУРА БІЛКАПервинна – це число і послідовність амінокислот у поліпептидному ланцюгу , тобто формула білка , його кількісний і якісний склад . Вторинна – це спосіб упаковки первинної структури . Кожному білку властивий певний характер укладки . Водневі зв’язки , багато разів повторюються і таким чином утворюється міцна сполука , у вигляді закрученої спіралі ( міозин ) . Третинна : більшість білків стають функціонально активними тільки після утворення третинної або глобулярної структури . Вона формується за рахунок згорання спіралі у глобулу ( кулька ) S – S ( альбуміни і глобуліни ) . Четвертинна – характерна не для всіх білків . Для виконання деяких функцій потрібна участь білків з високим рівнем організації , об’єднання глуболярних білків в одну четверту системи . Хімічні зв’язки різні . Наприклад молекула ( гемоглобіну ) .
ХІМІЧНІ ВЛАСТИВОСТІ БІЛКІВ1. Гідроліз (відбувається під впливом ферментів або кислот, які руйнують пептидні зв’язки, в такій послідовності: білок – поліпептид – дипептид – амінокислота) NH2-CH2-CONH-CH2-COOH + HOH →NH2-CH2-COOH + NH2-CH2-COOH 2. Денатурація – руйнування ІІ, ІІІ, IV структури білка, що веде до втрати його функцій. Можливий зворотній процес – ренатурація – відновлення структури білка. Денатурацію спричиняють: температура сильні кислоти, луги, солі важких металів (свинець, ртуть, цинк, мідь) спирт струшування радіація.
ХІМІЧНІ ВЛАСТИВОСТІ БІЛКІВ3. Кольорові реакції білків (якісні реакції): a) ксантопротеїнова (для білків, що містять бензольне кільце): білок + нітратна кислота(конц.) = жовте забарвлення при нагріванні; b) біуретова (виявляю пептидні зв’язки): білок + луг + купрум (ІІ) сульфат = фіолетове забарвлення
ЗНАЧЕННЯ АМІНОКИСЛОТ20 α - амінокислот входять до складу білків, причому 8 з них належать до незамінних. Хворим або виснаженим людям іноді вводять амінокислоти у кров для підтримки сил організму. Деякі амінокислоти являються ліками. Синтетичні амінокислотами підгодовують сільськогосподарських тварин.
Біологічна роль амінокислот. Валін. Один з головних компонентів в рості і синтезі тканин тіла. Основне джерело - тваринні продукти. Досліди на лабораторних щурах показали, що валін підвищує м’язову координацію і знижує чутливість організму до болю, холоду та спеки. Гістидин. Амінокислота, сприяє росту і відновленню тканин. У великій кількості міститься в гемоглобіні; використовується при лікуванні ревматоїдних артритів, алергій, виразок і анемії. Недолік гістидину може викликати ослаблення слуху.Ізолейцин. Постачається усіма продуктами, що містять повноцінний білок - м'ясом, птицею, рибою, яйцями, молочними продуктами. Лейцин. Одна з незамінних" амінокислот. Поставляється усіма продуктами, що містять повноцінний білок - м'ясом, птицею, рибою, яйцями, молочними продуктами. Необхідна не тільки для синтезу протеїну організмом, але й для зміцнення імунної системи. Лізин. Гарні джерела - сир, риба. Одна з важливих складових у виробництві карнітину. Забезпечує належне засвоєння кальцію; бере участь в утворенні колагену (з якого потім формуються хрящі і сполучні тканини); бере активну участь у виробленні антитіл, гормонів і ферментів. Недавні дослідження показали, що лізин, покращуючи загальний баланс поживних речовин, може бути корисний при боротьбі з герпесом. Недолік може виражатися в підвищеній втомлюваності, нездатності до концентрації, дратівливості, пошкодження судин очей, втрати волосся, анемії і проблем в репродуктивної сфері.
Метіонін. Добрі джерела - зернові, горіхи та злакові. Важливий в метаболізмі жирів і білків, організм використовує її також для виробництва цистеїну. Є основним постачальником сульфуру, який запобігає розлади у формуванні волосся, шкіри та нігтів; сприяє зниженню рівня холестерину, підсилюючи вироблення лецитину печінкою; знижує рівень жирів у печінці, захищає нирки; бере участь у виведення важких металів з організму; регулює утворення аміаку і очищає від нього сечу, що знижує навантаження на сечовий міхур; впливає на цибулини волосся і підтримує зростання волосся. Треонін. Важлива складова в синтезі пуринів, які, у свою чергу, розкладають сечовину, побічний продукт синтезу білка. Важлива складова колагену, еластину і протеїну емалі, бере участь у боротьбі з відкладенням жиру в печінці; підтримує більш рівну роботу травного і кишкового трактів; приймають загальну участь у процесах метаболізму і засвоєння. Триптофан. Є первинним по відношенню до ніацин (вітаміну В) і серотоніну, який, беручи участь в мозкових процесах управляє апетитом, сном, настрою і больовим порогом. Природний релаксант, допомагає боротися з безсонням, викликаючи нормальний сон, допомагає боротися зі станом неспокою і депресії. Фенілалаін. Використовується організмом для виробництва тирозину і трьох важливих гормонів - епінерфіна, норепінерфіна і тироксину. Використовується головним мозком для виробництва Норепінерфіна, речовини, яка передає сигнали від нервових клітин до головного мозку; підтримує нас в у стані неспання і сприйнятливості. Біологічна роль амінокислот
Тирозин. Використовується організмом замість фенілаланіну при синтезі білка. Джерела - молоко, м'ясо, риба. Мозок використовує тирозин при виробленні норепінерфіна, що підвищує ментальний тонус. Багатообіцяючі результати показали спроби використовувати тирозин як засіб боротьби з втомою і стресами. Цистин (цистеїн). Якщо в раціоні достатню кількість цистину, організм може використовувати його замість метіоніну для виробництва білка. Гарні джерела цистину - м'ясо, риба, соя, овес і пшениця. Цистин використовують в харчовій промисловості як антиоксидант для збереження вітаміну С у готових продуктах. Аланін. Є важливим джерелом енергії для м'язових тканин, головного мозку та центральної нервової системи; зміцнює імунну систему шляхом вироблення антитіл; активно бере участь у метаболізмі цукру і органічних кислот. Аргінін. Викликає уповільнення розвитку пухлин і ракових утворень. Очищає печінку. Допомагає виділення гормону росту, зміцнює імунну систему, сприяє виробленню сперми і корисна при лікуванні розладів і травм нирок. Також корисний при розладах печінки, таких, як цироз. Біологічна роль амінокислот
Аспарагін. Аспартова кислота. Бере активну участь у виведенні аміаку, шкідливого для центральної нервової системи. Недавні дослідження показали, що аспартова кислота може підвищувати стійкість до втомлюваності. Карнітин. Карнітин допомагає зв'язувати і виводити з організму довгі ланцюжки жирних кислот. Печінка і нирки виробляють карнітин з двох інших амінокислот - глютаміну і метіоніну. У великій кількості поставляється в організм м'ясом і молочними продуктами.. Вважається, що для найкращої утилізації жиру денна норма карнітину повинна становити 1500 міліграмів. Орнітин. Орнітин сприяє виробленню гормону росту. Необхідний для роботи печінки та імунної системи. На додаток до синтезу білків, стандартні і нестандартні амінокислоти в тваринному організмі виконують багато інших важливих біологічних функцій. Гліцин та глутамат (аніон глутамінової кислоти) використовуються як нейромедіатори при нервовій передачі через хімічні синапси, нейромедіаторами також є нестандартна амінокислота гамма-аміномасляна кислота, що є продуктом декарбоксилювання глутамату, дофамін — похідне тирозину, і серотонін, який утворюється із триптофану. Гістидин є попередником гістаміну – локального медіатора запальних і алергічних реакцій. Йодовмісний гормон щитоподібної залози тироксин утворюється із тирозину. Гліцин є одним із метаболічних попередників порфіринів (таких як дихальний пігмент гем)Біологічна роль амінокислот
Біологічна роль білків. Білки бувають: a. Прості (протеїни) – складаються лише з амінокислот b. Складні (протеїди) – містять жири (ліпопротеїни), вуглеводи (глікопротеїни), фосфопротеїни. Багаті на білок такі харчові продукти: сир та молочні продукти, м'ясо, риба, яйця, горіхи, бобові рослини. Добова норма людини – 90 г білків.
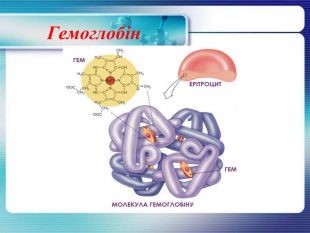
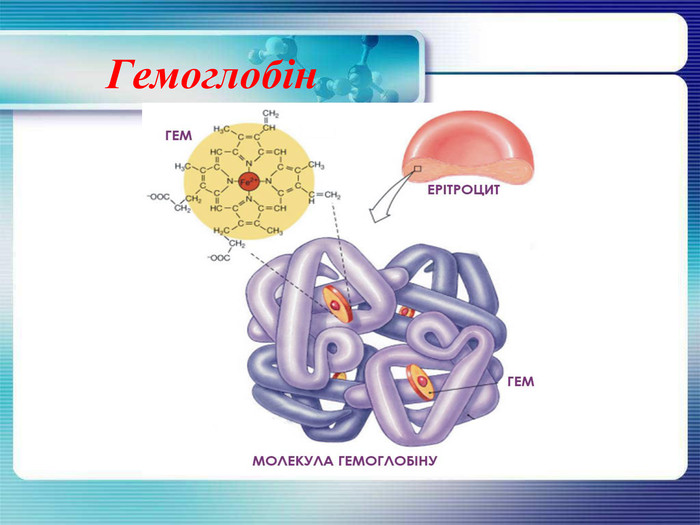
Гемоглобін Гемоглобін – складний білок , що має четвертинну структуру, містить залізо і здатний зв'язуватися з киснем, забезпечуючи його перенесення до тканин. У людини та інших хребетних тварин він міститься в еритроцитах. Чадний газ (CO) зв'язується з гемоглобіном крові в 250 разів сильніше, ніж кисень, утворюючи карбоксигемоглобін (Hb. CO). В такому випадку блокуються процеси транспортування кисню, людина задихається і може померти.
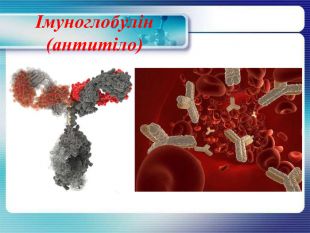
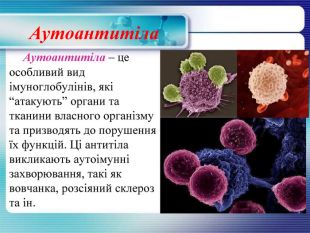
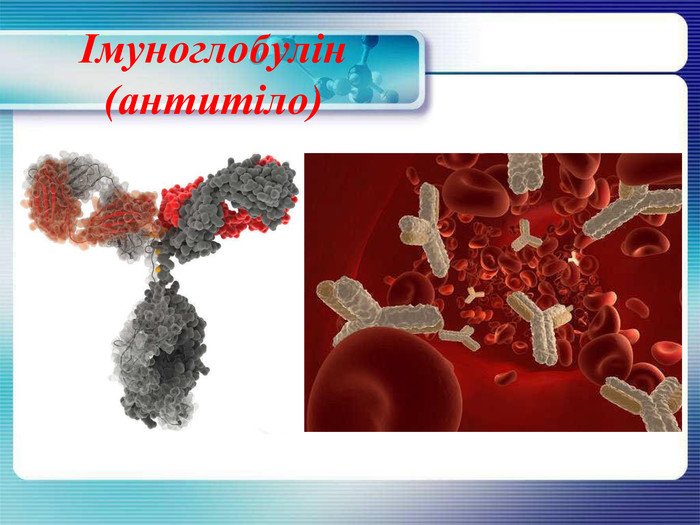
Імуноглобулін Антитіла або імуноглобуліни— білкові сполуки, які організм людини виробляє у відповідь на чужорідні речовини, що потрапляють до організму з метою знищити або нейтралізувати потенційно небезпечні з них — бактерії, віруси, отрути та деякі інші речовини. Імуноглобуліни містяться в сироватці крові. Є декілька типів антитіл. Одні з них безпосередньо викликають загибель збудників інфекції, інші – знешкоджують токсини, які виробляються ними. Треті – лише сигналізують про виявлення паразитів та збудників інфекцій
Інсулін Інсулін — гормон, що утворюється у клітинах, що знаходяться у хвості підшлункової залози. Основна дія інсуліну - зниження концентрації глюкози в крові. Цей гормон також впливає на багато аспектів обміну речовин практично у всіх тканинах. Інсулін збільшує проникність мембран клітини для глюкози, стимулює перетворення глюкози на глікоген в печінці і м'язах, підсилює синтез жирів і білків.
Колаген Колаген - фібрилярний білок, що становить основу сполучної тканини організму (сухожиль, кісток, хрящів, дерми), забезпечує їх міцність та еластичність. Колаген є найпоширенішим білком у людини, що становить від 25% до 35% білків всього організму. Порушення синтезу колагену в організмі лежить в основі таких спадкових захворювань, як «хвороба скляної людини», вроджений рахіт, вроджена ламкість кісток. Характерним проявом цих захворювань є пошкодження хрящів, кісткової системи, наявність вад серцевих клапанів.
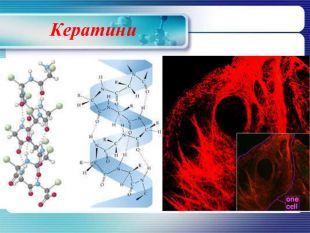
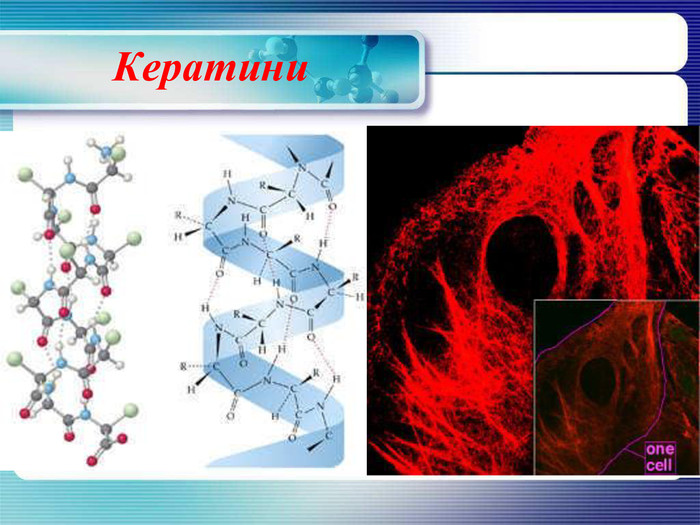
Кератини Кератини — сімейство фібрилярних білків, які характеризує механічна міцність. Переважно з кератинів складаються рогові похідні епідермісу шкіри: волосся, нігті, роги, пір'я, дзьоб птахів та інші. Також існують цитокератини, що утворюють елементи цитоскелету клітини. Кератин надає шкірі пружність і міцність. Тертя і тиск спричиняють більш інтенсивне виділення кератину клітинами з метою захисту, в результаті чого виникають мозолі. Кератизовані клітини епідермісу безперервно злущуються і заміщуються, виникає лупа.
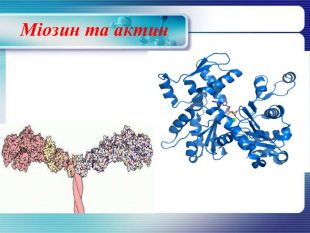
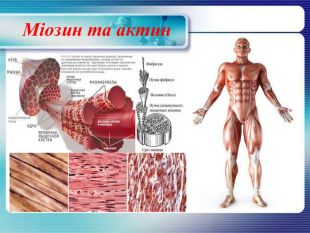
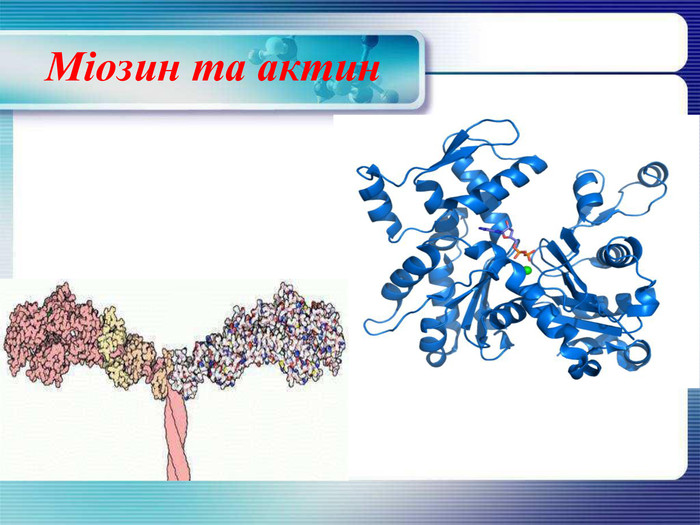
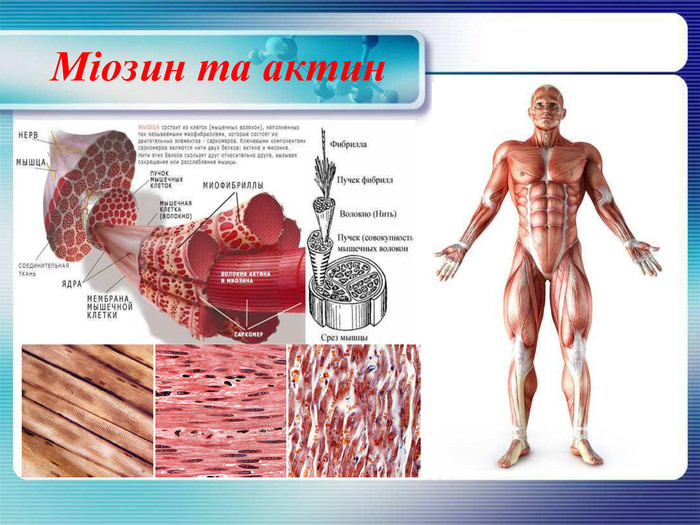
Міозин та актин Міозин - фібрилярний білок, один з головних компонентів скорочувальних волокон м'язів - міофібрил. Становить 40-60% загальної кількості м'язових білків організму людини. Міозин також здатний розщеплювати АТФ кислоту, завдяки чому виникає механічна енергія м’язових скорочень. Актин — білок м'язової тканини, що вступає в комплекс з міозином утворюючи актоміозин. Обидва білки відграють важливу роль в утворенні цитоскелета клітин.
Домашнє завдання1. Опрацювати презентацію та §33. Повторити амінокислоти, зробити конспект презентації 15-19 слайдів, з іншими слайдами ознайомитись.2. Виконати завдання №242,247. №242 оформити в форматі Word.3. Підготуватись до контрольної роботи за темою «Оксигеновмісні. Нітрогеновмісні сполуки». УВАГА! Контрольна робота буде розміщенна 28.04.2021, час на виконання 45 хв (з 11.15 до 12.00), далі буде закритий допуск. В разі неможливості виконання з різних причин – попередьте.
-
 Горбанева Ольга 03.05.2024 в 06:16Загальна:5.0Структурованість5.0Оригінальність викладу5.0Відповідність темі5.0
Горбанева Ольга 03.05.2024 в 06:16Загальна:5.0Структурованість5.0Оригінальність викладу5.0Відповідність темі5.0 -
 Sereda Tatyana 16.05.2022 в 14:08Дякую за змістовний, інтегрований, цікавий матеріал!Загальна:5.0Структурованість5.0Оригінальність викладу5.0Відповідність темі5.0
Sereda Tatyana 16.05.2022 в 14:08Дякую за змістовний, інтегрований, цікавий матеріал!Загальна:5.0Структурованість5.0Оригінальність викладу5.0Відповідність темі5.0


про публікацію авторської розробки
Додати розробку