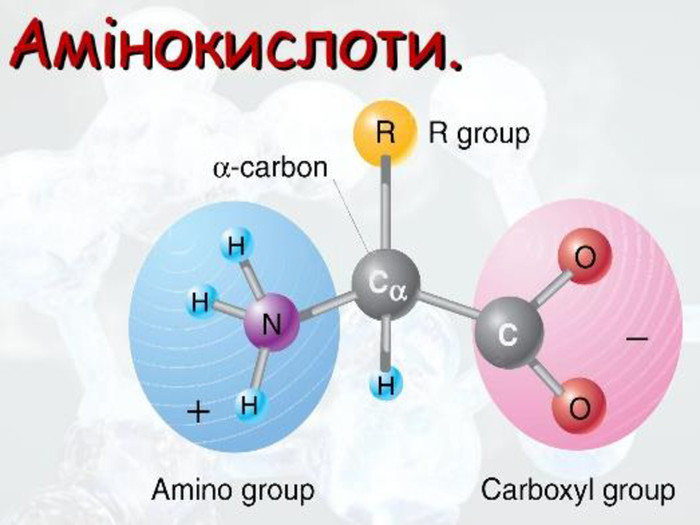
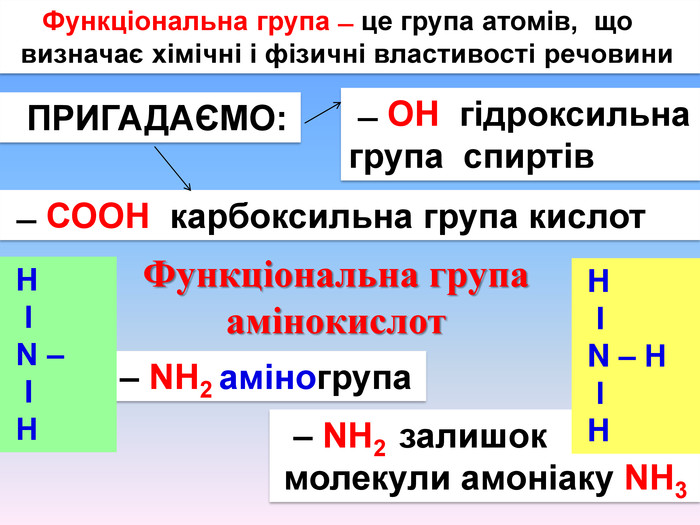
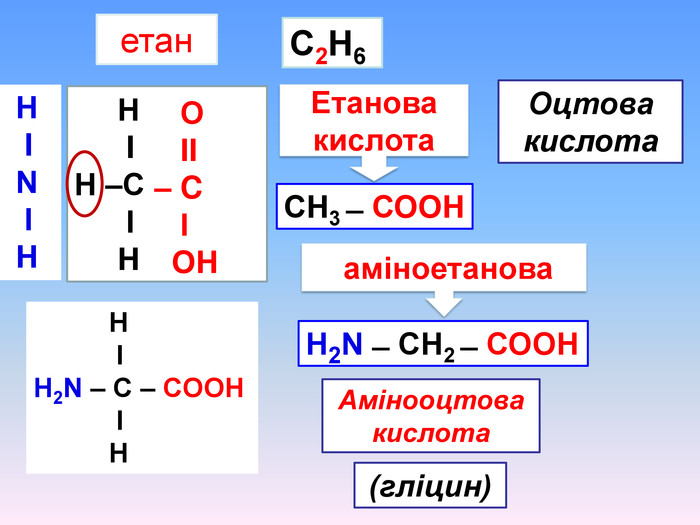
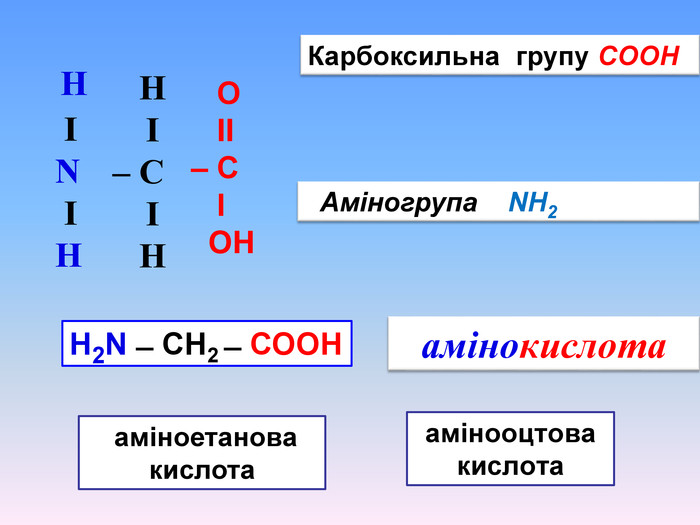
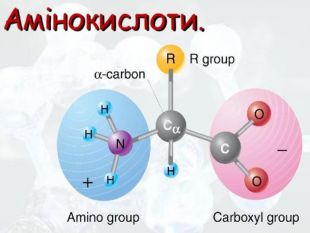
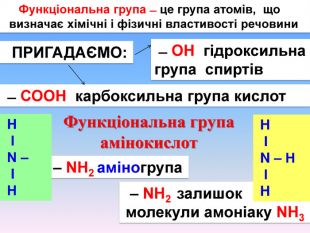
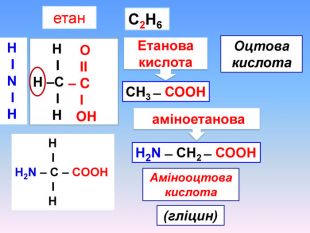
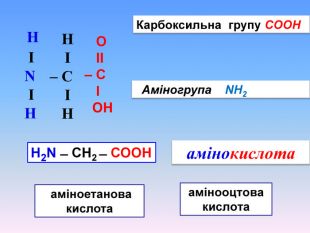
Амінокислоти будова, властивостивості
Про матеріал
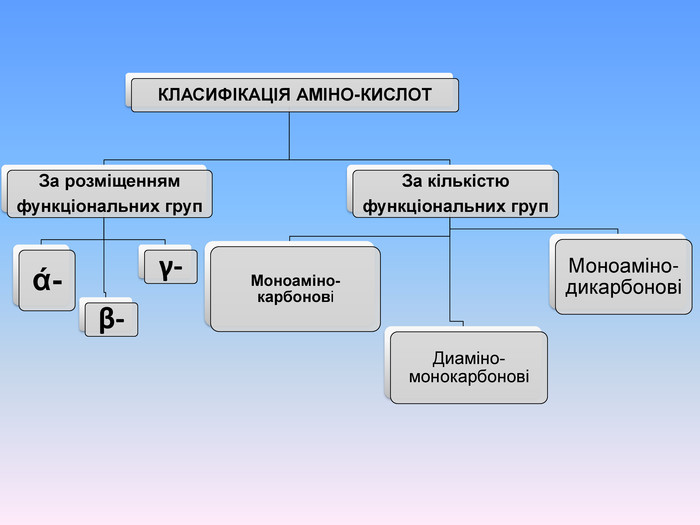
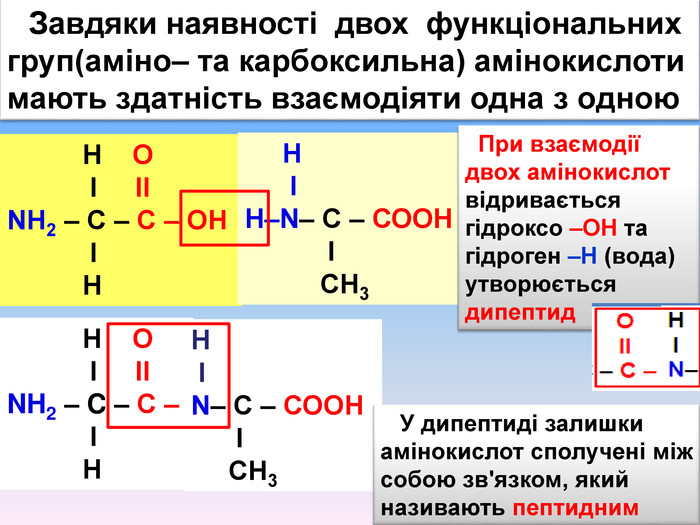
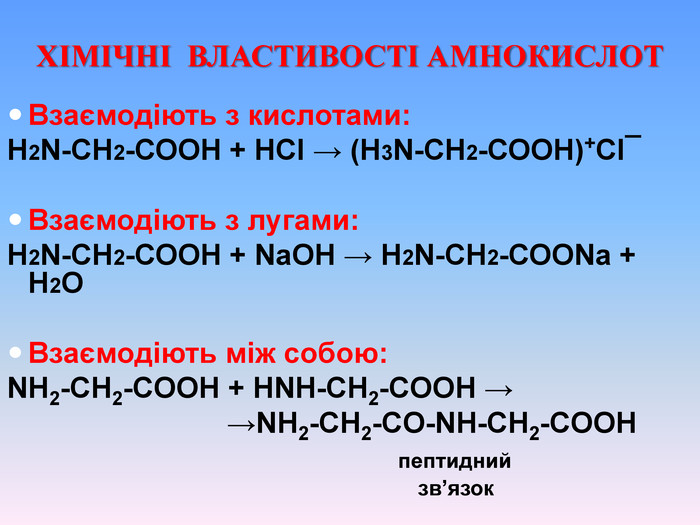
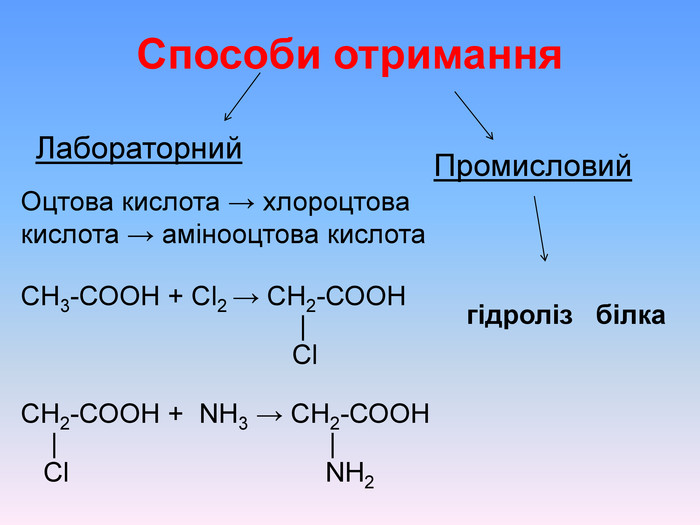
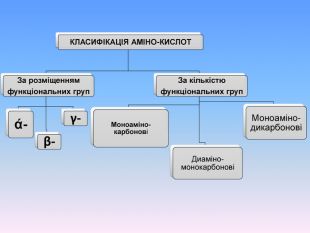
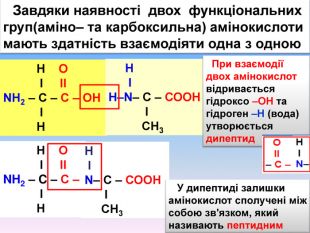
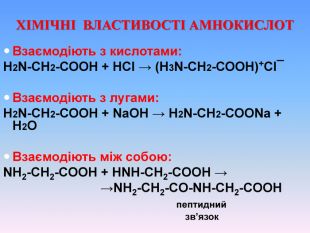
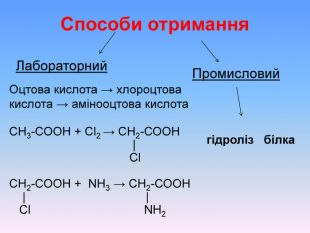
Презентаційний матеріал про будову, типи зв`язків, утворення зв`язків, фізичні та хімічні властивості амінокислот. Перегляд файлу
Зміст слайдів


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку