Діагностичні роботи з хімії 7 клас
НОВА УКРАЇНСЬКА ШКОЛА

Діагностичні роботи
ЗА МОДЕЛЬНОЮ ПРОГРАМОЮ «ХІМІЯ 7-9 КЛАСИ» для закладів загальної середньої освіти (авт..Григорович О.В.)
Підручник: Хімія: підручник для 7 класу загальноосвітніх навчальних закладів / Мідак Лілія . – Тернопіль: «Астон», 2024.
Підготувала Денисюк Юлія Іванівна
Компетентнісний потенціал курсу «Хімія. 7–9 класи»
|
Ключові компетентності |
Уміння та ставлення в курсі хімії |
|
Вільне володіння державною мовою |
Уміння:
та технічного змісту щодо тем, які потребують пошуку додаткової інформації під час виконання проєктів дослідницького характеру;
|
|
|
Ставлення: – повага до державної мови, усвідомлення її значення для здійснення різних видів комунікації. |
|
Здатність спілкуватися рідною (у разі відмінності від державної) та іноземними мовами |
Уміння:
Ставлення:
у природничій галузі для зарубіжної спільноти іноземними мовами. |
|
Математична компетентність |
Уміння: – оперувати математичними поняттями і величинами під час характеристики природних об’єктів, явищ і технологічних процесів; |
|
|
Ставлення:
|
|
Компетентності в галузі природничих наук, техніки і технологій |
Уміння:
Ставлення:
|
|
Інноваційність |
Уміння: – описувати тенденції розвитку природничих наук, техніки і технологій; |
|
|
Ставлення:
|
|
Екологічна компетентність |
Уміння:
Ставлення:
|
|
|
|
|
Інформаційно- комунікаційна компетентність |
Уміння:
Ставлення:
однокласників / однокласниць. |
|
Навчання впродовж життя |
Уміння:
Ставлення:
|
|
Громадянські та соціальні компетентності |
Уміння:
|
|
|
Ставлення:
|
|
Культурна компетентність |
Уміння: – застосовувати досягнення природничих наук і технологій, технічних засобів для втілення мистецьких ідей; |
|
|
Ставлення:
|
|
Підприємливість і фінансова грамотність |
Уміння:
Ставлення:
конкретних прикладах із використанням результатів власної проєктної діяльності. |
Діагностична робота. Тема 1. Хімія. Перші кроки.
Завдання 1- 6 з однією правильною відповіддю (кожне завдання по 0,5 б, разом 3 бали)
- Наука про властивості речовин та їх перетворення: а) фізика; б) хімія; в) біологія; г) екологія.
- Найвідоміший винахід Альфреда Нобеля, який мав велике значення для будівництва і військової справи: а) вугілля; б) динаміт; в) гіпс; г) крейда.
- Становлення хімії, як науки розпочалося у: а) Давньому Єгипті; б) Греції; в) Франції; г) Україні.
-
Що означає знак
 ? а) легкозаймиста речовина; б) обережно, пожежа! в) небезпека вибуху; г) отрута.
? а) легкозаймиста речовина; б) обережно, пожежа! в) небезпека вибуху; г) отрута.
- Фізична величина, що є мірою інертності: а) густина; б) об’єм; в) маса; г) температура.
- Метод наукового пізнання, у якому вивчення тіл і явищ відбувається в доцільно вибраних або штучно створених умовах: а) теорія; б) гіпотеза; в) експеримент; г) моделювання.
|
1 |
2 |
3 |
4 |
5 |
6 |
|
|
|
|
|
|
|
Завдання 7 Вставити пропущені слова (3бали)
- Виконуйте лише ті хімічні досліди, які погоджені з _________.
- Дотримуйтеся _________поводження з реактивами, хімічним посудом, лабораторним обладнанням.
- Під час нагрівання розчинів у пробірці користуйтеся _________.
Завдання 8 Встановлення відповідності (3 бали)
8.Виберіть лабораторний посуд і його призначення:
|
1. |
А. Призначена для демонстрацій реакцій, фільтрування, випарювання |
|
2. |
Б. Призначена для переливання рідини в посуд |
|
3. |
В. Призначений для розміщення у ньому пробірок |
|
4. |
Г. Призначена для здійснення хімічний реакцій у невеликих кількостях |
|
5. |
Д. Використовують для вимірювання об’єму рідини. |
|
6. |
Е. Застосовують для випарювання розчинів |
|
1 |
2 |
3 |
4 |
5 |
6 |
|
|
|
|
|
|
|
Завдання 9. Підпишіть складові частини спиртівки (3 бали)
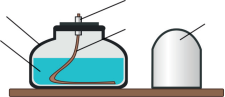
Запишіть правила роботи зі спиртівкою.__________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________

Оцінка
Діагностична робота. Тема 2. Від хімічних елементів до хімічних сполук.
Завдання 1- 6 з однією правильною відповіддю (кожне завдання по 0,5 б, разом 3 бали)
- Найменша хімічно неподільна електронейтральна частинка : а) атом; б) молекула; в) речовина; г) тіло.
- Вид атомів з однаковим зарядом ядра: а) хімічний елемент; б) тіло; в) речовина; г) хімічний символ.
- Символи хімічних елементів складаються з однієї або двох літер
і походять від їхніх назв: а) єгипетських; б) грецьких; в) латинських; г) українських.
- Горизонтальний ряд в періодичній системі називається: а) ряд; б) група; в) період; г) символ.
- На сьогодні відомо хімічних елементів: а) 116; б) 118; в) 120; г) 122..
- Виберіть металічний елемент; а) Літій; б) Оксиген ; в) Гідроген; г) Нітроген.
|
1 |
2 |
3 |
4 |
5 |
6 |
|
|
|
|
|
|
|
Завдання 7 Спробуйте відновити інформацію (3бали)
|
Символ |
Назва хімічного елементу |
Проста речовина |
|
О |
|
Кисень |
|
|
Гідроген |
|
|
Cu |
|
Мідь |
|
|
Карбон |
|
|
Fe |
|
Залізо |
|
|
Нітроген |
|
Завдання 8 Випишіть окремо формули простих і складних речовин (3 бали)
CaO, Cl2, N2, H2O, Au, HCl.
|
Прості речовини |
Складні речовини |
|
|
|
Завдання 9. Вкажіть якісний і кількісний склад таких речовин (3 бали)
|
Формула речовини |
Якісний склад |
Кількісний склад |
|
H2O |
|
|
|
NaCl |
|
|
|
H2SO4 |
|
|
Запишіть формулу речовини за її вимовою:
- Аш – три-пе-о-чотири _______________
- Ен- аш – три.__________________________
- Алюміній-два-о-три.____________________

Оцінка
Діагностична робота. Тема 3. Досліджуємо речовини та суміші.
Завдання 1- 6 з однією правильною відповіддю (кожне завдання по 0,5 б, разом 3 бали)
- Характеристики речовини, які не пов’язані зі зміною її хімічного складу: а) фізичні; б) хімічні; в) молекулярні; г) біологічні.
- До фізичних властивостей речовин належать: а) агрегатний стан; б) колір; в) розчинність у воді; г) всі перераховані варіанти.
- Чистою речовиною є: а) джерельна вода; б) газована вода; в) повітря; г) молоко.
- Розчин цукру у воді – це суміш; а) суспензія; б) аерозоль; в) однорідна; г) неоднорідна.
- Воду і кухонну сіль можна розділити способом: а) фільтрування; б) відстоювання; в) випаровування; г) перегонка.
- Масова частка компонентів у суміші позначається; а) W; б) m; в) V; г) g.
|
1 |
2 |
3 |
4 |
5 |
6 |
|
|
|
|
|
|
|
Завдання 7 Вставити пропущені слова (3бали)
- Масова частка компонента в суміші — це відношення ________ цього компонента до _______ суміші.
- До складу розчину входить розчинник і ___________ __________.
- Неоднорідні суміші можна розділити способами: ______________, дія магніту і ______________.
Завдання 8 Встановлення відповідності (3 бали)
8.Виберіть суміш і спосіб її розділення:
|
1. Суміш спирту і води |
А. Дія магніту |
|
2. Суміш кухонної солі і води |
Б. Перегонка |
|
3. Суміш піску і залізних ошурок |
В. Відстоювання |
|
4. Суміш олії і води |
Г. Випарювання |
|
1 |
2 |
3 |
4 |
|
|
|
|
|
Завдання 9. Спробуйте відновити інформацію (3бали)
Заповніть пропущені клітинки, зробивши відповідні розрахунки.
|
№ п/п |
Маса компонента 1, г |
Маса компонента 2, г |
Маса суміші, г |
Масова частка компонента 1 в суміші, % |
|
1 |
12 |
|
65 |
|
|
2 |
|
95 |
120 |
|
|
3 |
|
55 |
|
15 |

Оцінка
Діагностична робота. Тема 4. Моделюємо фізичні та хімічні явища.
Завдання 1- 6 з однією правильною відповіддю (кожне завдання по 0,5 б, разом 3 бали)
- Явища, під час перебігу яких не відбуваються зміни хімічного складу речовин: а) фізичні; б) хімічні; в) географічні; г) біологічні.
- До фізичного явища належить: а) спалювання деревини; б) скисання молока; в) випаровування води; г) іржавіння заліза.
- Хімічним явищем є: а) спалювання деревини; б) поширення запаху; в) випаровування води; г) утворення туману.
- Речовини, які утворюються в результаті реакції ; а) реагенти; б) продукти реакції; в) суміші; г) компоненти.
- У схемі реакції Mg + Cl2 = MgCl2 продуктом реакції є : а) Mg; б) Cl2; в) MgCl2; г) 2.
- Реакції, під час яких з одного реагента утворюються два і більше називаються ; а) сполучення; б) заміщення ; в) обміну; г) розкладу.
|
1 |
2 |
3 |
4 |
5 |
6 |
|
|
|
|
|
|
|
Завдання 7 Вставити пропущені слова (3бали)
- Хімічне рівняння — це запис хімічної реакції за допомогою _________ _________ реагентів і продуктів, який відповідає закону збереження маси речовин.
- Закон збереження читається: Маса вихідних речовин (реагентів) дорівнює _________ __________ реакції.
- Ознакою реакції взаємодії соди і оцту є _________ _____.
Завдання 8 Встановлення відповідності (3 бали)
8.Встановіть відповідність між схемою реакції і її типом:
|
1. MgO + 2HCI →MgCl2 + H2O |
А. Заміщення |
|
2. 2СаО → 2Са + О2 |
Б. Сполучення |
|
3. СаО + СО2 → СаСО3 |
В. Обміну |
|
4. 2Na + 2H2O → 2NaOH + H2↑ |
Г. Розкладу |
|
1 |
2 |
3 |
4 |
|
|
|
|
|
Завдання 9. Спробуйте відновити інформацію (3бали)
Перетворіть схеми реакцій на хімічні рівняння
Аg + Сl2 → АgСl
СuО + Н2 → Сu + Н2O
Mg +Ν2 → Мg3N2
КСlО3 → КСl + О2
Na + H2O → NaOH + H2
B + S → B2S3

Оцінка
На допомогу для учня !!!
Хімічна формула

![]()
Масова частка речовини у розчині

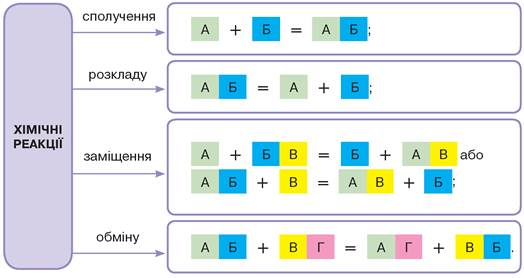
Типи хімічних реакцій




про публікацію авторської розробки
Додати розробку



-

Перевозникова Наталія
13.10.2025 в 15:43
Дякую колегам, які витрачають час та свої здібності та надають у використання свої розробки.
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Година Дмитро
06.05.2025 в 19:42
Дуже гарно я у захваті
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Полуда Тетяна Олександрівна
21.04.2025 в 09:10
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Лукша Дарія Олександрівна
19.03.2025 в 17:26
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Чепак Галина Олександрівна
05.12.2024 в 18:01
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Мандзюк Лідія
03.12.2024 в 11:35
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Сулік Оксана Петрівна
02.12.2024 в 21:51
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

B Olesya
29.11.2024 в 21:24
Загальна:
4.0
Структурованість
4.0
Оригінальність викладу
4.0
Відповідність темі
4.0
-

Ірина Грабовецька
10.11.2024 в 20:39
Дякую!
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
Показати ще 6 відгуків