Екологічний проєкт «Використання природних індикаторів із навчально-дослідною метою»
ТЕМА: Використання природних індикаторів із навчально-дослідною метою.
МЕТА: Приготувати розчини рослинних індикаторів у домашніх умовах. Дослідити зміни забарвлення пігментів рослин у різних середовищах.
ГІПОТЕЗА ДОСЛІДЖЕННЯ: рослини володіють індикаторними властивостями, які можна використати в різних сферах.
ОБ’ЄКТ ДОСЛІДЖЕННЯ: рослини, соки яких володіють властивостями індикаторів.
ПРЕДМЕТ ДОСЛІДЖЕННЯ: розчини природних індикаторів із плодів і ягід.
ЗАВДАННЯ:
1. Вивчити літературні джерела з теми.
2. Розглянути класифікацію індикаторів.
3. Охарактеризувати основні рослинні барвники.
4. Виділити із природної сировини речовини, які мають здатність за
певних умов змінювати свій колір, виготовити їх розчини.
5. Провести дослідження з визначення зміни забарвлення отриманих розчинів залежно від середовища.
6. Визначити рослинні індикатори , які можна використати для визначення реакції середовища.
МЕТОДИ ДОСЛІДЖЕННЯ: аналіз, синтез, порівняння, хімічний експеримент.
ТИПИ ІНДИКАТОРІВ: кислотно – основні.
АКТУАЛЬНІСТЬ ТЕМИ: зріс інтерес до рослин в зв'язку з їх застосуванням в різних областях науки, таких як хімія, біологія, екологія і медицина. Природні індикатори екологічні, прості в використанні, доступні, можуть бути використані в побуті для визначення рН середовища.
ЗМІСТ
ВСТУП 3
РОЗДІЛ 1. Рослинні барвники, їх характеристика
1.1. Основні групи пігментів та їх характеристика 5
1.2. Антоциани і їх властивості 7
РОЗДІЛ 2. Індикатори. Загальні поняття, класифікація
2.1. Характеристика кислотно-основних індикаторів 9
2.2. Відкриття природних індикаторів 10
РОЗДІЛ 3. Експериментально-дослідницька частина:
3.1. Методика виготовлення індикаторів з природної сировини 12
3.2. Дослідження властивостей природних індикаторів 14
3.2.1. Зміна кольору природного індикатора в різних середовищах
3.2.2. Вплив концентрації природного індикатора на інтенсивність
кольору розчину 15
ВИСНОВКИ ТА РЕКОМЕНДАЦІЇ 17 СПИСОК ВИКОРИСТАНИХ ДЖЕРЕЛ 18
ДОДАТКИ 19
ВСТУП
Індикатори – це речовини, які змінюють свій колір в залежності від середовища розчину. Значить в плодах рослин, листі містяться природні барвники (пігменти), які під дією лужних розчинів міняють свій колір на синій або фіолетовий, а від дії кислот стають червоними. Виникає питання - що це за природні індикатори, які містяться в плодах і ягодах? І якими властивостями вони володіють?
Слово «індикатор» у перекладі з латини означає «вказівник». Це органічні речовини, які можуть приєднувати йони H+ або OH–. Залежно від того, який йон приєднала молекула індикатора, вона змінює свою структуру. У результаті ми спостерігаємо зміну кольору індикатора. Якщо індикатор містився в розчині — змінюється колір розчину, якщо він був нанесений на папір (індикаторний папір) — змінюється колір індикатора. Легко й зручно змінюється колір індикатора.
Виділені з рослин пігменти – речовини з кольором – були відомі ще в Стародавньому Египті і Римі. Використання органічних речовин в якості індикаторів відомо з ХVІІ століття і пов’язано з іменем видатного англійського вченого фізика і хіміка – Роберта Бойля. Назва «індикатори» походить від латинського слова indicator, що означає «покажчик» ( Роберт Бойль 1640 р).
Найвідоміший рослинний індикатор – лакмус – відвар тропічного лишайника [ 10 ].
Колір рослин визначається хімічним складом клітинного вмісту кожної рослини (пігментом). Пігменти - органічні сполуки, які присутні в клітинах і тканинах рослин та надають їм певного забарвлення. Накопичуються пігменти у корінні, у квітках, у шкірці плодів і в листках рослин. Розташовані пігменти в хлоропластах і хромопластах. Пігменти багатьох рослин здатні змінювати колір залежно від кислотності клітинного соку. Тому пігменти є індикаторами, які можна застосувати для дослідження кислотності розчинів.
Усі пігменти рослин можна розділити на три групи — хлорофіли,
каротиноїди, антоціани. Хлорофіл надає зеленого забарвлення листкам. Без цього смарагдового пігменту неможливе життя на планеті, оскільки він приймає участь у фотосинтезі. Супутниками хлорофілу є каротиноїди, які надають жовте, помаранчеве і червоне забарвлення. Так, жовті зерна кукурудзи, помаранчева шкірка мандарина, червоні плоди шипшини зобов’язані своїм кольором [ 1 ].
Третя група пігментів — антоціани, які надають практично всіх кольори рослинам — від помаранчевого та червоного до синього. Вони мають добре виражені індикаторні властивості.
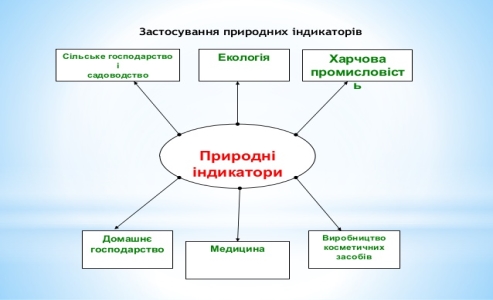
Природні індикатори можуть бути використані у сільському господарстві і садівництві, харчовій промисловості, виробництві косметичних засобів, медицині та домашньому господарстві.
Щоб яка-небудь речовина могла служити індикатором, вона повинна відповідати мінімум трьом умовам:
•має бути слабкою кислотою або слабкою основою;
•її молекули і іони повинні мати різне забарвлення;
•забарвлення її має бути надзвичайно інтенсивним, щоб його можна було помітити при додаванні до досліджуваного розчину навіть малої кількості індикатора [ 4 ].
Недоліки природних індикаторів: їх відвари досить швидко псуються – скисають або пліснявіють, тому частіше використовують більш стійкий спиртовий розчин. Інший недолік – дуже широкий інтервал зміни кольору. При цьому важко або неможливо відрізнити, наприклад, нейтральне середовище від слабо кислого або слабо лужного від сильно лужного. Позитивним моментом є те, що вони екологічно безпечні, і їх можна приготувати і використовувати в домашніх умовах.
РОЗДІЛ 1
Рослинні барвники, їх характеристика
1.1. Основні групи пігментів та їх характеристика
Рослинні барвники або пігменти нагромаджуються головним чином в корінні, квітках, шкірці плодів і в листі рослин.
Усі пігменти рослин можна розділити на три групи — хлорофіли, каротиноїди, антоціани. Хлорофіл надає зеленого забарвлення листкам. Без цього смарагдового пігменту неможливе життя на планеті, оскільки він приймає участь у фотосинтезі. Супутниками хлорофілу є каротиноїди, які надають жовте, помаранчеве і червоне забарвлення. Так, жовті зерна кукурудзи, помаранчева шкірка мандарина, червоні плоди шипшини зобов’язані своїм кольором [ 9 ].
Загальна кількість хлорофілу в листі невелика: близько одного відсотка (на суху вагу). Однак роль його величезна. За допомогою хлорофілу зелений лист поглинає енергію сонячного світла, перетворюючи її в хімічну енергію органічних сполук, які створюються з речовин неорганічної природи – вуглекислоти і води. В результаті складних перетворень в атмосферу виділяється кисень, забезпечуючи можливість життя на землі. Процес цей називається фотосинтезом. Хлорофіл завдяки своїм дивовижним якостям давно привертає увагу вчених різних спеціальностей: біологів, фізиків і хіміків.
К. А. Тімірязєв висловив цікаве припущення (згодом воно було підтверджено експериментально) про спільність хімічної природи червоного пігменту крові (геміну) і хлорофілу. Подібність молекул хлорофілу і геміну крові разюча. Вона дозволяє говорити про хлорофіл як біологічно активну речовину, подібну вітамінам у життєдіяльності тваринного організму.
Третя група пігментів — антоціани, які надають практично всіх кольори рослинам — від помаранчевого та червоного до синього. Вони мають добре виражені індикаторні властивості. Антоціани – барвні речовини (пігменти)
синього, червоного і фіолетового кольору, що містяться в багатьох рослинних клітинах.
Антоціани зумовлюють забарвлення квіток, плодів, стебел, листя. Їхньому нагромадженню в клітинах сприяють світло, низька температура, пошкодження тканин та ін. фактори. Антоціани містять осіннє листя, ягоди винограду, пелюстки квіткових рослин.
Третя група пігментів — антоціани, які надають практично всіх кольори рослинам — від помаранчевого та червоного до синього. Вони мають добре виражені індикаторні властивості. Антоціани – барвні речовини (пігменти)
синього, червоного і фіолетового кольору, що містяться в багатьох рослинних клітинах. Антоціани зумовлюють забарвлення квіток, плодів, стебел, листя. Їхньому нагромадженню в клітинах сприяють світло, низька температура, пошкодження тканин та ін. фактори. Антоціани містять осіннє листя, ягоди винограду, пелюстки квіткових рослин.
1.2. Антоціани і їх властивості
Антоціани (від греч. anthos - колір і ky аnos - лазоревий) - це одні з самих поширених пігментів в рослинному царстві. Група антоціанов найбільш численна і нараховує біля 10 видів. Відома велика кількість природних об'єктів, багаті антоціанами. Це анютині очки, малина, вишня, суниця, краснокочанная капуста, чорниця, журавлина, полуниці, чорний виноград і багато які інші. Вони утворяться в процесах гідролізу крохмаль і за своїм походженням є безазотистими з'єднаннями, близьким до глюкозидів - з'єднанням цукру з невуглеводною частиною.
Будова антоціанів встановлена в 1913 німецьким біохіміком Р. Вільштеттером, перший хімічний синтез здійснений в 1928 англійським хіміком Р. Робінсоном [ 12 ].
Антоціани надають тканинам рослин фіолетову, синю, червону, оранжеву і інші забарвлення. Це забарвлення нерідко залежить від рН клітинного вмісту, і тому може мінятися при дозріванні плодів, відквітанні квіток - процесах, що супроводяться закислением клітинного вмісту [3].
При цьому забарвлення рослин змінюється від зелених до червоних і синіх кольорів. Антоціани добре розчинні у воді і присутні в соку вакуолей. Діапазон кольорів змінюється завдяки наявності в рослинах в основному трьох моделей антоціанів, різних між собою числом гідроксильних груп: пеларгонідін (червоний), ціанідін (фіолетовий) і дельфінідін (синій).
Антоціани містяться майже у всіх рослинних тканинах в самих різних частинах рослин: в пелюстках, плодах, листі. Вони звичайно забарвлюють квітки і плоди в фіолетовий колір. У листі антоціани замасковані хлорофілом і виявляються лише при його руйнуванні. Цим і пояснюється червоний, жовтий і оранжевий колір осіннього листя. На колір антоціанів впливає не тільки кислотність середовища, але і її елементний склад. Наприклад, для вияву синього кольору необхідна наявність в клітках рослини комплексного з'єднання антоціанів з магнієм, алюмінієм, оловом, а також білками і цукром. Різноманітність антоціанових забарвлень рослин визначається внутрішніми біохімічними процесами і поєднанням різних антоціанів і їх похідних. Посилене утворення антоцианов в клітках рослини відбувається при зниженнях температур навколишнього середовища, при зупинках синтезу хлорофілу, при інтенсивному освітленні УХ-променями. Тому більше всього антоцианов накопичують рослини в місцевостях з суворими кліматичними умовами. Вважається, що антоциан захищає рослини від низьких температур і від шкідливого впливу сонячного кольору на цитоплазму [1].
Антоціани мають величезне біохімічне значення. Вони є могутніми антиоксидантами, які сильніше в 50 раз вітаміну С. Утворюючи комплекси з радіоактивними елементами, які згубно діють на наш організм, антоціани сприяють швидкому виведенню їх з організмів. Таким чином, антоціани є гарантами довгого і здорового життя кліток, а значить, продовжують і наше життя. Вони надають захисну дію на судини, зменшуючи їх ламкість, допомагають знизити рівень цукру в крові, поліпшують пам'ять. Поступаючи в організм людини з фруктами і овочами, антоціани виявляють дію, схожу з вітаміном Р, вони підтримують нормальний стан кров'яного тиску і судин, попереджаючи внутрішні крововиливи. Антоциани володіють унікальними властивостями - придушують зростання пухлин. Так, наприклад недавні дослідження показали, що вживання антоціанів в їжу допомагає скоротити ризик захворювання раком стравоходу і прямої кишки. Приготовані з рослин, вмісних антоціани, водні і підкислені настої протягом декількох годин знищували бактерії дизентерії і брюшного тифу. Антоціани допомагають запобігти розвитку катаракти і загалом надають сприятливий вплив на весь організм. Тому овочі і фрукти яскравих кольорів вважаються корисними для організму.
РОЗДІЛ 2
Індикатори. Загальні поняття, класифікація
2.1. Характеристика кислотно-основних індикаторів
Існує декілька визначень поняття «індикатор», але у всіх визначеннях індикатори представлені як речовини, які міняють колір в залежності від того, потрапили вони в кисле, лужне або нейтральне середовище. Так само як і визначень індикаторів, існує декілька їх класифікацій. У хімічній енциклопедії розглянуті індикатори кислотно-основні, окислювально-відбудовні, комплексонометричні, адсорбційні, ізотопні, люмінесцентні. Індикатори всіх цих шести груп інформують хіміків про те, як далеко зайшли зміни в реакційній системі. Кислотно - основні індикатори - розчинні органічні сполуки, які міняють свій колір або люмінесценцію в залежності від концентрації іонів Н+(рН середовища). Такі індикатори різко змінюють свій колір в досить вузьких межах рН. Універсальні індикатори – це суміш декількох індивідуальних індикаторів, підібраних так, що їх розчин по черзі міняє забарвлення, проходячи всі кольори райдуги при зміні кислотності розчину в широкому діапазоні pH - водневий показник. Це поняття, ввів датський хімік Серенсен для точної числової характеристики середовища розчину і запропонував математичне вираження для його визначення: рН = -lg[Н+]. Характер середовища має велике значення в хімічних і біологічних процесах, в залежності від типу середовища ці процеси можуть протікати з різними швидкостями і в різних напрямах. Тому в багатьох випадках важливо як можна більш точно визначати pH розчину. Існує нейтральна - рН = 7, рН < 7 - кислотна, при рН > 7 - лужна реакція.
2.2. Відкриття природних індикаторів
До кислотно-основних індикаторів відносяться природні індикатори. Ймовірно, самим древнім кислотно-основним індикатором є лакмус. Лакмус був відомий вже в Древньому Єгипті і Древньому Римі. Лакмус (від гол. lakmoes) - фарбувальна речовина, що добувається з деяких видів лишайників. Фактично природний лакмус являє собою складну суміш. Його основними компонентами є: азолитмин (C9H10NO5) і еритролитмин (С13H22O6) [10]. Лакмус в давнину використали як фіолетову фарба, але згодом, рецепт його приготування був загублений. У 1640 ботаніка описала геліотроп (Heliotropium Turnesole) - запашна рослина з темно-бузковими квітками, з якої було виділено фарбувальна речовина. Цей барвник, нарівні з соком фіалок, став широко застосовуватися хіміками як індикатор, який в кислому середовищі був червоним, а в лужному - синім. У 1667 році славнозвісний хімік і фізик Роберт Бойль запропонував просочувати фільтровальную папір відваром тропічного лишайника - лакмусу, а також відварами фіалок і волошок, і таким чином поклав початок застосуванню індикаторного (лакмусової) паперу. Колір рослин визначається хімічним складом клітини кожної рослини, що містить пігменти. Отже, індикатори можна знайти серед природних об'єктів. Пігменти багатьох рослин здатні міняти колір в залежності від кислотності клітинного соку. Тому, пігменти є індикаторами, які можна застосувати для дослідження кислотності розчинів. Рослинні пігменти - органічні сполуки, присутні в клітках і тканинах рослин, що забарвлюють їх. Розташовані пігменти в хлоропластах і хромопластах. У рослинному світі відомо біля 2 тисяч пігментів. Найбільш стійкими, є 150.
Клітинний сік рослини, в якому розчинений пігмент, має кислу середу, а цитоплазма - лужну. Вакуоли з клітинним соком відділені від цитоплазми мембраною, яка звичайно непроникна для антоціанів. Однак з віком в мембрані виникають дефекти, і в результаті пігмент починає проникати з вакуолей в цитоплазму. А оскільки середовище тут інакше, міняється забарвлення квіток.
В суцвіттях медунки лікарської можна одночасно знайти квітки з рожевими
віночками, ті, які розквітли – пурпурового забарвлення і ті, що вже відцвітають – синього кольору. Це зумовлене тим, що в бутонах клітинний сік має кислу реакцію, яка по мірі розпускання квіток переходить в нейтральну, а потім і в лужну. Подібні зміни забарвлення пелюсток спостерігаються у багатьох рослин, наприклад у герані. Зміна кольору пелюсток герані по мірі старіння можна пояснити індикаторними властивостями антоціанів.
РОЗДІЛ 3
Експериментально-дослідницька частина
3.1. Методика виготовлення індикаторів з природної сировини
Природні індикатори легко приготувати з рослинної сировини в домашніх умовах. Для приготування розчинів індикаторів з рослинної сировини рекомендується використовувати забарвлені рослини або їх частини. Вибір рослинного матеріалу для приготування індикаторів необмежений.
Рослинну сировину використовувала в сирому і в сушеному вигляді.
Рослинна сировина, яка була використана під час дослідження: сушені листки чаю, соковиті луски цибулі, листки капусти червонокачанної, коренеплоди буряка та моркви, бульби картоплі, ягоди вишні.
Дослід 1. Виготовлення індикатору з соку буряка, моркви, цибулі, картоплі:
1. рослинну сировину очистити від забруднення, помити;
2. натерти овочі на дрібній тертці;
3. віджати сік;
4. для отримання водного розчину додати води.
Дослід 2. Виготовлення індикатору з листя капусти червонокачанної:
1. листочки капусти дрібно нарізати, покласти в банку з водою, закрити кришкою;
2. банку поставити в кастрюлю з водою, прокип’ятити 5-7 хв;
3. забарвлений розчин охолодити, процідити.
Дослід 3. Виготовлення індикатору з ягід вишні:
1. покласти ягоди в марлю, віджати її, зібравши в вузлик;
2. для отримання водного розчину додати води.
Дослід 4. Виготовлення індикатору з листків чаю:
1. заварку чаю покласти в стакан;
2. залити заварку водою, яка щойно закипіла;
3. накрити блюдцем і почекати 15-20 хв;
4. розчин охолодити, профільтрувати.
Кожен розчин після приготування, охолодження і фільтрування злити в приготовлену заздалегідь чисту склянку з етикеткою.
Висновки за результатами дослідів:
1. В плодах, листях, коренеплодах, бульбах рослин містяться барвники (пігменти), що володіють індикаторними властивостями.
2. Рослинні індикатори можливо виготовити в домашніх і лабораторних умовах.
3. Рослинні індикатори мають яскраве забарвлення.
3.2. Дослідження властивостей природних індикаторів
3.2.1. Зміна кольору природного індикатора в різних середовищах
Щоб дізнатися, який відвар служить індикатором на те чи інше середовище і як змінюється його колір, провела випробування: піпеткою кілька крапель саморобного індикатора додавала по черзі в кислий або лужний розчин. Кислим розчином може служити 9 % розчин столовий оцету, а лужним розчином – 10 % розчин харчової соди.
Досвід 6. Дослідження чутливості розчинів рослинних індикаторів на зміну рН середовища
Мета: з'ясувати, які природні індикатори володіють високою чутливістю.
Обладнання: зразки природних індикаторі, що використовуються в попередніх дослідах, луг, кислота; пробірки.
Хід досвіду: у всі зразки додаємо кислоту і луг.
Результати всіх дослідів заносимо в таблицю.
Таблиця 3.2.1.
Зміна кольору природного індикатора в різних середовищах
|
№ п/п |
Сировина для приготування індикатора |
Природний колір індикатора |
Колір в кислому середовищі |
Колір в лужному середовищі |
|
1. |
Цибуля фіолетова |
світло-фіолетовий |
рожевий |
каламутний знебарвлений |
|
2. |
Чай чорний |
коричнево-жовтий |
світло-коричневий |
коричневий |
|
3. |
Морква |
помаранчевий |
незначне знебарвлення |
не змінився |
|
4. |
Буряк |
темно-червоний |
рожевий |
малиновий |
|
5. |
Картопля |
лимонно-жовтий |
каламутно-жовтий |
не змінився |
|
6. |
Плоди вишні |
червоний |
ясно-червоний |
не змінився |
|
7. |
Капуста червонокачанна |
червоний |
червоний |
зелений |
Висновок: внаслідок експерименту я пересвідчилася, що не всі речовини володіють яскраво вираженими індикаторними властивостями. У той же час рослинні індикатори, отримані з червонокачанної капусти, буряка можна з успіхом застосовувати для визначення кислих і лужних розчинів як універсальні.
3.2.2. Для дослідження впливу концентрації природного індикатору на інтенсивність кольору розчину використала сік буряка, отриманий в досліді 1
( Додаток 1).
Дослід 7. Виготовлення розчинів різної концентрації з соку буряка.
1. за допомогою мірного циліндра відміряти певну кількість соку буряка, додати воду.
2. розрахунки виготовлення розчинів приведено в таблиці.
Таблиця 3.2.2.
Виготовлення розчинів різної концентрації з соку буряка
|
№ п/п |
Кількість соку буряка, мл |
Кількість води, мл |
Концентрація розчину, % |
|
1. |
10 |
90 |
10 |
|
2. |
20 |
80 |
20 |
|
3. |
30 |
70 |
30 |
Досвід 8. Дослідження впливу концентрації природного індикатору на інтенсивність кольору розчину.
Мета: з'ясувати, чи впливає концентрація природного індикатора на інтен-
сивність кольору розчину.
Обладнання: зразки природниго індикатора, виготовлені з соку буряка різної концентрації, луг, кислота; пробірки.
Хід досвіду: у всі зразки додаємо кислоту і луг.
Результати всіх дослідів заносимо в таблицю.
Таблиця 3.2.3.
Вплив концентрації природного індикатору на інтенсивність кольору розчину
|
№ п/п |
Концентрація розчину індикатора |
Колір в кислому середовищі |
Колір в лужному середовищі |
|
1. |
10 |
|
|
|
2. |
20 |
|
|
|
3. |
30 |
|
|
Висновок: внаслідок експерименту я пересвідчилася, що концентрація розчину індикатора впливає на інтенсивність кольору розчину. 30 % коцентрація розчину індикатора показала найвищу інтенсивність кольору розчину.
ВИСНОВКИ
1. Найпоширеніші рослинні пігменти – антоціани.
2. Рослинна сировина, яка містить пігменти може бути використана в якості індикатора.
3. Природні індикатори можна виготовити з рослинної сировини як в сирому так і сушеному вигляді.
4. Найкраще використовувати соки та відвари з коренеплодів буряка, ягід вишні, листя червонокачанної капусти.
5. Розчини рослинних індикаторів можна використовувати як кислотно-основні індикатори для визначення рН середовища.
6. Інтенсивність забарвлення індикаторів залежить від значення рН середовища: від рожевого до червоного – у кислому, від фіолетового до жовто-зеленого і зеленого у лужному.
7. Перевагою природних індикаторів є їх екологічна безпечність, доступність, невисока вартість, швидкість та наочність аналізу.
9. Інформацію, отриману в цій роботі можна використовувати як на уроках хімії, так і на уроках біології ( Додаток 2).
СПИСОК ВИКОРИСТАНИХ ДЖЕРЕЛ
1. Артамонов В. И. Занимательная физиология растений.- М.: Агропромиздат,
1991. - 337с.
2. Байкова В. М. Химия после уроков. Петрозаводск «Карелия», 1976. - 175 с.
3. Велика Радянська Енциклопедія: в 30 т.: т. 2/Гл. ред.: Прохоров А. М. - М.: Сов. Енцикл., 1970. - 97 с.
4. Меженский В. Н. Рослини-індикатори. М.: ТОВ «Видавництво ACT»; Донецьк: «Сталкер», 2004 - 76 с.
5. Оганесян Е. Т. Руководство по химии для поступающих в вузы. - М.: Висш. школа, 1991. - 464с.
6. Семенов П. П. «Індикатори з місцевого рослинного матеріалу», // журнал Хімія в школі. №1, 1984 - 73 с.
7. Хімічна енциклопедія: в 5 т.: т. 2 / Гл. ред.: Кнунянц И. Л. - М.: Сов. Енцикл., 1990 - 671 с.
8. Енциклопедія для дітей. Том 17. Хімія / Гл. ред.: Володин В. А. - М.: Аванта+, 2002 - 640 с.
9. http://www.edudic.ru/. Біофлавоноїди. Хімічна енциклопедія
10. http://ru.wikipedia.org/wiki/. Лакмус. Вікипедія. Вільна енциклопедія.
11. http://www. moizveti.ucoz.ru/. Мій квітковий світ.
12. http://travi.uvaga.biz/. Антоциани. Лікувальні трави.
13. http://www.valleyflora.ru/. Дивний мир ростений.
ДОДАТОК 1
Виготовлення природного індикатору з буряка

ДОДАТОК 2
Застосування природних індикаторів на уроках біології та хімії
1


про публікацію авторської розробки
Додати розробку
