Презентація на тему: "Фізичні та хімічні властивості основних оксидів".
Про матеріал
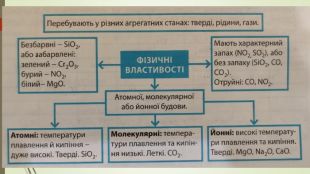
Презентація уроку на тему: "Фізичні та хімічні властивості основних оксидів".
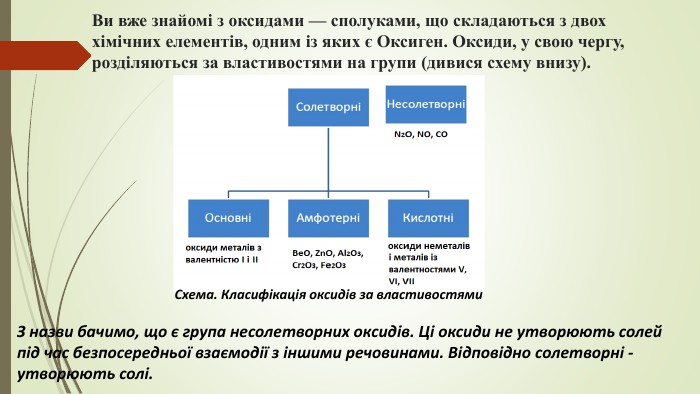
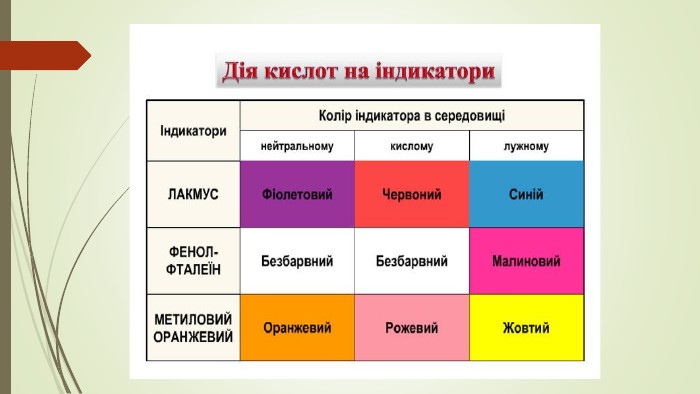
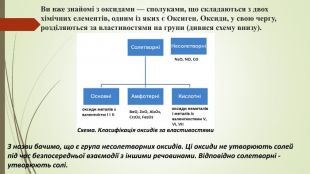
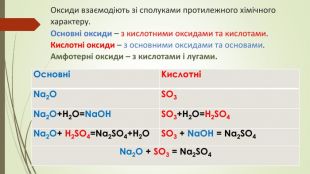
Матеріал допоможе зрозуміти, за якими ознаками поділяють оксиди, і які властивості вони проявляють в залежності від того чи вони основні чи кислотні.
Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки
-
Презентація допомагає легкому засвоєнню матеріалу.


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку