Презентація на тему: "Властивості амфотерних оксидів".
Про матеріал
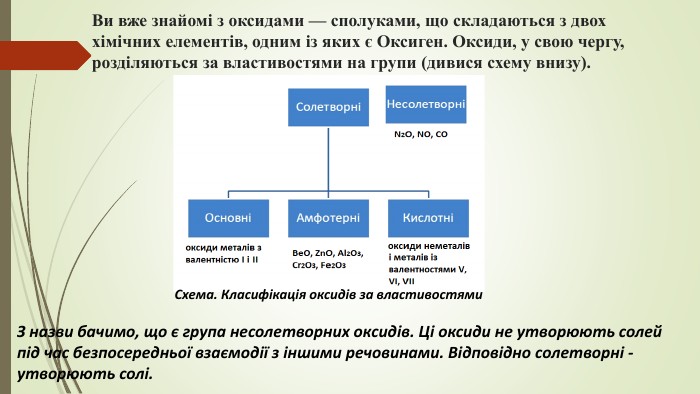
Презентація уроку на тему: "Амфотерні властивості оксидів"
Презентація допоможе учням з'ясувати, які сполуки називають амфотерними;
зрозуміти хімічний характер амфотерних оксидів;
складати формули продуктів реакцій амфотерних сполук з кислотами, основами, оксидами.
Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки
-
-
Дякую


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку










![Закінчіть рівняння можливих хімічних реакцій. Zn. O + H2 O → не реагують. Al2 O3 + Na2 O → Na3 Al. O3 Zn. O + 2 Li. OH → Li2 Zn. O2 + H2 O під час сплавляння або. Zn. O + 2 Li. OH+ H2 O → Li2[Zn(OH)4] під час реакції в розчині Закінчіть рівняння можливих хімічних реакцій. Zn. O + H2 O → не реагують. Al2 O3 + Na2 O → Na3 Al. O3 Zn. O + 2 Li. OH → Li2 Zn. O2 + H2 O під час сплавляння або. Zn. O + 2 Li. OH+ H2 O → Li2[Zn(OH)4] під час реакції в розчині](/uploads/files/1923723/279709/304006_images/12.jpg)
![Zn. O + SO2 → Zn. SO3 Al2 O3+ К2 O → 2 KAl. O2 Al2 O3+ 2 Li. OН → 2 Li. Al. O2 + H2 O під час сплавляння або. Al2 O3 + 6 Li. OН + 3 H2 O → 2 Li3[Al(OH)6] у розчиніAl2 O3+ Н2 O → не реагують. Al2 O3+ 3 SО3 → Al2(SО4)3 Zn. O + SO2 → Zn. SO3 Al2 O3+ К2 O → 2 KAl. O2 Al2 O3+ 2 Li. OН → 2 Li. Al. O2 + H2 O під час сплавляння або. Al2 O3 + 6 Li. OН + 3 H2 O → 2 Li3[Al(OH)6] у розчиніAl2 O3+ Н2 O → не реагують. Al2 O3+ 3 SО3 → Al2(SО4)3](/uploads/files/1923723/279709/304006_images/13.jpg)






















