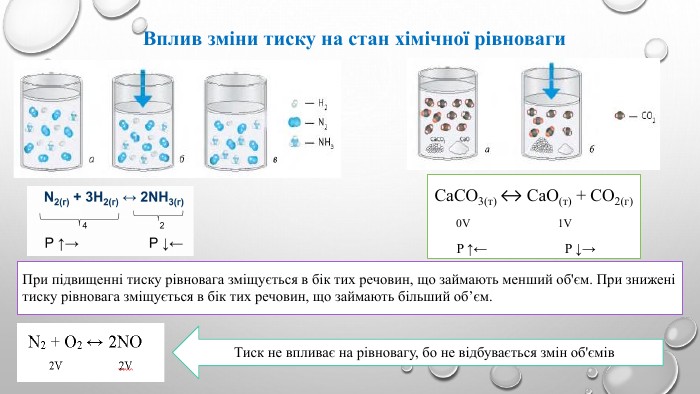
Хімічна рівновага. Принцип Ле Шательє
Про матеріал
Презентація до уроку хімії в 11 класі з теми "Хімічна рівновага. Принцип Ле Шательє". Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку