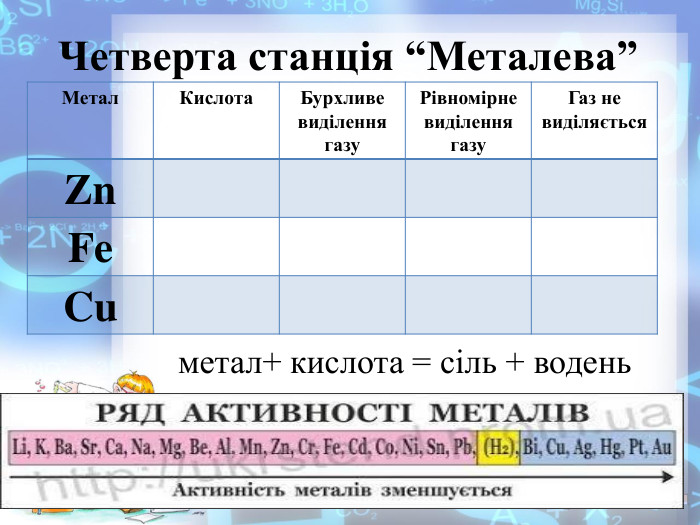
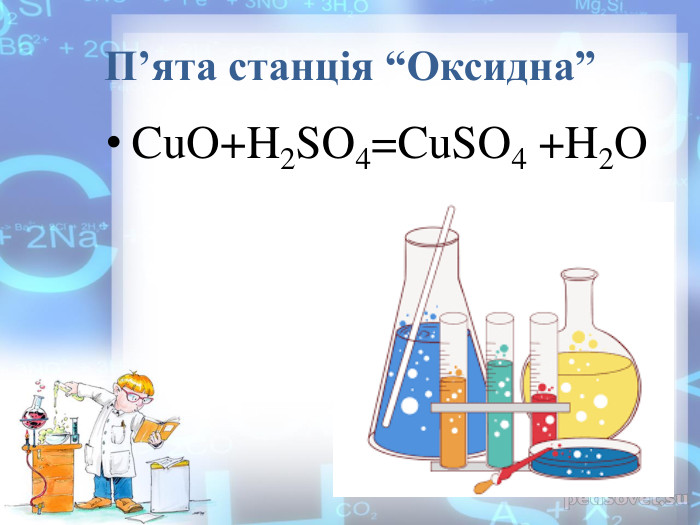
Хімічні властивості кислот
Про матеріал
Цікава презентація про хімічні властивості кислот та вправи на перевіку набутих знань про кислоти та їх властивості. Перегляд файлу
Зміст слайдів


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку