Узагальнення знань з теми «Хімічний зв'язок і будова речовин»
Тема уроку: Узагальнення та систематизація знань з теми: «Хімічний зв'язок і будова речовин»
Мета: узагальнити та систематизувати знання учнів про типи хімічного зв’язку та типи кристалічних ґраток; вміти наводити приклади сполук із ковалентним (полярним і неполярним) та йонним хімічними зв’язками, атомними, молекулярними та йонними кристалічними ґратками; пояснювати і складати утворення йонного, ковалентного (полярного і неполярного) зв'язків; давати характеристики цим речовинам.
Обладнання: періодична система хімічних елементів Д. І. Менделєєва, ряд електронегативності, онлайн-дошка Jamboard
Базові поняття і терміни: хімічний зв’язок, електронегативність, ковалентний зв’язок, йонний зв’язок, кристалічні ґратки, атомна, молекулярна, йонна, металічна кристалічні ґратки
Тип уроку: узагальнення й систематизація знань, умінь і навичок.
Хід уроку
І. Організаційний момент.
Сьогодні узагальнимо ваші знання з теми "Хімічний зв'язок і будова речовини". Перевірка домашнього завдання
ІІ. Узагальнення і систематизація знань.
1. Бліц – опитування
- Скільки спільних електронних пар виникає у молекулі хлору Cl2?
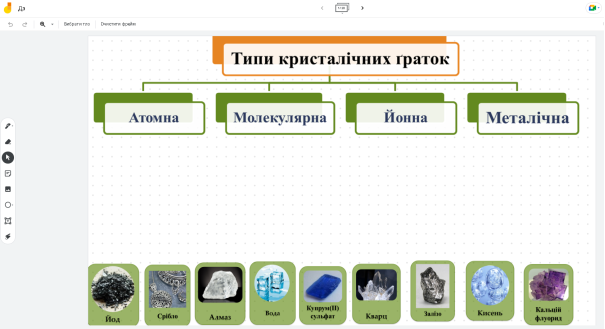
- Укажіть тип кристалічних граток в алмаза?
- Тип хімічного зв'язку між позитивно та негативно зарядженими іонами називають?
- Який тип хімічного зв’язку в сполуці Гідрогену з Сульфуром?
- Вкажіть тип хімічного зв'язку в речовині, формула якої SO2?
- Скільки спільних електронних пар у молекулі речовини, хімічна формула якої HCl?
- Укажіть кількість електронів, що взяли участь в утворенні зв’язків у молекулі водню H2?
- Укажіть тип зв’язку у сполуці, утвореній хімічними елементами з протонними числами 11 і 53?
2. Задача

Відносна густина двоатомного газу Х за воднем становить 15. Обчислити молярну масу газу Х. Що це за газ, якщо він містить один атом Оксигену і ще один невідомий атом?
Установіть тип хімічного зв'язку в молекулі газу.
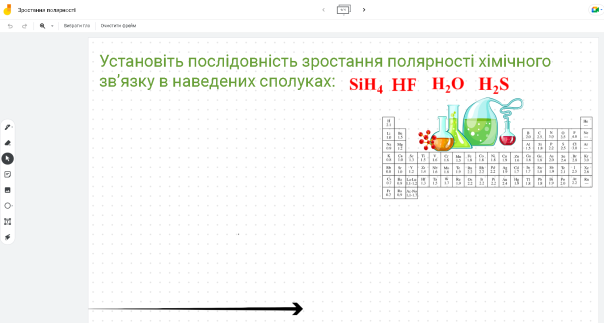
3. Установіть послідовність зростання полярності хімічного зв’язку в наведених сполуках: , H2O, HF, H2S, SiH4
˄EH(H-O) = 3,5-2,1=1,4
˄EH(H-F) =4-2,1=1,9
˄EH(H-S) =2,5-2,1=0,4
˄EH(Si-H) =2,1-1,8=0,3
SiH4 H2S H2O HF
![]()
ІІІ. Підведення підсумків уроку.
ІV. Підбиваємо підсумки уроку, оцінюємо роботу .
V. Рефлексія:
- Поділіться своїми враженнями…
- Сьогодні я дізнався/ дізналася….
- Мені сподобалося…/ не сподобалося…..


про публікацію авторської розробки
Додати розробку
