Інструкція для практичної роботи "Виявлення органічних речовин"
Практична робота - дидактичний інструмент для досягнення цілей навчання хімії. Тільки в тісній взаємодії експерименту і теорії можна досягти високої якості знань учнів з хімії. Провівши дані якісні реації на органічні речовини, учні закріплюють знання про органічні сполуки, підтверджують їх наявність. Ці реакції широко використовуються при проведенні якісного аналізу, метою якого є визначення наявності речовин в розчинах або сумішах.
![]()
«Виявлення органічних речовин»
Видані вам органічні речовини. Проводячи якісні реакції, знаючи хімічні властивості певних речовин – необхідно визначити в якій пробірці знаходяться речовини:
- Цукор,
- Гліцерин,
- Білок,
- Глюкоза,
- Крохмаль
- Мило.
МЕТАвиявити речовини, описати процес, скласти хімічні рівняння де можливо (гліцерин, глюкоза, мило)
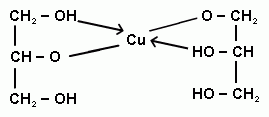
1,2 - якісною реакцією на багатоатомні спирти, є їх взаємодія зі свежеприготовленим Купрум (ІІ) гідроксидом. Яскраво-синє забарвлення свідчить про вміст у розчині багатоатомного спирту (гліцерин чи сахароза).
До розчину мідного купоросу (CuSO4) додати Натрію гідроксид (NaOH - луг), колір осаду - синій. Додаємо гліцерин чи сахарозу - осад розчиняється, колір стає більш яскравим і більш насиченим. Скласти рівняння
3. а) Біуретова реакція для виявлення пептидного зв'язку (CO-NH):
Білок + CuSO4 + NaOH -> червоно-фіолетове забарвлення
б) ксантопротеїнова Білок + HNO3 ---- осад жовтого кольору
4. Глюкоза містить у своєму складі п'ять гідроксильних груп і одну альдегідну групу. Тому вона відноситься до Альдегідоспиртів . Її хімічні властивості схожі на властивості багатоатомних спиртів і альдегідів . Реакція з Cu(OH)2 демонструє відновні властивості глюкози. До осаду, приготовленного при взаємодії кілька крапель розчину Купрум (II )сульфату і розчин лугу, доливаємо розчин глюкози. Розчин забарвлюється в яскраво -синій колір. У даному випадку глюкоза розчиняє осад і веде себе як багатоатомний спирт. Нагріємо розчин. Колір розчину починає змінюватися. Спочатку утворюється жовтий осад Cu2O. Глюкоза при цьому окислюється до глюконової кислоти.
5. При взаємодії крохмалю з йдом утворюється синій колір, якій при нагріванні зникає. Скористайтесь Піпеткою.
6.Мила - це натрієві (рідше калієві) солі жирних кислот складу СН3(СН2)16 COONa. Якщо в розчин мила додати CaCl2, випаде осад кальціевой солі у вигляді пластівців.
Утворюється Кальцій пальмі ат – нерозчинна сполука.


про публікацію авторської розробки
Додати розробку
