Кейс урок по темі: Жири як представники естерів. Класифікація жирів, їхні хімічні властивості
Мета уроку: формувати знання учнів про жири, їх склад, утворення; вивчити будову жирів і властивості їх як естерів гліцерину й вищих карбонових кислот; ознайомити учнів з хімічними властивостями жирів на прикладі гідролізу й гідрування; визначити сфери застосування жирів, способи їх одержання; розвивати вміння й навички складання рівнянь хімічних реакцій на прикладі реакцій синтезу й гідролізу жирів, гідрування жирів різного складу; показати практичне значення цих реакцій; ознайомити учнів з поширенням жирів у природі, їх біологічною роллю, застосуванням.
Навчальна мета: сформувати поняття про жири як естери; ознайомити учнів із поширенням, складом і фізичними і хімічнимивластивостями жирів на прикладі гідролізу й гідрування; сформувати вміння записувати формули жирів. показати поширення жирів у природі, їх біологічну роль, застосування.
Розвивальна мета: розвивати вміння висловлювати власну думку, узагальнювати факти, використовуючи набуті знання про будову, склад, властивості та способи одержання жирів; розвивати творчі здібності учнів, пам'ять;вибирати головне з тексту підручника.
Виховнамета: виховувати культуру спілкування, комунікативність, вміння співпрацювати.
Базові поняття й терміни: оксигеновмісніорганічні речовини, спирти, вищі карбонові кислоти, насичені, ненасичені карбонові кислоти, складні естери, реакція етерифікації, гідролізу.
Тип уроку: кейс-урок, комбінований урок засвоєння знань, умінь і навичок і творчого застосування їх на практиці.
Тип кейса: навчальний
Форми роботи: навчальна лекція, лабораторний експеримент, робота з кейсом.
Демонстрації
8. Відношення жирів до води та органічних розчинників.
9.Доведення ненасиченого характеру рідких жирів (віртуально).
Обладнання: зразки жирів рослинного і тваринного походження, кейс.
Кейс урок по темі: Жири як представники естерів. Класифікація жирів, їхні хімічні властивості. Застосування жирів
10 клас (нова програма)
Мета уроку: формувати знання учнів про жири, їх склад, утворення; вивчити будову жирів і властивості їх як естерів гліцерину й вищих карбонових кислот; ознайомити учнів з хімічними властивостями жирів на прикладі гідролізу й гідрування; визначити сфери застосування жирів, способи їх одержання; розвивати вміння й навички складання рівнянь хімічних реакцій на прикладі реакцій синтезу й гідролізу жирів, гідрування жирів різного складу; показати практичне значення цих реакцій; ознайомити учнів з поширенням жирів у природі, їх біологічною роллю, застосуванням.
Навчальна мета: сформувати поняття про жири як естери; ознайомити учнів із поширенням, складом і фізичними і хімічними властивостями жирів на прикладі гідролізу й гідрування; сформувати вміння записувати формули жирів. показати поширення жирів у природі, їх біологічну роль, застосування.
Розвивальна мета: розвивати вміння висловлювати власну думку, узагальнювати факти, використовуючи набуті знання про будову, склад, властивості та способи одержання жирів; розвивати творчі здібності учнів, пам'ять; вибирати головне з тексту підручника.
Виховна мета: виховувати культуру спілкування, комунікативність, вміння співпрацювати.
Базові поняття й терміни: оксигеновмісні органічні речовини, спирти, вищі карбонові кислоти, насичені, ненасичені карбонові кислоти, складні естери, реакція етерифікації, гідролізу.
Тип уроку: кейс-урок, комбінований урок засвоєння знань, умінь і навичок і творчого застосування їх на практиці.
Тип кейса: навчальний
Форми роботи: навчальна лекція, лабораторний експеримент, робота з кейсом.
Демонстрації
8. Відношення жирів до води та органічних розчинників.
9.Доведення ненасиченого характеру рідких жирів (віртуально).
Обладнання: зразки жирів рослинного і тваринного походження, кейс.
Структура уроку.
І. Організаційний.
ІІ. Мотивація навчальної діяльності.
ІІІ. Актуалізація опорних знань.
ІV. Вивчення нового матеріалу.
а) Біологічна роль жирів.
б) Класифікація жирів.
в) Склад і утворення жирів.
г) Фізичні властивості жирів.
д) Хімічні властивості жирів.
є) Добування жирів.
ж) Застосування.
V. Узагальнення знань. «Що означають твердження?»
За дошкою записані твердження:
- тваринного, рослинного походження;
- тверді жири утворені……., олії утворені……;
- жири належать до класу…;
- для жирів характерні реакції;
- у повсякденному житті протікають реакції.
VІ. Домашнє завдання.
VІІ. Підбиття підсумків уроку.
Хід уроку.
І. Організаційний етап.
ІІ. Мотивація навчальної діяльності.
Учитель. Ми з вами уже кілька уроків вивчаємо оксигеновмісні органічні речовини. Продовжимо вивчення окремих представників . Сьогодні на уроці ми поведемо мову про речовину, яка становить одну з основних частин нашої їжі.
ІІІ. Актуалізація опорних знань. Ви знаєте, що є таке важке дитяче захворювання - рахіт. Виявляється і його профілактика й лікування не обходяться без жиру, а саме, добре знайомого вам риб'ячого жиру. Що ж це за речовини - жири, які відіграють у нашому житті таку велику роль? Про них і піде мова на сьогоднішньому уроці.
Інтерактивна гра – «Уявний мікрофон»
- Які сполуки називаються оксигеновмісними?
- Які класи оксигеновмісних органічних речовин вам відомі?
- Які сполуки називаються спиртами?
- Які сполуки називаються карбоновими кислотами?
- Як класифікують карбонові кислоти?
- Формула гліцерину
- Яка загальна формула карбонових кислот?
- Яка реакція називається реакцією гідролізу?
ІV. Вивчення нового матеріалу.
Жири поряд з вуглеводами й білками є коштовним харчовим продуктом. Для здорового організму людини добова потреба жиру становить 70-100 г. Зі збільшенням віку й зменшенням фізичного навантаження споживання жирів повинне бути знижене, тому що надлишок жирів в організмі людини є однією з основних причин багатьох захворювань, зокрема, особливо серцево-судинних. В організмі людини основна функція жиру – бути джерелом енергії. Окиснення 1г жиру спричиняє виділенню 39 кДж енергії. Однак буде нерозумним прагнути забезпечити свій організм виключно жирами, оскільки, незважаючи на те, що вони багаті на енергію, жири важко засвоюються. Але не можна забувати, що надлишкова кількість жиру, навіть у раціоні здорової людини, дуже шкідлива. Жири не розчиняються ані водою, ані травними соками. В організмі вони розщеплюються й емульгуються за сприяння жовчі. Зайва кількість жиру не встигає проемульгуватися, порушує травні процеси та спричиняє неприємне відчуття печії.
Жири є не тільки джерелом енергії в організмі, а й джерелом води. Завдяки цій воді живуть верблюди тривалий час без свіжої води. Для розвитку зародка курчати в інкубаційний період потрібна вода, а надходження її ззовні відсутнє. Зародок забезпечується водою окисленого жиру. Жири необхідні й мешканцям холодного клімату: тюленям, моржам. Підшкірний жир допомагає зберегти внутрішнє тепло. Будь – якій тварині жирові відкладення пом’якшують силу різних поштовхів і ударів. Крім того, жири для тварин – мастильний матеріал. Відомо, водоплавні птахи самі проводять змащення під час чищення пір’я. Висока харчова цінність жирів зумовлена також розчинністю в них деяких вітамінів А, Д, Е.
Давайте ми з вами разом пригадаємо відоме про жири, дамо відповідь на питання:Як класифікують жири за походженням?»
б) Класифікація жирів.
Обговорення. Як класифікують жири за походженням?
Жири
![]()
![]()
тваринні жири рослинні жири, олії
( яловичий жир,свиняче сало, вершкове масло)
Учні наводять приклади тваринних і рослинних жирів.
в)Розглянемо питання про склад і утворення жирів.
Історичні факти:
К.Шеелє (шведський учений): “масляний цукор” в 1779р. уперше виявив жири.
М.Шеврель (французький учений): в 1811р. установив сполуку жирів.
У 1854 році М. Бертло уперше синтезував жир. Він нагрівав гліцерин з вищою карбоновою кислотою у запаяній посудині. Записуємо хімічне рівняння.
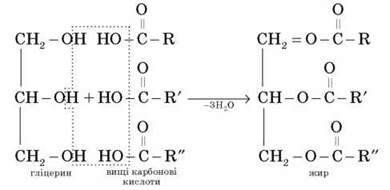
Перед вами формула жиру у загальному вигляді. R1, R2, R3 – вуглеводневі залишки (як правило різні, але можуть бути однаковими). Жири утворюють такі насичені кислоти як пальмітинова С15H31COOH, стеаринова C17H35COOH, ненасичена олеїнова C17H33COOН.
Чи можна довести, що жири містять насичені або ненасичені жирні кислоти?
Демонстрація.
Твердий жир + KMnO4 + Na2CO3; олія + KMnO4 + Na2CO3
без змін знебарвлення зміна фіолетового забарвлення
відбулася тому, що олія містить ненасичені кислоти
Робота в групах. З’ясуємо відношення до розчинників.
І ряд H2O + жир
ІІ ряд етанол + жир
ІІІ ряд гас + жир
Висновок: жири не розчинні у воді, розчинні у спирті, гасі.
Чи мають жири смак, запах, колір? Смак, запах, колір зумовлені різними домішками. При струшуванні рідких жирів з водою утворюється емульсія. Температури різні, жири утворені гліцерином і насиченими кислотами мають вищі температури плавлення
Опрацювання теоритичних відомостей кейсу у підручнику, або інтернет мережі та доповнення твердженнь. (На столі учнів видані аркуші з завданнями)
- Гідролізом називають реакцію жиру з……..(водою), внаслідок якої утворюються………(гліцерин) і ………(відповідні) кислоти.
- Гідроліз відбувається при температурі …….(200 – 2500С) .
- Якщо гідроліз здійснювати за наявності лугу, то крім гліцерину утворюються ..….(мила).
- Якщо рідкі жири приєднують……..(водень), то вони перетворюються на …….(тверді жири). Цей процес називається…………(гідруванням).
- Маргарин – це………..Його виробляють із…….
- Термічний розклад – це……..
- Внаслідок окиснення жирів на повітрі утворюються…..
- Калій перманганат окислює …….
- Повне окиснення жирів – це…….
Застосування жирів.
- харчова промисловість;
- маргарин;
- у домашніх умовах;
- мило;
- гліцерин;
- медицина;
- оліфа;
- косметичні засоби.
V Узагальнення знань.
Зміст кейсу
Жири–суміш складних естірів, утворених гліцерином і жирними кислотами. М.Э Шеврель присвятив вивченню жирів 14 років. В 1808 році до нього звернувся власник текстильної фабрики із проханням вивчити сполука м'якого мила, одержуваного на фабриці. Шеврель установив, що мило – натрієва сіль вищої жирної кислоти. Шеврель виготовляв мила з жирів різних тварин, виділяв з них жирні кислоти. Так були вперше отримані стеаринова, олеиновая, капронова кислоти. Шеврель показав, що жири складаються із гліцерину й жирних кислот, причому це не тільки їх суміш, а сполука, яка, приєднуючи воду, розпадається на гліцерин і жирні кислоти.
Завдання:
- Які формули жиру й мила?
- Запропонуєте спосіб одержання мила з жиру в домашніх умовах.
- Знайдіть із інших джерел додаткову інформацію про жири, мила, СМС.
- У сучасному світі пропонується багато косметичної, гігієнічної продукції. А як правильно вибрати мило, на що треба звернути увагу?
Виробництво мила складається із двох стадій: хімічної й механічної. На першій стадії (варіння мила) одержують водяний розчин натрієвих (рідше калієвих) солей, жирних кислот або їх замінників.
В Київській Русі варили мило з давніх часів. Варили й у майстернях, і в домашніх умовах. Для виготовлення мила використовували яловиче, бараняче, свиняче сало. До наших днів дійшла стара приказка: «Сало було, стало мило». Для м'якості додавали рослинні олії, наприклад лляне. Займалися «поташним промислом» цілими селами, саме так у ті часи називали миловарне виробництво.
Представляємо кілька способів миловаріння:
- Гарячий міцний розчин пральної соди налити в склянку й додавати по краплях рослинну олію, поки вона не перестане розчинятися. В отриманий розчин додати небагато повареної солі (процес так і називається - висалювання. Тверде мило спливе на поверхню, його легко зібрати.
- Виготовлення високоякісного ядрового мила. Нагріваючи на водяній лазні, розтопити 70 г. яловичого жиру й 30 г. свинячого сала. Потім, енергійно заважаючи, додати нагрітий розчин натрій гідроксиду (25 г сухого гідроксиду на 30г води). Обережно! Луг може розприскуватися!
Отриману суміш, помішуючи, нагрівати на водяній лазні 30 хв. У міру википан, додавати гарячу воду. Потім додати 100 мол. 20%-ного розчину повареної солі й знову нагріти до повного відділення мила. Зібране мило при необхідності загорнути в ганчірку й віджати (краще робити це в рукавичках, щоб не обпектися міцним розчином лугу).
Потім промити мило в невеликій кількості холодної води й додати небагато розчиненого в спирті запашної речовини ( це може бути кминне, ганусове, фенхельне масло або будь-яке інше). Його треба трохи, запах дуже сильний. Після цього загорнути мило в міцну ганчірку й ретельно розім'яти. І, нарешті, злегка підігріти отриману масу й пресуванням надати їй вид звичайного шматка мила.
Як правильно вибирати мило й на що звертати увагу?
Насамперед, потрібно ретельно прочитати сполука мила на впакуванні. Якщо Ви знайдете там речовини, список яких наведений нижче, те це, швидше за все, мило масового промислового виробництва.
|
Поліпропіленгліколь |
Продукт, який одержують із нафти, використовується в косметичній продукції, а також для готування антифризу й гальмової рідини. Він більш дешевий, чому гліцерин, але викликає більше алергійних реакцій і запалення шкіри. |
|
Лаурил-сульфат натрію (Sodiumlaurethsulfate) |
Дешевий мийний засіб, утворює багато піни, при цьому виникає ілюзія, що він має дуже сильні миючі властивості. Є припущення, що це канцероген. |
|
ПАР |
Усі вони є нафтопродуктами - DEA (Dieth-nolamine) MEA (Monoethanolamine) TEA (Trieth-anolamine), Cacamide DEA, Dea-cetylphosphate, DEA Oleth-3 phosphate, Myristamide DEA, Stearamide MEA, Cocamide MEA, Lauramide DEA, Linoleamide MEA, Oleamide DEA, TEA Laurylsulfate – усі ці компоненти використовуються як эмульгаторы й пінно-утворюючі речовини, дратують шкіру й очі, існує припущення, що це канцерогени. |
|
Формалін |
Використовується як консервант, але виробники розуміють, що наявність такого складового не робить продукт привабливим для покупця й уводять не вільний формалін, а речовини, які його виділяють. (5-bromo-5-nitro-1,3-dioxane ; 2-bromo-2-nitropropane-1,3-diol; imdazolidinylurea; Quaternium-15, DMDM hydantion ...) |
|
Бензол і толуол |
Дуже токсичні субстанції, звичайно використовуються у вигляді бензоатов. |
|
Діоксид титану |
Використовується як барвник (мило білого кольору завжди має в складі діоксид титану), є припущення, що це канцероген. |
|
Барвники |
FD&C і D&C – вугільна смола, є припущення, що це канцероген |
|
Содіумлаурил сульфат (Sodiumlaurylsulfate) |
Дешевий мийний засіб, який уважають найбільш небезпечним у препаратах для догляду за шкірою й волоссям. У промисловості використовують для миття підлоги, машин і двигунів. Залишає на шкірі плівку, яка викликає алергійні реакції й роздратування. |
|
Парабени (Methylparaben, Propylparabenидр.) |
Аналоги сульфаніламідних препаратів, які мають протимікробні властивості й використовуються в якості консервантів. Завдяки найширшому поширенню в косметичних засобах парабени сприяють утвору нових штамів нечутливих до ліків мікроорганізмів, порушують природний імунітет, є найбільш частою причиною алергійних реакцій на косметичні засоби. При усмоктуванні проявляють токсичну дію на печінку. |
Якщо в анотації зазначено, що в милі присутні тільки солі жирних кислот, вода й натуральні добавки, таке мило заслуговує Вашої уваги. Мило ручної роботи відрізняється й по зовнішньому вигляду. Як правило, воно простіше за формою, має включення й сліди від ручної нарізки. Натуральне мило ручної роботи не може мати сильний захід (такий захід мають тільки синтетичні віддушки) і яскравий неприродний колір. У натуральному милі ручної роботи не може бути ніяких хімічних і синтетичних добавок.
Сучасні CMC являють собою багатокомпонентні суміші, головний компонент яких — синтетичні миючі речовини - у вигляді водяних розчинів знімають із поверхні твердих тіл (тканин,виробів) забруднення різної природи.
Джерела інформації:
https://www.epochtimes.com.ua/krasa-ta-zdorovya/vybraty-bezpechne-mylo-115522
https://tsn.ua/video/video-novini/oleksiy-dushka-rozpoviv-yak-obrati-bezpechne-milo.html
http://doityourself.in.ua/2015/02/23/244/
VІ Домашнє завдання
Опрацювати §
Творча майстерня: Виготовити мило власними руками або користуючись додатками 2-4 підручника підготуйте для молодших школярів поради з раціонального харчування.
VІІ Підведення підсумків уроку.
Оцінювання роботи учнів.


про публікацію авторської розробки
Додати розробку
