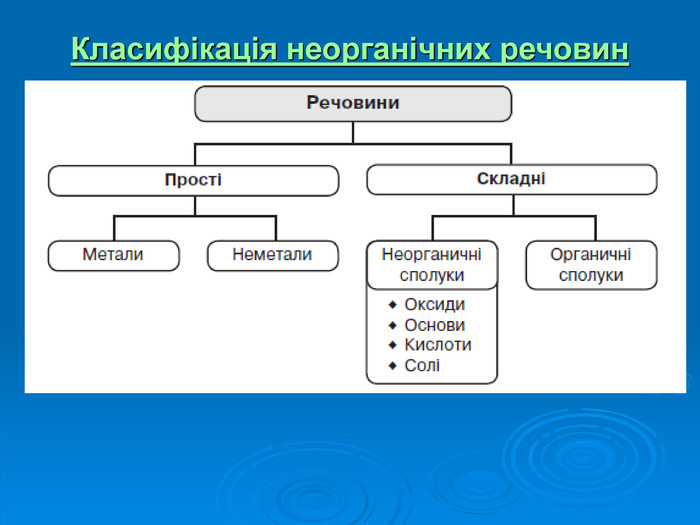
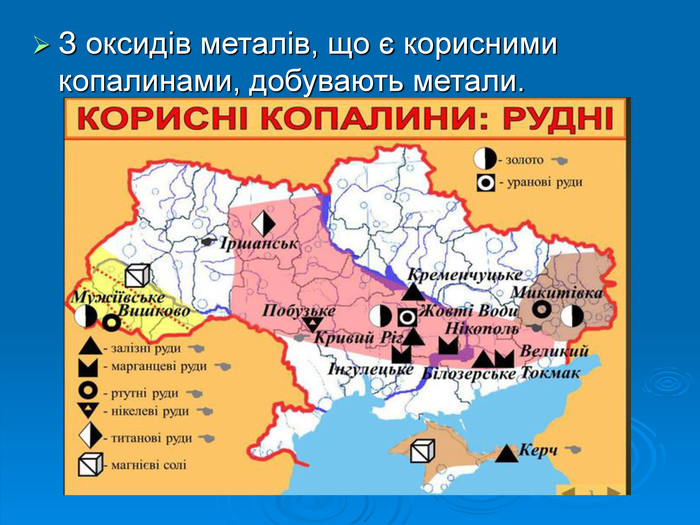
Класифікація неорганічних речовин. Оксиди: поняття, назви, поширеність
Про матеріал
Презентація до уроку хімії у 8-х класах з теми: "Класифікація неорганічних речовин. Оксиди: поняття, назви, поширеність" Перегляд файлу
Зміст слайдів


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку