Конспект уроку Microsoft Word. Тема уроку. Атомне ядро. Ядерні сили. Енергія зв'язку атомних ядер
Тема. Атомне ядро. Ядерні сили. Енергія зв'язку атомних ядер
Мета:
- провести аналіз контрольної роботи «Світлові кванти. Фотоефект»;
- формувати в учнів уявлення про будову атома та атомного ядра,
дати визначення ізотопам, ознайомити учнів з новим видом сил – ядерними силами, з’ясувати, що таке енергія зв’язку атомного ядра, та питома енергія зв’язку;
- розвивати логічне мислення, науковий світогляд, навички творчо-дослідницької роботи.
Епіграф.
- Фізика – найдивовижніша річ: вона цікава, навіть якщо в ній нічого не розумієш.
- Фізика - одна з найпрекрасніших наук. Вона показує нам, який великий і водночас близький до людини світ, в якому ми живемо. Фізика дає змогу людині відчути свою велич, надзвичайну силу свого розуму, робить її наймогутнішою істотою у світі.
- Зрозуміти і описати поведінку атомів легше, ніж зрозуміти і описати дії суверенних держав на міжнародній арені.
Джеймс Розенау
Тип уроку: засвоєння нових знань.
Обладнання: ноутбук, мультимедійний проектор, таблиці Менделєєва, портрети Е. Резефорда, Чедвіка, Іваненка, Гейзенберга.
«Дивно не те, що світ нескінченний, а те, що людина може пізнати його таємниці».
Б. Паскаль
Хід уроку
І. Організація групи.
ІІ.Аналіз контрольної роботи.
ІІІ. Актуалізація опорних знань.
Для ефективного засвоєння нового матеріалу ви мали повторити дома деякі теми.
- Будова речовини (молекули)
- З чого складаються молекули? (атоми)
- Будова атома. (ядро і електрони, які рухаються навколо ядра)
- Яка будова ядра? (протони і нейтрони)
- Чи мають заряд протони і нейтрони, якщо так, то які? (протони-позитивний, нейтрони-нейтральний)
- Який заряд ядра? (нейтральний)
- Чому ядро не має заряду? (кількість негативних зарядів (електронів) дорівнює кількості позитивних зарядів (протонів))
ІV. Мотивація навчальної діяльності.
Атом. Щоб уявити його розміри ми порівнюємо його з формою яблука. І ще один приклад. Щоб поставити 100 мільйонів атомів в рядок, то цей рядок буде довжиною 3 см. На сьогодні ми вже знаємо будову атома. Атом складається з ядра, в якому зосереджена вся масса і весь позитивний заряд, навколо якого обертаються електрони.
V. Вивчення нового матеріалу.
План
- Склад ядра атома.
- Ізотопи.
- Ядерні сили.
- Енергія зв᾽язку. Дефект мас.
- Після того як, Резерфорд довів будову атома, він висунув гіпотезу, що до складу ядра атома входить ядро Гідрогену.
У 1919 р. йому це вдалося на досліді перевірити. Перше ядро яке йому вдалось розщепити, було ядро Нітрогену.


Пізніше його учні розщепили ще кілька ядер і завжди вилітали ядра Гідрогену.
Ці ядра Резерфорд назвав протонами (походить від грецького – перший, первинний).
Дуже швидко стало ясно, що ядра атомів не можуть складатись тільки з протонів.
У 1932 р учень Резерфорда – Чедвік – відкрив нейтрон. Це електрично нейтральна частинка (з латинського – нейтрон)
Практично в тому ж таки році українці за походженням Іваненко і нім. Фізик Гейзенбер незалежно один від одного запропонували протонно-нейтронну модель ядра атома.
За цією моделлю ядро атома складається з протонів і нейтронів.
Протони і нейтрони вони назвали нуклонами. (лат. походження – ядро).
Для характеристики ядра того чи іншого атома, вводяться такі величини: як масове число (А)(кількість протонів і нейтронів) і зарядове число Z (число протонів у ядрі) 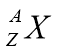
На прикладі ядра атома N Натрію ми дізнаємось як це зробити.
У вас є алгоритм. Читаємо.
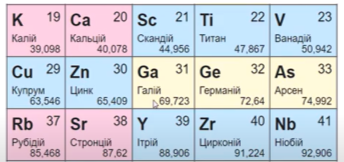
- Подивись в таблиці Менделєєва пошуковий номер елементу – це зарядове число (Z);
- Подивись в таблиці масу елементу і заокруглити до цілих – це масове число.
- Знайти різницю: N = A – Z
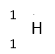 ІІ. Чим відрізняються ядра Гідрогену
ІІ. Чим відрізняються ядра Гідрогену
![]()
![]()
(масовим числом ) – N
Такі елементи, ядра яких мають однакову кількість протонів, але різне масове число (кількість нейтронів) називають – ізотопами.
У нашому випадку Гідроген має 3 ізотопи.
ІІІ. Виходячи з того, що однойменно заряджені частинки відштовхуються, вони мали б розлетілись в різні сторони. Тим не менше цього не відбувається. Чому? Тому, що протони і нейтрони в ядрі зв’язані ядерними силами. Що ж це за сили? Ці сили є найбільш потужними силами в природі.
Інша важлива особливість ядерних сил - це їх короткодіючий характер.
Електромагнітні сили порівняно повільно зменшуються з відстанню.
ІV. Ядерні сили набагато сильніші за кулонівські, тому, щоб “розділити” ядро на окремі нуклони, необхідно виконати роботу, тобто витратити певну енергію.
- Енергію, необхідно для повного розщеплення ядра на окремі нуклони, називають енергією зв‘язку атомного ядра ( Eзв )
Маси ядер можна виміряти з високою точністю за допомогою мас-спектрометра.
Маса атомного ядра завжди виявляється менше суми мас нуклонів.
Це явище називають дефектом мас.
Дефект маси – це різниця між сумою мас нуклонів, що містяться в ядрі і масою ядра.
![]()
Маси ядер можна виміряти з високою точністю за допомогою мас-спектрометра.
Маса атомного ядра завжди виявляється менше суми мас нуклонів.
Це явище називають дефектом мас.
Дефект маси – це різниця між сумою мас нуклонів, що містяться в ядрі і масою ядра.
Дефект маси обумовлений енергією зв'язку ядра, Eзв,
яка виділяється в результаті з'єднання нуклонів в ядрі .
Обчислити енергію зв'язку можна, лише застосовуючи співвідношення Ейнштейна між масою та енергією
![]()
- Дефект мас вимірюють в а.о.м., оскільки в таблицях відносні атомні маси наведені саме в а.о.м.
- Енергію зв’язку вимірюють в МеВ
![]()
![]()
![]()
-
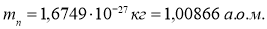 Маса нейтрона:
Маса нейтрона:
![]()
- Маса протона:
-
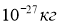 Атомна одиниця маси:
Атомна одиниця маси:
- 1 а.о.м.=1,6605∙
- Важливим параметром ядра є питома енергія зв'язку – це енергія зв'язку , що припадає на один нуклон ядра
Питома енергія зв’язку була виміряна експериментально практично для всіх ядер
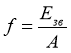
VI. Застосування нових знань
- Виконання вправ
- Як визначити кількість електронів в атомі?
- У ядрі атома певного хімічного елемента 31 протон і 39 нейтронів. Що це за елемент?
-
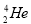
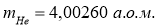 Обчисліть питому енергію зв'язку ядра Гелію ( ).
Обчисліть питому енергію зв'язку ядра Гелію ( ).
- Визначити нуклонний склад ядра Магнію, Цинку, Оксигену.
- Назвати хімічні елементи, у атомному ядрі яких міститься відповідно три протони і чотири електрони, п’ять протонів і шість нейтрони.
VIІ. Домашнє завдання
\Вивчити §44 (В.Д.Сиротюк)
§ 39 (В.Г.Бр᾽яхтар)
Вправа №3.44, 3.47 (В.Д.Сиротюк)
VIII. Підсумок уроку.
Гра «Так – ні»
Для ефективного засвоєння нового матеріалу ви мали повторити дома тему «Електричне поле». Я зачитую твердження.
Якщо відповідь правильна – піднімаєте зелену картку, якщо ні – червону.
- Існують два види зарядів: позитивні і негативні. (так)
- Два однойменні заряди відштовхуються. (так)
- Найменший заряд має частинка йон. (ні)
- За звичайних умов атом електрично нейтральний. (так)
- Усі тіла складаються з дрібних частинок, атомів. (так)
- В центрі атома знаходиться ядро. (так)
- Електрон має позитивний заряд. (ні)
- Ядро атома має негативний заряд. (ні)

про публікацію авторської розробки
Додати розробку
