Конспект уроку з хімії для 7 класу на тему: "Вода, склад молекули, поширеність у природі, фізичні властивості. Вода — розчинник."
№ 35
Дата: ______________
 Тема: Вода, склад молекули, поширеність у природі, фізичні властивості. Вода — розчинник.
Тема: Вода, склад молекули, поширеність у природі, фізичні властивості. Вода — розчинник.
Очікувані результати: учень називає склад молекули води; описує поширеність води у природі, фізичні властивості води; використовує здобуті знання та навички в побуті для раціонального використання води та збереження довкілля.
Тип уроку: засвоєння нових знань.
Методи навчання: словесні, наочні, практичні.
Клас: 7 клас.
Перебіг уроку
I. Організаційна частина.
II. Аналіз контрольної роботи.
ІІІ. Актуалізація опорних знань.
Вода – найпоширеніша сполука на нашій планеті. Вона вкриває понад 2/3 поверхні Землі. Приблизно 97 % усієї води – це вода морів і океанів. На прісну воду припадає 3 %. Річки і озера містять лише всього 0,03 % всієї води.
Вода – це єдина речовина на планеті Земля, що міститься одночасно у трьох агрегатних станах: твердому, рідкому і газоподібному.
Масова частка води в живих організмах становить від 50 % до 99 % (в організмі дорослої людини її приблизно 65 %).
Природна вода завжди містить домішки. А от про склад дистильованої води нам допоможе дізнатися такий віршик:
Вода благоволила литься…
Она блистала, столь чиста,
Что ни напиться, ни умыться.
И это было неспроста.
Ей не хватало ивы, тала
И горечи цветущих лоз.
Ей водорослей не хватало,
И рыбы, жирной от стрекоз.
Ей не хватало быть волнистой,
Ей не хватало течь везде.
Ей жизни не хватало, чистой
Дистиллированной Воде.
Якщо всю воду Землі розподілити рівним шаром по всій поверхні, то утворився б Світовий океан глибиною 4 км.
IV. Вивчення нового матеріалу.
Будова молекули води:
Молекула води має кутову будову. Щоправда, кут між прямими, що з'єднують центри атомів Гідрогену й Оксигену, становить не 90°, а 104,5°:
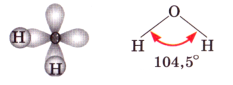
Оскільки Оксиген електронегативніший за Гідроген, то спільні електронні пари зміщені від двох атомів Гідрогену до атома Оксигену. Зв'язки О-Н є полярними. На атомі Оксигену зосереджений невеликий негативний заряд, а на кожному з двох атомів Гідрогену – позитивний:
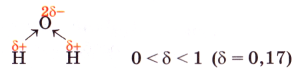
 Отже, молекула води з боку атома Оксигену заряджена негативно, а з протилежного боку, де розміщені атоми Гідрогену, - позитивно. Таку молекулу називають полярною; вона є диполем, тобто має два різнойменно заряджені полюси. Її умовно зображають еліпсом зі вписаними знаками «+» і «-» без зазначення величин зарядів:
Отже, молекула води з боку атома Оксигену заряджена негативно, а з протилежного боку, де розміщені атоми Гідрогену, - позитивно. Таку молекулу називають полярною; вона є диполем, тобто має два різнойменно заряджені полюси. Її умовно зображають еліпсом зі вписаними знаками «+» і «-» без зазначення величин зарядів:
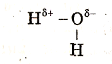
Тип зв'язку – ковалентний полярний, кут зв'язку - 104,5°.
Тип кристалічної ґратки – молекулярний.
- Ґратка молекулярна? Чому ж за нормальних умов вода рідина?
Молекула води полярна – диполь. Між молекулами води виникає взаємне притягання за температури менш ніж 100 °С. Такий зв'язок називається водневим.
Розглядаємо схему водневого зв'язку між молекулами води.
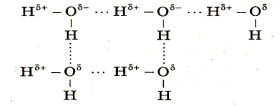
Такий зв'язок можливий між молекулами води й молекулами полярних розчинених речовин. Така особливість молекул води – одна з причин її розчинної сили.
Водневі зв’язки існують і в рідкій воді, й у льду. Кожна молекула Н2О сполучена водневими зв’язками з чотирма іншими:

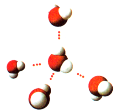
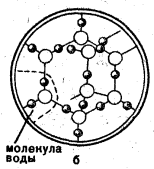
Кристали льоду:
а – сніжинка; б – кристалічна структура води.
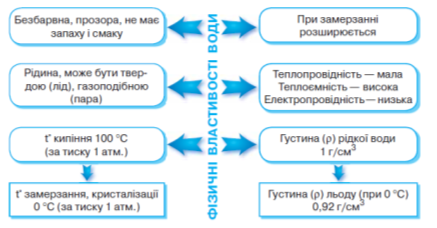
Фізичні властивості води:
Вода здатна зберігати пам'ять про об’єкти з якими була в близькості, або торкалась до яких. Ця властивість обумовлює здатність, що будь-яку воду можна структурувати, при цьому надати їй певні специфічні властивості.
Особливими властивостями води є висока теплоємність і розширення при охолодженні. Під теплоємністю води розуміють кількість теплоти, необхідної для того, щоб нагріти чи охолодити 1 г води на 1 °С.
При замерзанні вода розширюється, а не стискається, як усі інші речовини й тіла. Тому небезпечно залишати воду в закритій скляній посудині на морозі — замерзаючи, вода її зруйнує. Подібним чином відбувається руйнування гірських порід водою, яка потрапляє в їх тріщини.
Густина води при її замерзанні зменшується, тому лід плаває на поверхні водойм і захищає воду глибинних шарів від промерзання та втрат тепла.
Воду, яка не містить домішок інших речовин, називають хімічно чистою. Така вода погано проводить тепло й електричний струм. Та за наявності навіть невеликої кількості розчинених речовин (а вони завжди присутні у природній воді) ці якості води проявляються певним чином.
Вода, яку ви використовуєте щодня, не позбавлена інших розчинених вній речовин, тому добре проводить електричний струм. Тож слід обережно поводитися з електроприладами, якщо у вас мокрі руки.
Лід має густину 0,92 г/см3 (Інші речовини у твердому стані мають більшу густину, ніж у рідкому)
- цікавим є той факт про який навіть не всі вчені-хіміки знають – без наявності води у бензині він не буде горіти.
Вода – універсальний розчинник усіх речовин на Землі.
Вода річок, озер і деяких джерел містить розчинених речовин менше 1 г в 1 літрі (позначають 1 г/л), тому її називають прісною. Вміст солей у воді морів і океанів значно більший. Так, у Чорному морі їх близько 18 г/л, а в Червоному — близько 41 г/л. Таку воду називають солоною, або морською.
Розчинені речовини й гази входять до складу підземних вод. Деякі з них мають лікувальні властивості й відомі вам під назвою мінеральні води, наприклад «Миргородська», «Моршинська», «Поляна квасова».
Застосування води (робота з текстом підручника).
IV. Узагальнення і систематизація знань та вмінь учнів.
Згадуємо властивості води (на підставі знань про воду заповнюємо опорну схему).
Молекулярна формула:__________
Структурна формула:____________
М/н2о = _______________________
Поширення в природі
В організмі людини: _______
На Землі:_________________
Фізичні властивості
V. Підсумок уроку.
А вода – це справжнє диво!
Як прожити без води?
З нею ми завжди щасливі,
З нею в нас нема біди.
Є вода – ростуть рослини:
Ліс, сади, рясні поля.
Це чудово для людини
І радіє вся Земля!
VІ. Домашнє завдання.
Опрацювати §
Підготувати повідомлення на тему:
- «Значення води в житті людини»;
- «Проблема чистої води»;
- «Різноманітність мінеральних джерел України».
-
Дуже цікавий урок. Зібрано багато матеріалів до теми, але 7 клас ще не знає, що таке ковалентний зв'язок, кристалічна ґратка, електронегативність(((
-
дякую


про публікацію авторської розробки
Додати розробку
